(1)实验室制取Cl2的反应方程式之一为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O被氧化的盐酸占反应盐酸总量的 ,当标准状况下有11.2L氯气生成时,该反应的电子转移数为 。
(2)用双线桥法标出电子转移情况:3BrF3+5H2O=HBrO3+Br2+O2+9HF,当180g水都做还原剂时,被自身还原的BrF3是 mol。
(3)已知下列两个氧化还原反应:O2+4HI=2I2+2H2O 及Na2S+I2=2NaI+S,则三种单质的氧化性由强到弱的顺序为:
已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是________,被氧化的离子的物质的量分别是________________。
(2)如果向原溶液中通入3 mol Cl2,则被氧化的离子是________,其对应氧化产物的物质的量分别是________________。
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2:S2O82—+2I-=2SO42—+I2。通过改变反应途径,Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应的催化过程:______________________________、____________________________(不必配平)。
(1)写出下列反应的离子方程式:
①氯化铵溶液和氢氧化钠溶液反应 ;
②少量二氧化碳通入澄清石灰水 ;
③三氧化二铁和盐酸反应 。
(2)铜和浓硫酸发生反应的化学方程式为:Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O,其中硫元素被________(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_________剂,具有 性。
CuSO4+SO2↑+2H2O,其中硫元素被________(填“氧化”或“还原”,下同),发生 反应;浓H2SO4作_________剂,具有 性。
(1)①在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,这是因为________,离子方程式__________________________。
②在碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,这是因为________________________。离子方程式是_______________________。
③对比①和②实验所得的结果,将I2、ClO-、SO42—按氧化性由强到弱的顺序排列为________________________________________。
(2)今有铁片、铜片,设计实验证明以下事实,并写出反应的化学方程式。
①浓硫酸的氧化性比稀硫酸强。___________________________。
②氯化铁溶液中Fe3+的氧化性比硫酸铜溶液中的Cu2+强。__________________________________________。
③铁的还原性比铜强。_________________________。
(1)已知反应MnO2+4HCl (浓) MnCl2+Cl2↑+2H2O中,若二氧化锰与足量的浓盐酸反应制得3.55gCl2,通过计算回答:用双线桥标出反应中电子转移的方向和数目 ,参加反应的HCl的物质的量为 ,其中被氧化的HCl的质量 。
MnCl2+Cl2↑+2H2O中,若二氧化锰与足量的浓盐酸反应制得3.55gCl2,通过计算回答:用双线桥标出反应中电子转移的方向和数目 ,参加反应的HCl的物质的量为 ,其中被氧化的HCl的质量 。
(2)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、 H3AsO4、H2O和一种未知物质X。
①已知KBrO3在反应中得到电子,则该反应的还原剂是____________________。
②已知0.2 mol KBrO3在反应中得到1 mol电子生成X,则X的化学式为_______,写出一个包含上述七种物质的氧化还原反应方程式(不需配平)_________ ________。
③根据上述反应可推知( )
| A.氧化性:KBrO3>H3AsO4 | B.氧化性:H3AsO4>KBrO3 |
| C.还原性:AsH3>X | D.还原性:X>AsH3 |
氰(CN)2、硫氰(SCN)2的化学性质和卤素很相似,化学上称为“类卤素”,它们阴离子的还原性强弱为:Cl﹣<Br﹣<CN﹣<SCN﹣<I﹣.
试写出:
(1)(CN)2与KOH(aq)反应的化学方程式: ;
(2)NaBr和KSCN的混合溶液中加入足量(CN)2反应的离子方程式: .
有反应:
①2H2O+Cl2+SO2====H2SO4+2HCl
②2KMnO4+16HCl====2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)两反应中的氧化剂的氧化性强弱顺序为 ,
还原剂的还原性强弱顺序为 。
(2)反应①中氧化产物和还原产物质量比为 。
分析下列反应:5KCl + KClO3 + 3H2SO4 = 3Cl2↑+ 3K2SO4 + 3H2O,据此作答:
(1)标出该反应中电子的转移方向和数目:
5KCl + KClO3 + 3H2SO4 = 3Cl2↑+ 3K2SO4 + 3H2O
(2)该反应的氧化剂是 。
(3)该反应的氧化产物与还原产物的质量比是 。
(4)当反应生成0.3 mol Cl2时,则转移的电子的物质的量是 。
(每空1分,共11分)从下列各组反应对比,判断那种微粒的氧化性最强。
(1)铁钉浸入硫酸铜溶液中后,表面会附有红色物质,铜丝浸入硝酸银溶液后,表面会附有银白色物质。则铜、铁、银中,_____ ___原子的还原性最强;Cu2+、Ag+、Fe2+中, 离子的氧化性最强。
(2)在氯气中Fe锈蚀成棕褐色物质FeCl3,而在盐酸中生成淡绿色溶液FeCl2。则氯气分子、氢离子、氯离子中, 具有氧化性, 氧化性最强。请书写出以上各反应的化学方程式________ 、 。
(3)已知在ⅣA族元素中,Pb2+和Sn4+的化合物较为稳定。
①据此可判断PbO2具有较强的________性,SnCl2具有较强的 性;写出PbO2溶于盐酸的离子方程式__________;写出SnCl2和FeCl3溶液混合的离子方程式__________ ;
②PbO2、Fe3+、Cl2、Sn4+氧化性由强到弱的顺序是__________ 。
)(1)2KClO3=2KCl+3O2↑ 是氧化剂, 是还原剂; 元素被氧化, 元素被还原; 是氧化产物, 是还原产物;并用双线桥法标出这个反应的电子转移方向和数目。
2KClO3=2KCl+3O2↑
(2)已知反应:
①MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O
②Cl2+SO2+2H2O=H2SO4+2HCl
1)两反应中的氧化剂的氧化性强弱顺序为 ;
2)反应②中氧化剂与还原剂的物质的量之比为 ;
3)反应①的离子方程式 ;
4)用174kg MnO2通过①②两反应可以处理SO2的质量为 。
高锰酸钾是一种典型的强氧化剂。完成下列填空:
I:在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO4-+Cu2S+H+ Cu2++SO2↑+Mn2++H2O(未配平)
Cu2++SO2↑+Mn2++H2O(未配平)
② MnO4-+CuS +H+ Cu2++SO2↑+Mn2++H2O(未配平)
Cu2++SO2↑+Mn2++H2O(未配平)
(1)下列关于反应①的说法中错误的是 (填字母序号)。
a.被氧化的元素是Cu和S
b.氧化剂与还原剂的物质的量之比为8∶5
c.生成2.24 L(标况下)SO2,转移电子的物质的量0.8 mol d.还原性的强弱:Mn2+>Cu2S
II:在稀硫酸中,KMnO4与 (NH4)2Fe(SO4)2也能发生氧化还原反应。
(2)写出KMnO4与(NH4)2Fe(SO4)2反应的离子方程式: 。
(3)欲配制480mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为 g。需要的玻璃仪器有 .
III:实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:高温下使软锰矿与过量KOH(s)和KClO3(s)反应,生成K2MnO4(锰酸钾)和KCl;用水溶解,滤去残渣;酸化滤液,K2MnO4转化为MnO2和KMnO4;再滤去沉淀MnO2,浓缩结晶得到KMnO4晶体。请回答:
(4)用软锰矿制备K2MnO4的化学方程式是: 。
(5)K2MnO4转化为KMnO4的反应中氧化剂和还原剂的物质的量之比为 。并用单线桥表示电子的转移情况 。
分析下列反应:3S+6 KOH = 2K2S+K2SO3+3H2O,据此作答:
(1)用双线桥标出该反应中电子的转移方向和数目:3S +6 KOH = 2K2S+K2SO3+3H2O
(2)该反应的氧化产物是 。
(3)该反应的氧化剂与还原剂的质量比是 。
(4)当消耗0.3 mol S时,则转移的电子数是 。
下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②KClO3+6HCl=3Cl2↑+KCl+3H2O
③KMnO4+HCl(浓)—KCl+MnCl2+Cl2↑+H2O(未配平),
根据以上三个反应,回答有关问题:
(1)反应的②的离子方程式为________________。
(2)反应②中,氧化产物与还原产物的质量比为____________。
(3)请将反应③配平:__KMnO4+__HCl(浓)=__KCl十__MnCl2+__Cl2↑+__H2O
(4)若要制得相同质量的氯气,①②③反应中电子转移的数目之比为_________。
(5)已知反应④:4HCl(g)+O2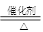 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为________________。
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为________________。
过氧化氢H2O2(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
| A.Na2O2 +2HCl= 2NaCl+H2O2 |
| B.Ag2O+ H2O2=2Ag+O2+ H2O |
| C.2 H2O2="2" H2O+O2 |
| D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O |
(1)H2O2仅体现氧化性的反应是(填代号) 。
(2)H2O2既体现氧化性又体现还原性的反应是(填代号) 。
(3)B反应式中的氧化产物是 。
(4)上述反应说明H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是: 。
试题篮
()