25℃时,(1)、将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”,“中性”或“碱性”,下同),溶液中c(Na+) c(CH3COO-)(填“ >” 或“=”或“<” )。
(2)、pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 ,
溶液中c(Na+) c(CH3COO-)
(3)、物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 ,醋酸体积 氢氧化钠溶液体积。
(4)、将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后溶液的pH=7,则醋酸溶液中c(H+) 氢氧化钠溶液中c(OH-),m与n的大小关系是m n。
(5)、相同物质的量浓度的NH4HSO4和(NH4)2SO4溶液,都呈 性,前者显酸性的主要原因是 ;后者显酸性的主要原因是 。
25℃时,下图烧杯中各盛有25 mL的溶液。
甲 乙 丙
(1)甲溶液pH=_______。
(2)若将甲溶液全部倒入乙中,所得的混合溶液的pH(填“>”、“<”或“=”)_______
丙溶液的pH。
(3)若将乙溶液全部倒入丙中,所得的混合溶液pH>7,所得溶液中离子浓度大小顺序是 _______。
用0.1 mol·L-1 NaOH溶液分别滴定体积均为20 mL、浓度均为0.1 mol·L-1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图:

(1)HX为 酸(填“强”或“弱”)。
(2)N点pH>7的原因是(用化学用语表示)______________。
(3)下列说法正确的是__________(填字母)。
a. M点c(HX)<c(X-)
b. M点c(Na+)>c(OH-)
c. P点c(Cl-)=0.05 mol·L-1
某温度(t℃)时,水的KW=10-13,则该温度(填大于、等于或小于)______25℃,理由是_________________________________________________,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
(1)若所得混合溶液为中性,则a:b=_________;
(2)若所得混合溶液pH=2,则a:b=__________。
在温度T下,c(OH-)=0.1 mol·L-1的Ba(OH)2的PH值为11。
(1)该温度下,100ml水中含有OH-约有_ 个。
(2)该温度下,在PH=8的Ba(OH)2溶液中加入PH=5的盐酸,欲使混合溶液pH=7,则Ba(OH)2溶液与所加盐酸的体积比为__ __
(1) 常温下,0.10 mol/L NH4Cl溶液pH______7(填>、=或<),溶液中各离子浓度由大到小的顺序是______ ________________________。
________________________。
(2) 相同物质的量浓度的 Na2CO3溶液与NaHCO3溶液,pH大小: Na2CO3_______NaHCO3(填>、=或<),两种溶液中微粒种类:Na2CO3_______NaHCO3(填>、=或<)。
Na2CO3溶液与NaHCO3溶液,pH大小: Na2CO3_______NaHCO3(填>、=或<),两种溶液中微粒种类:Na2CO3_______NaHCO3(填>、=或<)。
(3) Na2S溶液呈碱性的原因是________________________________(写出有关的离子方程式,下同),Al2(SO4)3溶液呈酸性的原因是_______________________________,普通泡沫灭火器是利用NaHCO3溶液跟Al2(SO4)3溶液混合,产生大量的气体和沉淀,气体将混合物压出灭火器,相关反应的离子方程式是________________________________。
已知某溶液中只存在OH-、H+、NH、Cl-四种离子,某同学推测其离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c(NH)>c(H+)>c(OH-) ②c(NH)>c(OH-)>c(Cl-)>c(H+)
③c(NH)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH)>c(OH-)
填写下列空白
(1)若溶液中只溶解一种溶质,则该溶质是________,上述四种离子浓度的大小顺序为(填序号)________;
(2)若四种离子的关系符合④,则溶质为________;
(3)则pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数,下列图像正确的是(填图像符号)________;
(4)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________c(NH3·H2O)(填“大于”“小于”或“等于”)
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 |
HA物质的量浓度(mol·L-1) |
NaOH物质的量浓度(mol·L-1) |
混合溶液的pH |
| ① |
0.1 |
0.1 |
pH=9 |
| ② |
c |
0.2 |
pH=7 |
| ③ |
0.2 |
0.1 |
pH<7 |
请回答:
(1) 从①组情况分析, HA是 酸(选填“强”、“弱”)。
(2) ②组情况表明,c 0.2 (填“>”、“=”或“<”)。
(3) 从③组实验结果分析,说明HA的电离程度______NaA的水解程度(填“>”、“=”或“<”),该混合溶液中离子浓度由大到小的顺序是 。
(4) ①组实验所得混合溶液中由水电离出的c(OH-)= mol·L-1。
常温下,将四种不同的一元酸(用 HA 代表)分别和 NaOH 溶液等体积混合。 两种溶液的物质的量浓度和混合溶液的 pH 如下表所示:
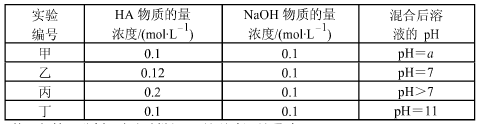
(1)从甲组情况分析,如何判断 HA 是强酸还是弱酸?________________。
(2)乙组混合溶液中粒子浓度 c(A-)和 c(Na+)的大小关系_____________。
A.前者大 B.后者大 C.两者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是:___________
(4)分析丁组实验数据,写出混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=_______mol·L-1。
(5) 某二元酸(化学式用 H2B 表示)在水中的电离方程式是:
H2B===H++HB- HB- H++B2-
H++B2-
回答下列问题:
在 0.1 mol·L-1的 Na2B 溶液中,下列粒子浓度关系式正确的是________。
A.c(B2-)+c(HB-)=0.1 mol·L-1
B.c(B2-)+c(HB-)+c(H2B)=0.1 mol·L-1
C.c(OH-)=c(H+)+c(HB-)
D.c(Na+)+c(H+)=c(OH-)+c(HB-)
(1)常温下,0.1 mol/L的醋酸和0.1 mol/L的盐酸各100 mL,分别与足量的锌粒反应,产生的气体体积前者 后者(填“<”、“>”或“=”).
(2)将体积和物质的量浓度都相同的醋酸和氢氧化钠溶液混合后,溶液呈 性(填“酸”,“中”或“碱”下同),溶液中 c(Na+ ) c(CH3 COO- )(填“ >” 或“=”或“<”,下同 )。
(3)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 性,溶液中c(Na+) c(CH3COO- )
(4)用Al2(SO4)3 与NaHCO3 溶液混合反应就是泡沫灭火器的工作原理,请写出反应的离子方程式___________。
某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿制取活性ZnO的方案,实现废物综合利用,方案如图所示。

已知:298K时各离子开始沉淀及完全沉淀时的pH如下表所示。
| 离子 |
开始沉淀时的pH |
完全沉淀时的pH |
| Fe2+ |
6.34 |
9.7 |
| Fe3+ |
1.48 |
3.2 |
| Zn2+ |
6.2 |
8.0 |
请回答下列问题:(1)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,这是由于相同温度下:Ksp(CuS) Ksp(ZnS)(选填“>”“<”或“=”)。
(2)你认为在除铁过程中选用下列物质中的 (填序号)作为试剂甲是比较合适的。
A.KMnO4 B.HNO3 C.H2O2 D.Cl2
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在 范围之间。
(4)请写出加甲物质后,加入氨水控制调节溶液的pH生成Fe(OH)3反应的离子方程式 。
(5)298K时残留在乙溶液中的c(Fe3+)在 mol/L以下。Fe(OH)3的KSP= 2.70×10-39
(6)乙的溶液可直接用作氮肥,则乙的化学式是 。
(7)请写出“沉淀Zn2+”步骤中发生反应的化学方程式
(8分)某温度下,纯水的c(H+)=2×10-7 mol·L-1,则此时c(OH-)为 ;若温度不变,滴入稀盐酸使c(H+)=5×10-4 mol·L-1则溶液中c(OH-)为 ,由水电离产生的c(H+)为 ,此时温度_____(填“高于”、“低于”或“等于”)25℃。
试题篮
()