将pH=3的盐酸a L分别与下列三种溶液混合后,混合液均呈中性;①1×10-3 mol·L-1的氨水b L;②c(OH-)=1×10-3 mol·L-1的氨水c L;③c(OH-)=1×10-3 mol·L-1Ba(OH)2的溶液d L;则a、b、c、d的关系正确的是
| A.b>a=d>c | B.a=b>c>d | C.a=b>d>c | D.c>a=d>b |
40℃时,在氨-水体系中不断通入CO2,各种离子变化趋势如下图所示。下列说法不正确的是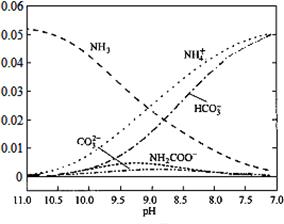
| A.在pH=9.0时,c(NH4+)>c(HCO3-)>c(NH2COOˉ)>c(CO32-) |
| B.不同pH的溶液中存在关系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COOˉ)+c(OHˉ) |
C.随着CO2的通入,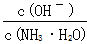 不断增大 不断增大 |
| D.在溶液中pH不断降低的过程中,有含NH2COOˉ的中间产物生成 |
常温下,0.1 mol·L-1某一元酸(HA)溶液的pH=3。下列叙述正确的是
A.该溶液中:c2(H+)≠c(H+)·c(A-)+Kw
B.0.1 mol·L-1 HA溶液与0.05 mol·L-1 NaOH溶液等体积混合,所得溶液中:
2c(H+)+c(HA)===c(A-)+2c(OH-)
C.浓度均为0.1 mol·L-1的HA和NaA溶液等体积混合,所得溶液中:
c(A-)>c(HA)>c(Na+)>c(OH-)>c(H+)
D.由pH=3的HA溶液与pH=11的NaOH溶液等体积混合,所得溶液中:
c(Na+)>c(A-)>c(OH-)>c(H+)
(1)常温下将0.2mol/L HCl溶液与0.2mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,混合溶液中由水电离出的c(H+)_______0.2mol/LHCl溶液中由水电离出的c(H+)(填“>”、“<”、或“=”) 。
(2)常温下若将0.2mol/L MOH溶液与0.1mol/L HCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度__________MCl的水解程度。(填“>”、“<”、或“=”)
(3)常温下若将0.1mol/L的HR溶液与0.1mol/L的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH_____________。(填“>7”、“<7”、或“无法确定”)
(4)用0.1000mol/L HCl溶液滴定未知浓度的NaOH溶液,重复三次的实验数据如下所示
| 实验序号 |
0.1032mol/L HCl溶液体积/mL |
待测NaOH溶液体积/mL |
| 1 |
27.83 |
25.00 |
| 2 |
26.53 |
25.00 |
| 3 |
27.85 |
25.00 |
①待测NaOH溶液的物质的量浓度为________________mol/L。(保留四位有效数字)
②下列情况可能引起测定结果偏高的是____________。
A.酸式滴定管未用标准盐酸溶液润洗 B.滴定前滴定管尖嘴中有一气泡,滴定后气泡消失了
C.锥形瓶未用待测液润洗 D.酸式滴定管滴定前平视读数,滴定后俯视读数
(5)滴定的方法有酸碱中和滴定、沉淀滴定、络合滴定等.沉淀滴定所用的指示剂本身就是一种沉淀剂.已知一些银盐的颜色和Ksp(20℃)如下,测定水体中氯化物的含量,常用标准硝酸银溶液进行滴定.
| 化学式 |
AgCl |
AgBr |
AgI |
Ag2S |
Ag2CrO4 |
| 颜色 |
白色 |
浅黄色 |
黄色 |
黑色 |
红色 |
| Ksp |
1.8×10﹣10 |
5.0×10﹣13 |
8.3×10﹣17 |
2.0×10﹣48 |
1.8×10﹣10 |
滴定时,你认为该滴定适宜选用的指示剂是下列中的_________________。
A.KBr B.KI C.K2S D.K2CrO4
下列说法不正确的是( )
| A.0.2 mol•L﹣1的NaHCO3溶液中:c(Na+)>c(HCO3﹣)>c(OH﹣)>c(H+)>c(CO32﹣) |
| B.将等体积pH=4的盐酸和醋酸稀释成pH=5的溶液,盐酸需加的水量多 |
| C.向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+)=c(Cl﹣) |
| D.pH=1的NaHSO4溶液:c(H+)= c(SO42﹣)十c(OH﹣) |
下列说法正确的是( )
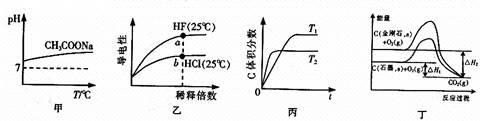
| A.由图甲可知,升高温度醋酸钠的水解程度增大 |
| B.由图乙可知,a点Kw的数值比b点Kw的数值大 |
C.由图丙可知,反应A(g)+B(g) 2C(g)是吸热反应 2C(g)是吸热反应 |
| D.由图丁可知,反应C(金刚石,s) = C(石墨,s)的焓变△H =△H1-△H2 |
物质的量浓度相同的下列溶液中:①NH4Cl ②(NH4)2CO3 ③(NH4)2SO4 ④NH4HSO4 ⑤NH4HCO3c(NH)由大到小的顺序是( )
| A.⑤②③①④ | B.④①③②⑤ | C.③②①⑤④ | D.③②④①⑤ |
物质的量浓度相同(0.1mol/L)弱酸HX和NaX溶液等体积混合后,溶液中微粒关系错误是 ( )
| A.c(Na+)+c(H+)=c(X﹣)+c(OH﹣) |
| B.c(HX)+c(X﹣)=2c(Na+) |
| C.若溶液显酸性,则有:c(X﹣)>c(Na+)>c(HX)>c(H+)>c(OH﹣) |
| D.若溶液显碱性,则有:c(Na+)>c(HX)>c(X﹣)>c(OH﹣)>c(H+) |
常温下,如果取0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液中由水电离出的c(H+)_______0.1mol/L NaOH溶液中由水电离出的c(H+) (填“>”、“<”或“=”)
(2)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断:NH4HCO3溶液的pH_______7(填“大于”、“小于”或“等于”);
(3)将同温度下等浓度的四种盐溶液:
A.NH4HCO3 B.NH4A C.(NH4)2SO4 D.NH4Cl
按pH由大到小的顺序排列是:__________________________(填序号)
(4) 求出混合液中下列算式的精确计算结果(填具体数字):
c(Na+)-c(A-)=_________mol/L,c(OH−)-c(HA)=_________mol/L
现有25 ℃时,0.1 mol/L的氨水。请回答下列问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中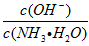 ________。(填“增大”、“减小”或“不变”)。
________。(填“增大”、“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好完全中和,写出反应的离子方程式:___________________;所得溶液的pH________7(填“<”、“>”或“=”),用离子方程式表示其原因_______________。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH)=a mol/L,则c(SO)=____________。
(4)若向氨水中加入pH=1的硫酸溶液,且氨水与硫酸溶液的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的顺序是___________________________________。
下列溶液中有关物质的量浓度关系正确的是( )
A.NaHSO3溶液呈酸性,则有:c(Na+)>c(HSO3-)>c(SO32-)>c(H+)>c(OH−)
B.pH相等的CH3COONa和Na2CO3两种溶液:c(CH3COONa)<c(Na2CO3)
C.强酸HA溶液与弱碱MOH溶液混合后溶液呈中性,则c(M+)=c(A-)
D.0.1 mol/L的 NaHA 溶液pH=1则c(Na+)=c(H2A)+c(HA-)+c(A2-)
(1)稀释0.1 mol·L-1氨水时,随着水量的增加而减小的是 (填写序号)。
① ②
② ③c(H+)和c(OH-)的乘积 ④OH-的物质的量
③c(H+)和c(OH-)的乘积 ④OH-的物质的量
(2)pH相同的等体积的A、B两份溶液(A为盐酸,B为醋酸)分别与锌粉反应,若最后仅有一份溶液中存在锌粉,且放出氢气的质量相同,则下列说法正确的是________(填写序号)。
①反应所需的时间B>A ②开始反应时的速率A>B
③参加反应的锌粉物质的量A=B ④反应过程中的平均速率B>A
⑤A溶液里有锌粉剩余 ⑥B溶液里有锌粉剩余
(3)将等体积、等物质的量浓度的氨水和盐酸混合后,升高温度(溶质不会分解)溶液的pH随温度变化是图中的_________曲线(填写序号) 。

(4)室温下,向0.1mol·L-1的盐酸与0.2mol·L-1 的氨水等体积混合,则所得溶液中所有离子物质的量浓度由大到小的顺序为______________ 。
(5)由电离常数可知酸性强弱:CH3COOH>H2CO3>HCO3-,则浓度相同的下列溶液碱性由强到弱顺序为: (填序号)
①CH3COONa ②NaHCO3 ③Na2CO3
(6)氯化铁溶液呈酸性的原因是(用离子方程式表示): 。
某二元酸(化学式用H2B表示)在水中的电离方程式是:H2B=H++HB-;HB- H++B2-
H++B2-
完成下列问题:在0.1 mol/L 的Na2B溶液中,下列粒子浓度关系式正确的是 。
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol/L B.c(Na+)+c(OH-)=c(H+)+c(HB-)
C.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-) D.2c(Na+)=c(B2-)+c(HB-)
向体积为Va的0.05mol·L-1CH3COOH溶液中加入体积为Vb的0.05mol·L-1KOH溶液,下列关系正确的是
| A.Va= Vb时:c(CH3COO-)= c(K+) |
| B.Va<Vb时:c(CH3COOH)+ c(H+)= c(OH-) |
| C.Va>Vb时:c(CH3COO-) > c(K+) > c(OH-) > c(H+) |
| D.Va与Vb任意比时:c(K+) + c(H+)= c(OH-) + c(CH3COO-) |
下列关于溶液的说法错误的有几个
①NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大
②浓度均为0.1 mol/L的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)]
③在0.1 mol/L氨水中滴加0.l mol/L盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-a mol/L
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
| A.2个 | B.3个 | C.4个 | D.5个 |
A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互的转化关系如下图所示。请回答下列问题: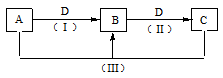
(1)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一.
①A中所含化学键类型为___________,D的电子式为___________;
②25℃时,0.1mol•L-1 B、C溶液,pH较大的是___________溶液(填溶质的化学式),写出B溶液中显电中性的原因___________,已知,B溶液里的pH=10,则其水电离出来的H+的浓度为________________。
(2)向反应体系中同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
I.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1=-802.6kJ/mol
II.CH4(g)+O2(g)═CO2(g)+2H2(g)△H2=-322.0kJ/mol
III.CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.2kJ/mol
Ⅳ.CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H4=+165.0kJ/mol
请回答下列问题:
①CH4的燃烧热△H________△H1.(填“>”、“<”或“=”);
②在反应初始阶段,反应II的反应速率大于反应III的反应速率.比较反应II的活化能EII和反应III的活化能EIII的大小:EII________EIII(填“>”、“<”或“=”)。
试题篮
()