向1000mL3mol·L-1NaOH中通入适量CO2气体,溶液中有关阴离子的物质的量变化曲线如图所示:
下列说法张正确的是
| A.水的电离程度一直增大 |
| B.溶液的pH逐渐下降 |
| C.M、N两点对应的溶液中离子种类不同 |
| D.CD段反应的离子方程式为OH-+CO2=HCO3- |
已知常温下:PH(NaHCO3)>7>PH(NaHSO3)。则在NaHCO3或NaHSO3溶液中,有关微粒的物质的量浓度表示式一定正确的是(X表示S或C)( )
A.C(Na+)>C(HXO3-)>C(OH-)>C(H2XO3)>C(XO32-)
B.C(Na+)+C(H+)=C(OH-)+C(XO32-)+C(HXO3-)
C.C(H2XO3)+C(HXO3-)+C(XO32-)=C(Na+)
D.C(OH-)=C(H+)+C(HXO3-)+C(H2XO3)
下列说法正确的是
| A.0.1 mol·L-1的NaHS溶液中离子浓度关系:c (OH-)="c" (H+)-c (S2-)+c (H2S) |
| B.0.1 mol·L-1的NH4Cl和0.1 mol·L-1的NH3·H2O等体积混合后,溶液中的离子浓度关系:c (Cl-)>c (NH4+)>c (H+)>c (OH-) |
| C.常温下,醋酸钠溶液中滴加少量盐酸使溶液的pH=7,则混合溶液中,离子浓度关系:c (Na+)="c" (CH3COO-)>c (OH-)=" c" (H+) |
| D.0.1 mol·L-1的Na2CO3溶液中离子浓度关系:c (Na+)="2c" (CO32-)+c (HCO3-)+c (H2CO3) |
下列溶液中微粒的物质的量浓度关系一定正确的是
| A.0.1mol/LNH4Cl溶液与0.05mol/LNaOH溶液等体积混合后所得的碱性溶液中: c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+) |
| B.等物质的量的NaClO、NaHCO3混合溶液中: c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+  c(CO32-) c(CO32-) |
| C.pH=2的HA溶液与pH=12的MOH溶液等体积混合: c(M+)=c(A-)>c(OH-)=c(H+) |
| D.某二元弱酸的酸式盐NaHA溶液:c(Na+)+ c(H+)=c(OH-)+c(HA-)+c(A2-) |
中学化学实验,淡黄色的pH试纸常用于测定溶液的酸碱性。在25 ℃,若溶液的pH=7,试纸不变色;若pH<7,试纸变红色;若pH>7,试纸变蓝色。而要精确测定溶液的pH,需用pH计。pH计主要通过测定溶液中H+浓度来测定溶液的pH。
(1)已知水中存在如下平衡H2O  H++OH- ΔH>0。现欲使平衡向右移动,且所得溶液呈中性,选择的方法是 (填字母)。
H++OH- ΔH>0。现欲使平衡向右移动,且所得溶液呈中性,选择的方法是 (填字母)。
| A.向水中加入NaHSO4溶液 |
| B.向水中加入Cu(OH)2固体 |
| C.加热水至100 ℃[其中c(H+)="1×10-6" mol·L-1] |
| D.在水中加入H2SO4溶液 |
(2)现欲测定100 ℃沸水的pH及酸碱性,若用pH试纸测定,则试纸显 色,若用pH计测定,则pH 7(填“>”“<”或“=”),溶液呈 性(填“酸”“碱”或“中”)。
(3)证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是 (填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸
d.加入品红溶液 e.用蓝色石蕊试纸检测
下列说法错误的是
①NaHCO3溶液加水稀释, 的比值保持增大
的比值保持增大
②浓度均为0.1mol•L﹣1的Na2CO3、NaHCO3混合溶液:2c(Na+)═3[c(CO32﹣)+c(HCO3﹣)]
③在0.1mol•L﹣1氨水中滴加0.lmol•L﹣1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH﹣)=l0﹣amol•L﹣1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32﹣)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH﹣)+c(H2S)+c(HS)
| A.①④ | B.②⑤ | C.①③ | D.②④ |
向体积为Va的0.05 mol·L-1CH3COOH溶液中加入体积为Vb的0.05 mol·L-1KOH溶液,下列关系错误的是
| A.Va>Vb时:c(CH3COOH)+c(CH3COO-)>c(K+) |
| B.Va=Vb时:c(CH3COOH)+c(H+)=c(OH-) |
| C.Va<Vb时:c(CH3COO-)>c(K+)>c(OH-)>c(H+) |
| D.Va与Vb任意比时:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
已知化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。请回答下列问题:
(1)常温下,浓度均为0.1 mol·L-1的下列六种溶液的pH如下表:
| 溶质 |
CH3COONa |
NaHCO3 |
Na2CO3 |
NaClO |
NaCN |
C6H5ONa |
| pH |
8.8 |
9.7 |
11.6 |
10.3 |
11.1 |
11.3 |
①上述盐溶液中的阴离子,结合质子能力最强的是______________
②根据表中数据判断,浓度均为0.01 mol·L-1的下列五种物质的溶液中,酸性最强的是____________;(填编号,下同)将各溶液分别稀释100倍,pH变化最小的是__________
A HCN B HClO C C6H5OH D CH3COOH E H2CO3
③据上表数据,请你判断下列反应不能成立的是 (填编号)。
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为
(2)CaCO3是一种难溶物质,其KSp=2.8×l0-9。现将浓度为2×l0-4 mol/L Na2CO3溶液与CaCl2溶液等体积混合,则生成CaCO3沉淀所需CaCl2溶液的最小浓度为___________mol/L。
常温下,下列溶液中离子浓度关系表达正确的是
| A.Na2CO3溶液中:c(H+)+c(Na+)=c(OH-)+c(CO32-)+c(HCO3-) |
| B.0.1mol/L的Na2CO3溶液中:c(Na+)> c(CO32-) > c(OH-)>c(HCO3-) |
| C.pH=5.3的NaHSO3溶液:c(Na+)>c(HSO3-)>c(H2SO3)>c(SO32-) |
| D.pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后:c(Na+)>c(CH3COO-)+c(OH-)+c(H+) |
无水氯化铝在生产、生活中应用广泛。
(1)氯化铝在水中形成具有净水作用的氢氧化铝胶体,其反应的离子方程式为 ;
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:
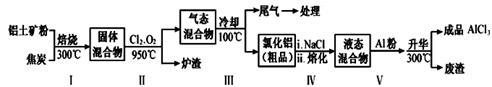
已知:
| 物质 |
SiCl4 |
AlCl3 |
FeCl3 |
FeCl2 |
| 沸点/℃ |
57.6 |
180(升华) |
300(升华) |
1023 |
①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是 (只要求写出一种);
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是 ;
③已知:
Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1="+1344.1kJ" ·mol-1
2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2="+1169.2kJ" ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为 ;
④步骤Ⅲ经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为 ;
⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是 。
下列说法正确的是( )
| A.泡沫灭火器中用的是硫酸铝和苏打溶液,并且苏打放在小塑料桶里。 |
B.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
| C.在常温下用惰性电极电解足量食盐水的实验中,若电解后溶液总体积为0.5L,阴极析出的气体的分子数为0.5NA,电解后溶液的pH为14 |
| D.常温时,浓度均为0.01mol/L Na2CO3溶液和NaHCO3溶液,等体积混合,其溶液中粒子浓度关系为2c(Na+)=3c(HCO3-)+3c(CO32-)+3c(H2CO3) |
室温下,在0.2 mol·L-1 Al2(SO4)3溶液中,逐滴加入1.0 mol·L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积的变化曲线如图所示,下列有关说法正确的是( )

A.a点时溶液呈酸性的原因是Al3+水解,离子方程式为Al3++3OH- Al(OH)3 Al(OH)3 |
| B.a~b段,溶液pH增大,Al3+浓度不变 |
| C.b~c段,加入的OH-主要用于生成Al(OH)3沉淀 |
| D.d点时,Al(OH)3沉淀开始溶解 |
下列关系式中,正确的是
| A.等浓度等体积的CH3COOH和CH3COONa溶液混合:c(CH3COO- )+c(OH -)=c(H+)+c(CH3COOH) |
| B.常温下,0.1 mol·L-1 HA溶液与0.1 mol/LNaOH溶液等体积完全反应时,溶液中一定存在:c(Na+)=c(A- )>c(OH )=c(H+) |
| C.常温下,0.1 mol·L-1 Na2S溶液中存在:c(OH- )=c(H+)+c(HS- )+c(H2S) |
| D.常温下,将0.1 mol·L-1 CH3COOH溶液加水稀释,当溶液的pH从3.0升到5.0时,溶液中c(CHCOO-)/c(CHCOOH)的值增大到原来的100倍 |
有①CH3COOH、②HCl、③H2SO4三种溶液,下列说法不正确的是
| A.pH相同时,其物质的量浓度由大到小的顺序是①>②>③ |
| B.物质的量浓度相同时,其pH由大到小的顺序是①>②>③ |
| C.中和等量的烧碱溶液,需等物质的量浓度的①②③三种酸溶液的体积比为2∶2∶1 |
| D.体积和物质的量浓度均相同的①②③三溶液 ,分别与同浓度的烧碱溶液恰好完全反应,所需烧碱溶液的体积比为2∶1∶2 |
试题篮
()