固体硝酸盐加热易分解且产物较复杂。某学习小组以Mg(NO3)2为研究对象,拟通过实验探究其热分解的产物,提出如下4种猜想,其中不成立的是
| A.Mg(NO3)2、NO2、O2 | B.MgO、NO2、O2 | C.Mg3N2、O2 | D.MgO、NO2、N2 |
根据硝酸和硫酸所具有的性质,选择适当的字母按要求填空。
| A.吸水性 | B.脱水性 | C.强氧化性 | D.强氧化性和酸性 |
(1)浓硫酸常用作干燥剂,说明浓硫酸具有 ;
(2)用玻璃棒蘸浓硫酸滴在纸上,发现变黑,说明浓硫酸具有 ;
(3)浓硫酸和浓硝酸都可以与铜反应,反应中浓硫酸和浓硝酸显示出 。
将NO2、NH3、O2混合气22.4L通过稀硫酸后,溶液质量增加了26.7g,气体体积缩小为4.48L。(气体体积均在标况下测定)剩余气体能使带火星的木条着火,则混合气体的平均相对分子质量为(4NO2+O2+2H2O=4HNO3)( )
| A.28.1 | B.30.2 | C.33.1 | D.34.0 |
在某稀溶液中含有0.1mol HNO3和x mol H2SO4,向其中加入9.6 g铜粉,充分反应后产生的气体在标准状况下的体积为2.24L,则x值至少为 ( )
| A.0.1 | B.0.12 | C.0.15 | D.0.2 |
同温同压下,在3支体积不同的试管中分别充满等体积混合的2种气体,它们是:①NO和NO2,②NO2和O2,③NH3和N2。现将3支试管均倒置于水槽中,充分反应后,试管中溶质的物质的量浓度分别为c1、c2、c3(假设溶质全在试管中),则下列关系正确的是
| A.c1>c2>c3 | B.c1>c3>c2 | C.c1=c3>c2 | D.c1=c2>c3 |
右图A→E是五种中学化学常见物质其中A、B、C、D常温下都是气体,B 为红棕色,A为气体单质。
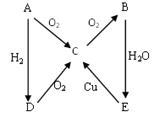
(1)写出化学式:B C
(2)实验室制备D实验中所用的干燥剂是: 。
(3)B与H2O反应,该反应的氧化剂和还原剂的物质的量之比为 。
(4)A与O2的反应方程式: ;D与O2的反应方程式:
;A与H2的反应方程式: 。
下列有关硝酸化学性质的叙述中,正确的是 ( )
| A.敞口放置的浓硝酸浓度变小是因为浓硝酸的吸水性 |
| B.硝酸可与Na2SO3反应制得SO2气体 |
| C.浓硝酸因分解放出的NO2又溶解于硝酸而呈黄色 |
| D.硝酸能与Fe2O3反应,表现氧化性 |
下列叙述错误的是( )
| A.检验NH时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体 |
| B.液氨汽化时要吸收大量的热,可用作制冷剂 |
| C.实验室用NH4Cl和Ca(OH)2制备NH3涉及氧化还原反应 |
| D.将分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
在浅绿色的Fe(NO3)2溶液中存在如下平衡:Fe2++2H2O Fe(OH)2+2H+,若向该溶液中滴 加足量的盐酸,则溶液的颜色( )
Fe(OH)2+2H+,若向该溶液中滴 加足量的盐酸,则溶液的颜色( )
| A.绿色更浅 | B.绿色更深 | C.变黄 | D.无变化 |
以下物质间的转化通过一步反应都能实现的是( )

| A.Si→SiO2→H2SiO3→Na2SiO3 | B.HCl→Cl2→HClO→NaClO |
| C.S→SO3→H2SO4→Al2(SO4)3 | D.NH3→NO2→HNO3→NaNO3 |
锌与很稀的硝酸反应生成Zn(NO3)2、NH4NO3和水。当生成1mol硝酸锌时,被还原的硝酸的物质的量为( )
| A.0.25mol | B.0.5mol | C.1mol | D.2mol |
下列反应中,硝酸既表现酸性,又表现氧化性的是( )
| A.Fe2O3跟稀硝酸反应 | B.Al(OH)3跟稀硝酸反应 |
| C.CuO跟稀硝酸反应 | D.Fe(OH)2跟稀硝酸反应 |
试题篮
()