N2O5是一种新型硝化剂,其性质和制备受到人们的关注。






(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 。
(2)一定温度下,在恒容密闭容器中N2 O5可发生下列反应: 2N2O5(g) 4NO2(g)+O2(g);ΔH>0
2N2O5(g) 4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将 。(填“增大”或“减小”、“不变”)
②下表为反应在T1温度下的部分实验数据:
| t/s |
0 |
500 |
1000 |
| c(N2O5)/mol·L-1 |
5.00 |
3.52 |
2.48 |
则500s内N2O5的分解速率为 。
③在T3温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2 T1。
 |
(3)如上图所示装置可用于制备N2O5,则N2O5在电解池的
区生成,其电极反应式为 .
某兴趣小组设计出右图所示装置来改进教材中"铜与硝酸反应"实验,以探究化学实验的绿色化。

(1)实验前,关闭活塞,试管
中加水至浸没长导管口,塞紧试管
和
的胶塞,加热
。其目的是。
(2)在中加适量
溶液,
中放一小块铜片,由分液漏斗
向
中加入2
浓硝酸。
中反应的化学方程式是。再由
向
中加2 mL蒸馏水,
中的实验现象是。
| 方案 |
反应物 |
| 甲 |
|
| 乙 |
|
| 丙 |
(3)右表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是。理由是。
(4)该小组还用上述装置进行实验证明氧化性。操作步骤为,实验现象为;但此实验的不足之处是。
已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐热分解的反应方程式如下(条件都是加热):
①2KNO3=2KNO2+O2↑
②2Cu(NO3)2=2CuO+4NO2↑+O2↑
③2AgNO3=2Ag+2NO2↑+O2↑
今有某固体可能由上述三种硝酸盐中的一种或几种组成。取适量该固体充分加热,得到一定量的气体,将这些气体通入水中,结果全部被吸收,没有剩余,回答:
(1)该固体是否可能只由一种盐组成?若可能,指出是哪种盐,若不可能,说明原因。___________________________________________________________________________________.
(2)若固体是混合物,指出它的可能组成(即物质的量之比),若没有这种组成,也请说明__________________________________________________________________________________。
在做氨的催化氧化实验时,铂丝不能接触氨水,原因是…( )
| A.铂丝的温度高,接触氨水会使氨气大量逸出 | B.红热铂丝会与氨水反应,使铂丝腐蚀 |
| C.防止铂丝温度降低而不能起催化作用 | D.防止爆炸 |
某化学课外小组所做实验的示意图如下图
 |
 图中“ ”表示气体流向,M是一种子纯净而干燥的气体,Y为另一种气体。当与M气体反应时y气体过量,E内有棕色气体产生。实验所用到的物质只能由下列物质中选取:Na2CO3、Na2O2 、NaCl、CaCl2、(NH4)2CO3碱石灰等固体及蒸镏水。据此实验,完成下列填空:
图中“ ”表示气体流向,M是一种子纯净而干燥的气体,Y为另一种气体。当与M气体反应时y气体过量,E内有棕色气体产生。实验所用到的物质只能由下列物质中选取:Na2CO3、Na2O2 、NaCl、CaCl2、(NH4)2CO3碱石灰等固体及蒸镏水。据此实验,完成下列填空:
(1)A中所用装置的主要仪器有
(2)B中所选的干燥剂是 ,作用是 。
(3)C中发生的主要反应的化学方程式是
(4)制取y气体的D装置所用的主要仪器是
制取y的化学方程式是 。
(5)当F中为紫色石蕊试液时,见到的现象是 主要
反应方程式
为 、 。
为测定固体磷铵化肥中铵态氮的质量分数,实验室用右图所示装置进行实验。实验时,在A中加入mg磷铵样品,关闭止水夹a,打开止水夹b,向A中加入足量的浓NaOH溶液,完全反应后C中浓硫酸增重ng。请回答下列问题:

(1)试说明检查该装置气密性的操作方法和实验现象: 。
(2)实验过程应该在何时鼓入空气?答: (填“实验开始前”、“反应过程中”或“完全反应后”)
(3)如某次测定的铵态氮的质量分数明显偏低,则可能的原因是 (填字母)。
A.磷铵样品与氢氧化钠未充分反应 B、A和B中残留了一定量的氨气
C.氢氧化钠溶液的浓度太大
(4)某厂利用生产磷铵排放的磷石膏废渣制硫酸联产水泥,硫酸返回用于生产磷铵。其生产流程图如下:


①操作b的名称是浓缩、冷却、 。
②如反应Ⅱ的产物是两种酸式盐,则物质B中溶质的化学式是 。
③若在实验室中对反应Ⅲ产生的气体用NaOH溶液吸收,可使用的装置是
(填字母)。
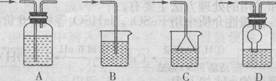
④该生产流程最大的优点是尽可能地实现原料的循环使用和副产物的综合利用,该生产流程体现的基本思想是 。
含氮废水进入水体后而对环境造成的污染越来越严重,对含氮废水进行有效的检测和合理的处理是人们研究和关心的重要问题。
⑴环境专家认为可以用金属铝将水体中的NO3-还原为N2,从而消除污染。其反应的离子方程式是:6NO3-+10Al+18H2O=3N2↑+10Al(OH)3+6OH—。又有人认为金属镁比铝能更快消除氮的污染,其反应原理和金属铝相同。
写出镁和含NO3-的废水反应的离子方程式
____________________ 。
⑵水中的NO2-是含氮有机物分解的产物,其浓度的大小是水源污染程度的标志之一。检测水中的NO2-可用目视比色法(比较溶液颜色深浅度以测定所含有色物质浓度的方法),检测步骤如下:
步骤一:配制标准溶液:称取0.69gNaNO2,溶于水后在容量瓶中稀释至1L得溶液A,移取5mL溶液A,稀释至1L,得溶液B。
步骤二:配制标准色阶:取6只规格为10mL的比色管(即质地、大小、厚薄相同且具有塞的平底试管),分别加入体积不等的溶液B,并稀释至10mL,再加入少许(约0.30g)氨基苯磺酸粉末,实验结果如下表所示。
| 色阶序号 |
1 |
2 |
3 |
4 |
5 |
6 |
| 加入溶液B的体积/mL |
0.0 |
2.0 |
4.0 |
6.0 |
8.0 |
10.0 |
| 反应后溶液颜色 |
由无色变为由浅到深的樱桃红色 |
步骤三:取10mL水样倒入比色管中,加少许氨基苯磺酸,显色后与标准色阶对比。
①利用步骤三在野外检测水样污染程度的优点
是 。
②步骤二中设计色阶序号1的作用
是 。
③如果水样显色后比6号还深,应采取的措施
是 。
⑶现有含NH3为3.4mg·L—1的废水150m3(密度为1g·cm-3),可采用如下方法进行处理:将甲醇加入含氨的废水中,在一种微生物作用下发生反应:
2O2 + NH3=== NO3- + H+ + H2O 6NO3-+ 6H+ + 5CH3OH→ 3N2↑ + 5CO2↑ + 13H2O
若用此方法处理,假设每步的转化率为100%,需要甲醇 g。
试题篮
()