右图是实验室制乙烯的发生装置和乙烯性质实验,根据图示回答下列问题:
 (图2)
(图2)
(1)图1中仪器①、②的名称分别为_______、________。
(2)写出②中发生反应的化学方程式: 。
(3)反应前在②中放入几块碎瓷片的目的是 。
(4)向溴的四氯化碳溶液中通入乙烯(如图2),溴的橙红色很快褪去,该反应属于________(填反应类型),反应的化学方程式为____________________________。
(5)请给下面的有机物命名 。
CH3CH2C(CH3)2C(CH2CH3)2CH3
已知用P2O5作催化剂,加热乙醇可制备乙烯,反应温度为80℃~210℃。某研究性小组设计了如下的装置制备并检验产生的乙烯气体(夹持和加热仪器略去)。
(1)仪器a的名称为 。
(2)用化学反应方程式表示上述制备乙烯的原理 。
(3)已知P2O5是一种酸性干燥剂,吸水放出大量热,在实验过程中P2O5与乙醇能发生作用,因反应用量的不同,会生成不同的磷酸酯,它们均为易溶于水的物质,沸点较低。写出乙醇和磷酸反应生成磷酸二乙酯的化学方程式(磷酸用结构式表示为 )
)
。
(4)该装置中还缺一种必备仪器,该仪器为 。某同学认为即使添加了该仪器上述装置验证产生了乙烯不够严密,仍须在酸性高锰酸钾溶液之前添加洗气装置,其理由为 。
实验室制乙烯,常常因为温度过高而使乙醇与浓硫酸反应生成少量的二氧化碳,有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。
(1)写出实验室制取乙烯的化学方程式________________________________
(2)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置中可盛放的试剂是:(将下列有关试剂的序号填入空格内)
Ⅰ: 、Ⅱ: 、Ⅲ: 、Ⅳ: 。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.溴水 |
(3)能说明二氧硫存在的现象是 。
(4)使用装置(Ⅱ)的目的是 。
(5)使用装置(Ⅲ)的目的是 。
(6)确证含乙烯的现象 。
(7)进行下列实验时,都要使用温度计,回答下列问题:
制取乙烯时,温度计水银球部位应放在 。
石油分馏时,温度计水银球部位应放在 。
某化学兴趣小组用图1所示装置进行探究实验。当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓硫酸与乙醇的混合液体变为棕黑色。
(1)该实验中生成乙烯的化学方程式为: ;
(2)一些同学认为:溴水褪色的现象不能证明反应中有乙烯生成和乙烯具有不饱和性,因为棕黑色物质与浓硫酸反应生成某气体,该气体使溴水褪色反应的化学方程式为: ;
另一些同学经过细致的观察后认为:试管中另一个现象可证明反应中有乙烯生成,且乙烯具有不饱和性。这个现象是 ;
(3)该小组改用图2装置实验,将烧瓶置于润滑油(沸点、燃点均高于300℃)中加热。此法加热的优点是① ;② ;
(1)下面是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,完成下列问题。 
①A中碎瓷片的作用是 。
②B中反应类型是 。C中实验现象是 。
③在D处点燃前必须进行的操作是 。
(2)制取氯乙烷(CH3CH2Cl)的最佳方法是(用化学方程式表示): 。
(3)来自石油的另一产品是苯,请写出由苯制硝基苯的化学方程式: 。
(4)该实验中D处乙烯燃烧的化学方程式: 。
30.将11.2L(标准状况)乙烯和乙烷的混合气体通入足量的溴的四氯化碳溶液中,充分反应后,溴的四氯化碳溶液的质量增加了8.4g,求原气体混合物中乙烯与乙烷的物质的量之比和质量比。
(A)乙烯是石化工业的重要原料,实验室是将 和浓硫酸(体积比为 )的混合液迅速加热到 的方法值得的,此反应中浓硫酸的作用是 和 ;乙烯在一定条件下发生加聚反应,其产物的名称是 ;乙烯还对水果具有 功能;乙烯能在空气中燃烧,由于乙烯的 ,所以火焰 并伴有 产生。
(B)实验室制取乙烯时常因温度过高生成少量的SO2,有人设计了下列实验以确定上述混合气体中含有乙烯和SO2。
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是:Ⅰ 、Ⅱ 、Ⅲ 、Ⅳ 。
(将下列有关试剂的序号填入空格内)
A.品红溶液 B.NaOH溶液 C.浓H2SO4 D.酸性高锰酸钾溶液
(2)能说明SO2气体存在的现象是
(3)使用装置Ⅱ的目的是
(4)使用装置Ⅲ的目的是
(5)证明含有乙烯的现象是
乙烯是一种重要的化工原料,我们已学过用两种方法制得乙烯:
A.在实验室里用乙醇与浓硫酸共热制乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题: ;
;
(1)I、II、III、IV装置可盛放的试剂是I ;II ;
III ;IV (将下列有关试剂的序号填入空格内)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是 。
(3)确定含有乙烯的现象是 。
(4)写出生成乙烯的反应方程式: 。
B.为检验利用溴乙烷发生消去反应后生成的气体中是否含乙烯的装置如图所示。回答:
(1)利用溴乙烷发生消去反应的化学方程式为: 。
(2)试管a的作用是 ;若省去试管a,试管b中试剂为 。
实验室制乙烯,常因温度过高生成少量SO2,有人设计了如下图所示实验,以验证上述混合气体中是否含有乙烯和SO2。
(1) 装置中X仪器的名称是: ; 碎瓷片的作用是: 。
(2) 写出生成乙烯的反应方程式: 。
(3)A、B、C、D装置中盛放的试剂是(从下列所给试剂中选出,填序号)
①品红溶液,②NaOH溶液,③ KMnO4酸性溶液。
A. B. C. D.
(4)能说明SO2气体存在的现象是 。
(5)确证含有乙烯的现象是 。
实验室制取乙烯并检验乙烯性质的装置如下图。请回答有关问题: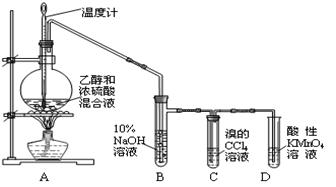
 (1)烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是 。
(1)烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是 。 (2)烧瓶中产生乙烯的反应方程式为 。
(2)烧瓶中产生乙烯的反应方程式为 。 (3)反应开始后,可观察到C和D中共同的现象是 ; C中的反应类型为 反应、D中的反应类型为 反应。
(3)反应开始后,可观察到C和D中共同的现象是 ; C中的反应类型为 反应、D中的反应类型为 反应。 (4)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是
(4)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是  ;10%的NaOH溶液起的作用是 。
;10%的NaOH溶液起的作用是 。
(10分,每空1分)实验室制乙烯的反应原理为CH3CH2OH  CH2===CH2↑+H2O,制取时常因温度过高而发生副反应,使部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑。
CH2===CH2↑+H2O,制取时常因温度过高而发生副反应,使部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑。



(1)请用图中编号为①、②、③、④的装置设计一个实验,以验证上述反应混合气体中含有CO2、SO2和水蒸气。用装置的编号表示装置的连接顺序(按产物气流从左到右):
→ → → 。
(2)实验时装置①中A瓶的现象是 ,原因是 。
B瓶中的现象是 ,B瓶溶液的作用是 。
若C瓶中品红溶液不褪色,说明 。
(3)装置③中加的固体药品是 ,以验证混合气体中有 。装置②中盛的溶液是 ,以验证混合气体中的 。
实验室制取乙烯的装置如下图所示,请回答:
(1)实验室制取乙烯所用的乙醇为无水乙醇,但工业酒精中乙醇的含量为95%,将工业酒精转化为无
水乙醇的方法是 。
(2)反应中浓硫酸起 和 的作用。加热前应该在烧瓶内放入少量碎瓷片,它的作用是 。温度计的作用是 。
(3)该实验可能产生的主要的有机副产物是 。
(4)反应的化学方程式是: 反应类型是 。
实验室制取乙烯的装置如下图所示,请根据图示回答下列问题:
(1)实验室制乙烯的化学方程式为____________________________________
在这个反应中,浓硫酸的作用是___ _和_____ 。
(2)某化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:
①I、II、Ⅲ、IV装置可盛放的试剂是I II Ⅲ IV____ (填试剂的序号)。
| A.品红溶液 | B.NaOH溶液 |
| C.浓硫酸 | D.酸性KMnO4溶液 |
②能说明SO2气体存在的现象是_____________________________________________。
③确定含有乙烯的现象是____________________________________________________ 。
(1)在实验室里制取乙烯常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计如下图所示实验以确认上述混和气体中有C2H4和SO2。 (乙烯的制取装置略)
①Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛入的试剂是Ⅰ__________、 Ⅱ__________、Ⅲ__________、Ⅳ__________。(将下列有关试剂的序号填入空格内)
A.品红溶液 B.NaOH溶液 C.浓H2SO4 D.KMnO4酸性溶液
② 乙醇制取乙烯的反应装置此处略去,写出该反应的化学方程式:
③ 能说明SO2气体存在的现象是_____________________________________________。
④ 使用装置Ⅲ的目的是_____________________________________________________。
⑤ 确定含有乙烯的现象是___________________________________________________。
(2)1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下是无色液体,密度2.18g/cm3,沸点131.4℃,熔点9.79℃,不溶于水、易溶于醇、醚、丙酮等有机溶剂。在实验中可以用乙烯来制备1,2-二溴乙烷。 请填写下列空白:
①写出用乙烯制备1,2-二溴乙烷的化学方程式: 。
②要检验某溴乙烷中的溴元素,正确的实验方法是
A.加入氯水振荡,观察水层是否有棕红色出现
B.滴入AgNO3溶液,再加入稀HNO3,观察有无浅黄色沉淀生成
C.加入NaOH溶液共热,冷却后加入AgNO3溶液,观察有无浅黄色沉淀生成
D.加入NaOH溶液共热,然后加入稀HNO3使溶液呈酸性,再滴入AgNO3溶液,观察有无浅黄色沉淀生成
(1)下面是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,完成下列问题。
①A中碎瓷片的作用是 。
②B中反应类型是 。C中实验现象是 。(2)制取氯乙烷(CH3CH2Cl)的最佳方法是(用化学方程式表示): ;(3)用空气吹溴水到SO2溶液中的化学方程式: ;(4)把干海带放在 (仪器的名称)中灼烧。灼烧后的海带溶于水中,过滤后的滤液中酸化后加过氧化氢的离子方程式
(5)在试管A中加入3 mL 乙醇,然后边振荡试管边慢慢加入2 mL 浓硫酸和2 mL 乙酸,按下图所示连接好装置制取乙酸乙酯。
①试管B中盛放饱和Na2CO3溶液的作用是:中和乙酸、溶解乙醇和 。
②实验完成后,若要分离B中的液体混合物,需要用到的玻璃仪器主要是 。
试题篮
()