下列叙述正确的是( )
| A.非金属元素之间构成的化合物都不是离子化合物 |
| B.阴、阳离子通过静电引力所形成的化学键叫离子键 |
| C.离子化合物中一定没有共价键 |
| D.含有阳离子的化合物一定含有阴离子 |
下列说法中,不正确的是 ( )
| A.非极性键也可能存在于离子化合物中 |
| B.非金属原子及其阴离子的核外电子层数等于该元素所在的周期数 |
| C.共价化合物在液态时不能导电 |
| D.双原子分子中的共价键,一定是非极性键 |
下列晶体或分子中,含有化学键类型有差异的一组是 ( )
| A.H2O、CO2 | B.MgF2、H2O2 |
| C.NaOH、Ba(OH)2 | D.NaCl、KCl |
根据要求回答下列问题。
(1)分子球棍模型可以帮助人们认识有机物的结构。
下列是某有机物的分子比例模型,其中不同颜色的球代表不同的原子,球之间的“棍”
表示单键、双键或三键。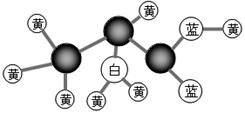
该有机物分子中可能存在的两种官能团的名称分别为 ▲ 、 ▲ ;
这类有机物在化学性质上表现的特点是 ▲ 。
(2)有机物的特征性质常可用以有机物之间的鉴别。
①欲区分葡萄糖和淀粉,可选用 ▲ (填字母)。
A.碘水 B.银氨溶液 C.盐酸 D.NaOH溶液
②欲区分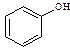 和
和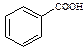 ,可选用 ▲ (填字母)。
,可选用 ▲ (填字母)。
A.AgNO3溶液 B.NaOH溶液 C.FeCl3溶液 D.Na2CO3溶液
(3)同分异构现象是有机物种类繁多的原因之一。
分子式为C7H6O2的有机物有多种同分异构体,其中含有苯环和1个侧链的同分异构体的结构简式是 ▲ 、 ▲ ……。
(4)高分子化合物在生产、生活中有着广泛的应用。
PES(聚丁二酸乙二醇酯)是一种生物可降解的聚酯,它在塑料薄膜,食品包装等方面有着广泛的应用。其结构简式如下:
合成PES的有机化学反应类型是 ▲ 反应。形成该聚合物的两种单体的结构简式分别是 ▲ 和 ▲ 。
下列各组物质中,全部以共价键结合的是 ( )
| A.H2S、NH3、CO2 | B.MgBr2、CaO、HCl |
| C.Na2S、MgO、HF | D.CO2、H2O、Na2O2 |
现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E是同族元素,且D最外层电子数是次外层电子数的3倍。A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态。请回答下列问题(填空时用化学符号作答):
(1)BC-的电子式为 ;元素F在周期表中的位置为 。
(2)最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4分子。C4分子结构如右图所示。根据以上信息和数据,下列说法正确的是 。
A.C4属于一种新型的化合物 B.C4与C2互为同素异形体
C.C4稳定性比P4(白磷)差 D.C4与C2互为同位素
(3)A与C两种元素可形成多种化合物分子,其中CA3分子的分子的空间构型为
,键角 ;C2A4分子的结构式为 。
(4)为了除去化合物A2ED4稀溶液中混有的A2ED3,常采用A2D2为氧化剂,发生反应的离子方程式为 。
(5)E与F形成的化合物E2F2在橡胶工业上有重要用途,遇水易水解,其空间结构与A2D2极为相似。对此以下说法正确的是
A.E2F2的结构式为:F-E—E-F B.E2F2在一定条件下,有氧化性或还原性
C.E2F2中的两各E原子的化合价分别为0价和+2价
D.E2F2与H2O反应的化学方程式可能为:2E2F2+2H2O=EO2↑+ 3E↓+4HF
(6)B与D可形成两种常见化合物,其中一种化合物BD2是 分子(填“极性”或“非极性”)。在1000 mL 0.1 mol/L的 Ca(OH)2物质的水溶液中逐渐通入BD2并充分搅拌,溶液中析出沉淀的质量发生变化,在右图中画出沉淀质量随通入BD2的物质的量的变化曲线。
 |
X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,X、W在周期表中的相对位置如下表;X元素最低负化合价的绝对值与其原子最外层电子数相等;Z是地壳中含量最多的金属元素。
(1)元素Q在周期表中位于第_____族,Z的离子结构示意图为_____。
(2)Z、W、Q的原子半径由大到小的顺序为 。(用元素符号表示其原子)。
(3)X和氢组成的化合物分子中有6个原子,其结构简式为______,写出该物质与水加成的化学方程式 。
(4)Y的最简单气态氢化物甲的水溶液显碱性
①用电离方程式表示氢化物甲的水溶液中的显碱性的原因 ,
②在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为____ __。该反应的氧化剂是 当有1mol甲参加反应时,电子转移 mol。
③Y的最简单气态氢化物甲和Q的氢化物乙反应生成正盐的电子式 ,
该化合物中所含化学键类型是 ,该化合物属于 晶体。
氢气、纳米技术制成的金属燃料、非金属固体燃料已应用到社会生活和高科技领域。
⑴已知短周期金属元素A和B,其单质单位质量的燃烧热大,可用作燃料。其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) |
I1 |
I2 |
I3 |
I4 |
| A |
899.5 |
1757.1 |
14848.7 |
21006.6 |
| B |
738 |
1451 |
7733 |
10540 |
①根据上述数据分析, B在周期表中位于 区,其最高价应为 ;
②若某同学将B原子的基态外围电子排布式写成了ns1np1,违反了 原理;
③B元素的第一电离能大于Al,原因是 ;
⑵氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。
①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由 。
②C60分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子相对稳定结构,则C60分子中σ键与π键的数目之比为 。
下列说法正确的是
| A.含有阴离子的晶体中必含有阳离子 |
| B.由极性键构成的AB2型分子必是极性分子 |
| C.非金属元素组成的化合物中只含有共价键 |
| D.离子晶体中必含有离子健,分子晶体中必含有共价键 |
试题篮
()