下列关于碰撞的说法正确的是( )
| A.活化分子之间的碰撞一定能引发化学反应,即活化分子之间的碰撞为有效碰撞 |
| B.发生有效碰撞的分子必为活化分子 |
| C.反应物分子之间的碰撞一定会引发化学键的断裂 |
| D.反应物分子之间只要有合适的取向的碰撞必为有效碰撞 |
下列各组物质中化学键类型与晶体类型均相同的是( )
| A.HCl NaCl | B.SiO2 CO2 |
| C.Na2CO3 KClO3 | D.H2O2 Na2O2 |
下列有关物质结构的叙述正确的是 ( )
| A.只含有共价键的物质不一定是共价化合物 |
| B.由电子定向移动而导电的物质是金属晶体 |
C.有键能很 大的共价键存在的物质熔沸点一定很高 大的共价键存在的物质熔沸点一定很高 |
| D.在离子化合物中不可能存在非极性共价键 |
下列说法正确的是
①离子化合物一定含离子键,也可能含极性键或非极性键
②共价化合物一定含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的化合物一定是离子化合物
| A.①③⑤ | B.②④⑥ | C.②③④ | D.①③⑥ |
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:
| 元素 |
Al |
B |
Be |
C |
Cl |
F |
Li |
| X数值 |
1.5 |
2.0 |
1.5 |
2.5 |
2.8 |
4.0 |
1.0 |
| 元素 |
Mg |
Na |
O |
P |
S |
Si |
|
| X数值 |
1.2 |
0.9 |
3.5 |
2.1 |
2.5 |
1.7 |
|
试结合元素周期律知识完成下列问题:
(1)经验规律:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AIBr3中的化学键类型是 。
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系 。
简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系
。
(3)某化合物分子中含有S-N键,该共用电子对偏向于 原子(填元素符号)。
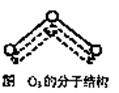
1994年度诺贝尔化学奖授予为研究臭氧作出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。臭氧分子的结构如图,呈V型,两个O-O键的夹角为116.5º,三个原子以一个O原子为中心,与另外两个氧原子分别构成共价键;中间O原子提供2个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学健―三个O原子均等地享有这4个电子。(如右图所示)。请回答:
(1)臭氧与氧气的关系是______________。
(2)选出下列分子与O3分子的结构最相似的是( )
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
(3)分子中某原子没有跟其他原子共用的价电子对叫孤对电子,那么O3分子有 对孤对电子。
(4)O3具有强氧化性,它能氧化PbS为PbSO4,而O2不能,试配平:
_____PbS + _____O3 ——_____PbSO4 + _____O2;
向盛有硫酸铜水溶液的试管里加入氨水,先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是 ( )
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变。 |
| B.沉淀溶解后,将生成深蓝色的配合离子[Cu (NH3)4]2+ |
C.硫酸铜水溶液 里加入氨水生成的沉淀是氢氧化铜,继续加氨水沉淀又溶解,说明氢氧化铜是两性氢氧化物 里加入氨水生成的沉淀是氢氧化铜,继续加氨水沉淀又溶解,说明氢氧化铜是两性氢氧化物 |
| D.在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
下列说法中,正确的一组是( )
①两种元素构成的共价化合物分子中的化学键都是极性键
②两种非金属元素原子间形成的化学键都是极性键
③含有极性键的化合物 分子一定不含非极性键
分子一定不含非极性键
④只要是离子化合物,其熔点就比共价化合物的熔点高
⑤离子化合物中含有离子键
⑥分子晶体中的分子不含有离子键
⑦分子晶体中的分子内一定有共价键
⑧原子晶体中一定有非极性共价键
| A.②⑤⑥⑦ | B.①②③⑤⑥ | C.②⑤⑥ | D.②③⑤⑥⑦ |
CO2、CH4、BF3都是非极性分子,HF、H2O、NH3都是极性分子,由此推测ABn型分子是非极性分子的经验规律正确的是( )
| A.所有原子在同一平面 | B.分子中不含有氢原子 |
| C.在ABn中A原子没有孤对电子 | D.A的相对原子质量小于B |
试题篮
()