根据碳原子的成键特点,甲烷分子中形成共价键的数目为( )
| A.4 | B.5 | C.6 | D.7 |
我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:
HCHO+O2 CO2+H2O。下列有关说法正确的是
CO2+H2O。下列有关说法正确的是
| A.该反应为吸热反应 | B.CO2分子由极性键形成的极性分子 |
| C.HCHO分子中有3个σ键,1个π键 | D.每生成1.8gH2O消耗2.24L O2 |
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解,得到深蓝色的透明溶液。下列对此现象说法正确的是
| A.反应后溶液中不存在任何沉淀,所以反应前后[Cu(H2O)4]2+的数目不变 |
| B.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ |
| C.向反应后的深蓝色溶液中加入乙醇,不会产生任何现象 |
| D.在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
下列说法错误的是( )
A.新榨油脂不及时干燥脱水易变质
B.聚氯乙烯可制作食品内包装材料
C.维生素C可作预包装食品抗氧剂
D.卤水点豆腐本质属于蛋白质聚沉
下列关于丙烯(CH3CH=CH2)的说法正确的是
| A.丙烯分子有7个σ键和1个π键 |
| B.丙烯分子存在非极性键 |
| C.丙烯分子中3个碳原子都是sp3杂化面上 |
| D.丙烯分子中有3个碳原子在同一直线上 |
下列性质与氢键无关的是
| A.NH3的熔、沸点比第ⅤA族其他元素氢化物的熔、沸点高 |
| B.乙酸可以和水以任意比互溶 |
| C.常温下H2O为液态,而H2S为气态 |
| D.水分子高温下也很稳定 |
氮化钠和氢化钙都是离子化合物,与水反应的化学方程式(末配平)如下:Na3N+H2O→NaOH+NH3,CaH2+H2O→Ca(OH) 2+H2。有关它们的叙述正确的是
| A.离子半径的大小:Na+>N3->H- |
| B.它们与水发生的反应均属于氧化还原反应 |
| C.两种化合物均只含离子键,不含共价键 |
| D.两固体混合物溶于足量盐酸中可得到三种盐 |
下列说法中正确的是
| A.中子数为18的氯原子可表示为18Cl |
B.某金属阳离子的结构示意图为 ,其与Cl-形成的化合物都是离子化合物 ,其与Cl-形成的化合物都是离子化合物 |
C.二硫化碳的电子式为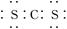 |
| D.17.4g熔融K2SO4与7.8 g熔融Na2O2中阴离子数目相同 |
下列事实与氢键有关的是:
| A.水加热到很高的温度都难以分解 |
| B.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 |
| C.水结成冰体积膨胀,密度变小 |
| D.HF、HCl、HBr、HI的热稳定性依次减弱 |
有关乙烯和苯分子中的化学键描述正确的是( )
| A.苯分子中每个碳原子的sp2杂化轨道中的其中一个形成大π键 |
| B.乙烯分子C-H之间是sp2形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键 |
| C.苯分子C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形成的π键 |
| D.乙烯和苯分子每个碳原子都以sp2杂化轨道形成σ键,未杂化的2p轨道形成π键 |
下列说法错误的是( )
| A. |
糖类化合物也可称为碳水化合物 |
| B. |
维生素D可促进人体对钙的吸收 |
| C. |
蛋白质是仅由碳、氢、氧元素组成的物质 |
| D. |
硒是人体必需的微量元素,但不宜摄入过多 |
膦(PH3)又称为磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,它的分子是三角锥形。以下关于PH3的叙述中,正确的是
| A.PH3是非极性分子 |
| B.PH3分子中有未成键的电子对 |
| C.PH3是强氧化剂 |
| D.PH3分子中的P—H键是非极性键 |
下列物质中含有共价键的离子化合物是
| A.HCl | B.NaOH | C.CaCl2 | D.N2 |
下列分子中所有原子都满足最外层8电子结构的是( )
①CO2 ②XeF6 ③PCl3 ④SO2 ⑤BF3 ⑥N2 ⑦P4 ⑧PCl5
| A.①③⑥⑦ | B.①④⑤ | C.①④⑥ | D.②③④⑤ |
试题篮
()