下列反应的离子方程式正确的是
| A.物质的量浓度相等的碳酸氢钡溶液和氢氧化钠溶液等体积混合 Ba2+ + 2HCO3- + 2OH- = BaCO3↓+CO32- + 2H2O |
|
| B.NaHSO4溶液中滴加入Ba(OH)2溶液至中性 电解 |
C.以石墨作电极电解氯化镁溶液:2Cl-+2H2O ="==" 2OH-+H2↑+Cl2↑ |
D.碳酸氢钠溶液加入氯化铝溶液 3HCO3-+Al3+ 3CO2+Al(OH)3 3CO2+Al(OH)3 |
下列说法正确的是
| A.KClO3和SO3溶于水后均能导电,故KClO3和SO3都是电解质 |
| B.常温下将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.常温下,等浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
| D.25℃时,用pH=3的盐酸滴定等浓度的氨水至溶液的pH=7,V(氨水)<V(盐酸) |
有体积相同、pH相等的烧碱溶液和氨水,下列叙述中正确的是
| A.两溶液溶质物质的量浓度相同 |
| B.用同浓度的盐酸中和时,消耗盐酸的体积相同 |
| C.两溶液中OH-离子浓度相同 |
| D.加入等体积的水稀释后,它们的pH仍相等 |
关于浓度均为0.1mol·L-1的三种溶液:①醋酸溶液 ②NaOH溶液 ③醋酸钠溶液,下列说法不正确的是( )
| A.C(CH3COO-):③>① |
| B.水电离出的C(OH-):②>① |
| C.①和②等体积混合后的溶液:C(OH-)=C(H+)+C(CH3COOH) |
| D.①和③等体积混合后的溶液显酸性:C(CH3COO-)>C(Na+)>C(H+)>C(OH-) |
常温常压下,将amolCO2气体通入1L1mol/L的NaOH溶液中,下列对所得溶液的描述不正确的是
| A.当1/2<a<1时,所得溶液中一定存在: c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| B.当a=1时,所得溶液中存在: c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| C.当a=1/2时,所得溶液中存在: c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
| D.当a=2时,随着CO2气体的通入,溶液中水电离出c(H+)有如上图变化关系 |
按要求填空:
(1)写出制取氢氧化铁胶体的水解方程式:
(2)有4中混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①CH3COONa与HCl②CH3COONa与NaOH③CH3COONa与NaCl④CH3COONa与NaHCO3,则c(CH3COO-)从大到小的关系为 。(填序号)。
(3)25℃时,已知0.1mol·L-1 CH3COONa溶液的PH=8,精确表达下列算式的数学结果:
①c(Na+)-c(CH3COO-)= ;②c(OH-)-c(CH3COOH)=
(4)若往Mg(OH)2的悬浊液中逐滴滴入NH4Cl溶液至澄清,该过程中沉淀溶解的离子反应是 。
120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是
| A.2.0mol/L | B.1.5 mol/L | C.0.18 mol/L | D.0.24mol/L |
常温下,某溶液中由水电离出的c(H+)与c(OH-)的乘积为10-10,该溶液可能是( )
| A.pH等于5的醋酸溶液 | B.一定浓度的NaOH溶液 |
| C.一定浓度的NaHSO4溶液 | D.一定浓度的NH4Cl溶液 |
水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度。将水样与 碱性悬浊液(含有 )混合,反应生成 ,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化, 被 还原为 ,在暗处静置 ,然后用标准 溶液滴定生成的 ( )。
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是_____________。
(2)"氧的固定"中发生反应的化学方程式为_______________。
(3) 溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶和____________;蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除____及二氧化碳。
(4)取 水样经固氧、酸化后,用 溶液滴定,以淀粉溶液作指示剂,终点现象为________________;若消耗 溶液的体积为 ,则水样中溶解氧的含量为_________mg·L − 1。
(5)上述滴定完成时,若滴定管尖嘴处留有气泡会导致测量结果偏___________。(填"高"或"低")
下列实验操作能达到实验目的的是( )
| A. |
用长颈漏斗分离出乙酸与乙醇反应的产物 |
| B. |
用向上排空气法收集铜粉与稀硝酸反应产生的 NO |
| C. |
配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释 |
| D. |
将 与 混合气体通过饱和食盐水可得到纯净的 |
下列有关说法正确的是
A.一定条件下反应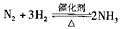 ,达到平衡时, ,达到平衡时,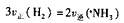 |
| B.10mL浓度为1mol/L的盐酸与过量的Zn粉反应,若加入适量的CH3COONa溶液,既能减慢反应这率,又不影响H2的生成 |
C.将PH=a十l的氨水稀释为pH=a的过程中,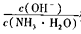 变小 变小 |
| D.常温下,向浓度为0.1 mol/L的CH3COONa溶液中加入等体积等浓度的CH3COOH,混合溶液的pH=7 |
下列叙述正确的是
| A. | 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 |
| B. |
25℃时,等体积等浓度的硝酸与氨水混合后,溶液
|
| C. |
25℃时,0.1
|
| D. |
0.1
|
下列说法正确的是( )
| A.pH=4的溶液中水电离出的H+一定是1×10-4mol/L |
| B.25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<VNaOH |
| C.向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| D.AgCl沉淀易转化为AgI沉淀且K(AgX)=c(Ag+)·c(X-),故K(AgI)<K(AgCl) |
下列说法中,正确的是
| A.25℃时,1L pH=3的盐酸和醋酸能消耗等质量的镁粉 |
| B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)将增大 |
| C.V1L pH=12的NaOH溶液与V2L pH=2的HA溶液混合,若混合液显中性,则V1≤V2 |
| D.在0.1mol·L-1 NaHCO3溶液中,加入少量NaOH固体,Na+和CO32―离子浓度均增大 |
试题篮
()