醋酸溶液中存在电离平衡:CH3COOH(aq) H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
| A.CH3COOH溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) |
| B.0.1 mol/L的CH3COOH溶液加水稀释,溶液中c(OH-)减小 |
| C.CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动 |
| D.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
1.8×l0-5 |
4.9×l0-10 |
K1=4.3×l0-7 K2=5.6×l0-11 |
根据上述电离常数分析,下列表述不正确的是( )
A.25℃时,等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(NaHCO3)>pH(CH3COONa)
B.a mol/L HCN溶液与b mol/L NaOH溶液等体积混合后,所得溶液中c(Na+)=c(CN-),则a一定大于b
C.2 NaCN + H2O + CO2 =2 HCN + Na2CO 3
D.2CH3COOH + Na2CO3 → 2 CH3COONa + H2O + CO2 ↑
已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
1.8×l0–5 |
4.9×l0–10 |
K1=4.3×l0–7 K2=5.6×l0–11 |
则下列有关说法正确的是( )
A、等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B、将a mol·L—1 HCN溶液与a mol·L—1 NaOH溶液等体积混合,混合液中:c(OH–)>c(H+),c(Na+)>c(CN–)
C、冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
D、NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +c(CO32–)
常温下下列关系的表述中,正确的是( )
| A.中和pH和体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比为1∶1 |
| B.pH=3的盐酸和pH=3的FeCl3溶液中,水电离的c(H+)相等 |
| C.0.1 mol·L-1 NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| D.浓度均为0.1 mol/L的三种溶液:①CH3COOH溶液;②NaOH溶液;③CH3COONa溶液,溶液的pH:②>③>① |
25°C时,几种弱酸溶液的PH如下表所示:
| 弱酸 |
CH3COOH |
H2SO3 |
HCN |
| 物质的量浓度mol/L |
0.01 |
0.01 |
0.01 |
| PH |
3.4 |
2.3 |
5.6 |
下列有关说法正确的是
A.相同PH的CH3COOH与HCN溶液中水电离的氢离子浓度CH3COOH溶液中的大
B.物质的量浓度相同的CH3COONa与NaCN溶液中,各离子浓度之和两者相等。
C.25°C时,HCN溶液的电离平衡常数(Ka)与NaCN溶液的水解平衡常数(K)存在
如下关系:Ka ·K = Kw
D.0.01mol/L的Na2SO3溶液与0.01mol/L的CH3COONa溶液相比,一定是后者的碱性强
下列说法正确的是
| A.在由水电离产生的氢离子浓度为10-13 mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3-四种离子能大量共存 |
| B.已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-) ,且c(Mg2+)∙c(CO32-)=6.82×10-6 |
| C.对于反应2N2H4(l)=N2(g)+2H2(g),△H=-50.6 kJ∙mol-1,它只在高温下自发进行 |
| D.常温下,将0.2 mol∙L-1某一元碱(ROH)溶液和0.1 mol∙L-1HCl溶液等体积混合,混合后溶液pH<7,则c(ROH)>c(R+) |
已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数(25℃) |
1.8×l0–5 |
4.9×l0–10 |
K1=4.3×l0–7 K2=5.6×l0–11 |
则下列有关说法正确的是( )
A、等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B、将a mol·L—1 HCN溶液与a mol·L—1 NaOH溶液等体积混合,混合液中:c(OH–)>c(H+),c(Na+)>c(CN–)
C、冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
D、NaHCO3和Na2CO3混合液中,一定有c(Na+)+ c(H+)=c(OH–)+ c(HCO3–) +c(CO32–)
下列各选项中所述的两个量,前者一定大于后者的是()
| A.pH=10的NaOH和Na2CO3溶液中,水的电离程度 |
| B.物质的量浓度相等的NH4NO3溶液和氨水中NH4+的物质的量浓度 |
| C.将pH=3的盐酸和醋酸分别加水稀释成pH=5的溶液,所加水的量 |
| D.相同温度下,10mL 0.1mol·L-1的醋酸和100mL 0.01mol·L-1的醋酸中H+物质的量 |
下列溶液均为0.100mol/L,下列关系正确的是
① NH4Cl ② NH4HSO4 ③ NH4Fe(SO4)2 ④ NH3·H2O
| A.①②显酸性,③④显碱性 | B.c(NH4+):④<③<② |
| C.溶液的pH:①<②<④ | D.②溶液中:c(NH4+)+c(H+)=c(SO42-)+c(OH-) |
下列说法正确的是
A.用坩埚灼烧MgCl2·6H2O的反应式 MgCl2·6H2O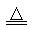 MgCl2+6H2O MgCl2+6H2O |
| B.根据下表提供的数据,等物质的量浓度的NaClO、NaHCO3混合溶液中,有c(HCO3-)>c(ClO-)>c(OH-) |
| C.常温下将pH=2的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一 |
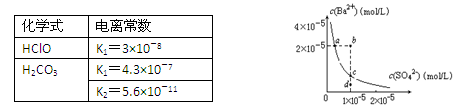
| D.某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,溶度积CKsp=c(Ba2+)·c(SO42-)。则加入Na2SO4可使溶液由a点变到b点;通过蒸发可以使溶液由d 点变到c 点 |
下列图像能正确反映所对应实验的是 
| A.①为向pH=13的NaOH溶液中不断加水 |
B. ②为向MnO2中加入一定量的H2O2溶液 ②为向MnO2中加入一定量的H2O2溶液 |
| C.③为向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 |
| D.④为将氨气通入醋酸溶液中 |
某学习小组根据化学知识和下表的数据,设计了表中的实验,以验证酸性:盐酸>碳酸>苯酚>碳酸氢根离子,其中不合理的是 ( )
| 物质 |
电离常数 |
和溶解度(25℃) |
| C6H5OH |
K=1.28×10-10 |
S = 9.3g/100g水 |
| H2CO3 |
K1 =4.3×10-7 |
|
| K2 =5.6×10-11 |
|
| |
组别 |
操作 |
判断依据 |
| A |
盐酸和碳酸 |
往碳酸钙固体中滴加盐酸 |
观察有无气体产生 |
| B |
碳酸与苯酚 |
往苯酚钠饱和溶液中,通入足量CO2 |
观察溶液是否变浑浊 |
| C |
碳酸与苯酚 |
配制同物质的量浓度的碳酸钠溶液和苯酚钠溶液 |
比较溶液的pH |
| D |
HCO3-与苯酚 |
在苯酚悬浊液中,加入过量的 Na2CO3溶液 |
观察悬浊液是否变澄清 |
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
(1)合成氨反应N2(g)+3H2(g) 2NH3(g),在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“向右”或“不”);使用催化剂使反应的△H (填“增大”、“减小”或“不改变”)。
2NH3(g),在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“向右”或“不”);使用催化剂使反应的△H (填“增大”、“减小”或“不改变”)。
(2)在25℃下,向浓度均 为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,沉淀会分步析出。
为0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,沉淀会分步析出。
首先生成沉淀的离子方程式为 __________________
氨水过量后,生成的沉淀会部分溶解,写出溶解沉淀的离子方程式__________________________.
( 已知25℃时Ksp[Mg(OH)2]=1.8×10-11, KsP[Cu(OH)2]=2.2×10- 20 )
20 )
(3)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后溶液中
c(NH4+) = c(Cl-)。则溶液显 _____ 性(填“酸”、“碱”或“中”),请用含a的代数式表示NH3·H2O的电离常数Kb= 。
(4) 在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO3 0.18mol,则v(o2)= mol.L-1.min-1:若继续通入0.20mol SO2和0.10mol O2,再次达到平衡后, n(SO3)的取值范围为________________。
下列说法正确的是
A.常温下,反应4Fe(OH)2(s)+2H2O(1)+O2(g)=4Fe(OH)3(s)能自发进行,则该反应的
B.浑浊的苯酚试液中加入饱和Na2CO3溶液变澄清,则酸性:苯酚>碳酸
C.在等浓度NaCl和NaCrO4稀溶液中滴加AgNO3溶液,分析出AgCl,则KSP(AgCl)<KSP(Ag2CrO4)
D.等体积、物质的量浓度的HA与NaA(HA为弱酸)混合溶液,其酸碱性取决于Ka(HA)的大小
试题篮
()