0.02mol·L-1的HCN溶液与0.02mol·L-1NaCN溶液等体积混合,已知混合溶液中
c(CN-)﹤c(Na+),则下列关系中,正确的是
| A.c(Na+)﹥c(CN-)﹥H+ ()﹥c(OH-) | B.c(HCN)+c(CN-)=0.04mol·L-1 |
| C.c(Na+)+c(H+)=c(CN-)+c(OH-) | D.c(CN-)﹥c(HCN) |
下列说法中正确的是( )
| A.二氧化硫溶于水能导电,故二氧化硫属于电解质 |
| B.硫酸钡难溶于水,故硫酸钡属于弱电解质 |
| C.硫酸是强电解质,故纯硫酸能导电 |
| D.相同条件下,氢离子浓度相同的盐酸和醋酸导电能力相同 |
下列物质中属于强电解质且能导电的是
①氢氧化钠溶液 ②硫酸钙固体 ③铜 ④蔗糖 ⑤三氧化硫 ⑥熔融氯化钠
| A.①②⑤ B.①②⑥ C.③⑥ D.⑥ |
、根据电离平衡移动原理完成下列表格
(1)已知:CH3COOH为弱电解质,在醋酸溶液中,当改变条件后,完成表格中的变化情况
| 外加条件 |
平衡移动方向 |
C(OH -) |
C(CH3COO -) |
| 升温 |
|
不填 |
不填 |
| 加水 |
|
|
不填 |
| 加盐酸 |
不填 |
|
|
| 加少量氢氧化钠固体 |
不填 |
不填 |
|
(2)在一定温度下,冰醋酸加水稀释过中溶液的导电能力如下图所示,请回答: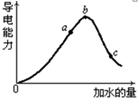
①写出醋酸的电离方程式________________。
②a、b、c三点溶液中氢离子浓度由小到大的顺序为__________________ 。
③a、b、c三点中醋酸的电离程度最大的是 。
④取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:C(H+)甲_____ 10C(H+)乙(填“大于”、“小于”或 “等于”),
下列溶液中c(Cl-)与50 mL 1mol/L 的AlCl3溶液中氯离子浓度相等的是
A.150 mL 1mol/L NaCl溶液 |
B.75 mL 2mol/L NH4Cl溶液 |
| C.75 mL 1mol/L FeCl3溶液 | D.150 mL 2mol/L MgCl2溶液 |
25℃时,浓度均为0.1 moI.L-l的HA溶液和BOH溶液,pH分别是l和11。下列说法正确的是
| A.BOH溶于水,其电离方程式是BOH=B++OH- |
| B.若一定量的上述两溶液混合后pH=7,则c(A—)=c(B+) |
| C.在0.1 mol·L-lBA溶液中,c(B+)>c(A一)> c(OH-)>c(H+) |
| D.若将0.1mol·L-lBOH溶液稀释至0.001mol·L-1,则溶液的pH=9 |
常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的 pH如下表:
下列判断正确的是 ( )
| A.a>9 |
| B.在乙组混合液中由水电离出的c(OH-)=10-5mol·L-1 |
| C.c1=0.2 |
| D.丁组混合液:c(Na+)>c(A-)>c(H+)>c(OH-) |
下列物质属于电解质的是()
①氯化钠溶液 ②氯化铵固体 ③铜 ④石墨 ⑤熔融NaOH ⑥盐酸 ⑦乙酸
⑧NH3·H2O ⑨三氧化硫
| A.①②⑥⑧ | B.②⑤⑦⑧ | C.②⑤⑥⑦ | D.②④⑤⑨ |
下列关于氯水的叙述正确的是( )
| A.氯水中只存在一种电离平衡 |
| B.向氯水中通入SO2,其漂白性增强 |
| C.向饱和氯水中通入氯气,c(H+)/c(ClO一)减小 |
| D.向氯水中加入NaOH至中性,溶液中c(Na+)=c(Cl一)+c(CIO一) |
常温下,pH=3的一元酸和pH=13的氢氧化钠溶液等体积混合后(不考虑混合后溶液体积的变化),恰好完全反应。下列说法不正确的是
| A.两溶液混合反应后的所得的混合溶液呈碱性 |
| B.所用酸溶液的浓度大于所用氢氧化钠溶液的浓度 |
| C.若酸为醋酸,原醋酸溶液中有1%的醋酸已电离 |
| D.若酸为醋酸,反应后的溶液中CH3OO-与CH3COOH的平衡浓度之和约为0.05mol?L-1 |
下列有关实验原理,方法和结论都正确的是 ( )
| A.某钠盐溶液中加入盐酸酸化的硝酸钡溶液有白色沉淀,该钠盐一定是硫酸钠 |
| B.在硫酸钡中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,说明K10(H2SO4)>K10(BaCO3) |
| C.新制氯水中加入碳酸钙粉末搅拌,过滤、滤液中c(HC1O)将增大 |
| D.相同质量的两份锌粒分别加入足量稀硫酸,在一份中加入少量CuSO4·5H2O,其反应速率将加快,且最终产生的H2与另一份相同 |
标准状况下,VL氨气溶解在1L水中(水的密度近似为1g/ml)所得溶液的密度为ρg/ml,质量分数为ω,物质的量浓度为cmol/L,则下列关系中不正确的是( )
| A.c=1000ρω/17 | B.ω=17c/1000ρ |
| C.ω=17V/(17V+22400) | D.c=Vρ/(17V+22400) |
在常温下,10mLpH=10的KOH溶液中,加入pH=4的CH3COOH溶液至pH刚好等于7(假设反应前后体积不变),则对反应后溶液的叙述正确的是
| A.c(CH3COO-)< c (K+) |
| B.c(H+) = c(OH-)< c(K+)< c(CH3COO -) |
| C.V总> 20mL |
| D.V总 < 20mL |
试题篮
()