(1)25℃,柠檬水的pH是3,其中c(OH-)==
(2)下列溶液中,c(H+)由小到大的排列顺序是
① 0.1mol/L HCl 溶液 ② 0.1mol/L H2SO4溶液
③ 0.1mol/L NaOH溶液 ④0.1mol/L CH3COOH溶液
(3)在25℃时,1mol· L-1的①(NH4)2SO4 ②CH3COONH4 ③(NH4)2Fe(SO4)2 ④NH4Cl的溶液中,c(NH4+)由大到小的顺序为
(4)pH=3盐酸和pH=11氨水等体积混合后溶液呈 性(选填“酸”、“中”或“碱”),溶液中c(NH4+) c(Cl-)(选填“ >”“=”“<” )。
下列说法正确的是
| A.pH=5的盐酸,再加水冲稀1000倍,溶液的pH=8 |
| B.给稀醋酸溶液加热,溶液pH值增大 |
| C.pH=1的盐酸中c(H+)是pH=3的盐酸的c(H+)100倍 |
| D.在H2CO3溶液中,C(H+) :C(CO32—-)=2∶1 |
 向体积为 Va的0.05mol·L-1CH3COOH溶液中加入体积为Vb的0.05mol·L-1KOH溶液,下列关系错误的是
向体积为 Va的0.05mol·L-1CH3COOH溶液中加入体积为Vb的0.05mol·L-1KOH溶液,下列关系错误的是
A.Va>Vb时:c (CH3COOH) +c (CH3COO-)>c (K+) |
B.Va=Vb时:c (CH3COOH) +c (H+)>c (OH-) |
C.Va<Vb时:c (CH3COO-)>c (K+)> c (OH-)> c (H+) |
D.Va与Vb任意比时:c (K+)+ c (H+) =c (OH-)+ c (CH3COO-) |
用0.1mol·L—1的盐酸滴定0.1mol·L—1的氨水,在滴定过程中不可能出现的结果是
| A.c(NH4+)>c(Cl-),c(OH-)>c(H+) |
| B.c(NH4+)=c(Cl-),c(OH-)=c(H+) |
| C.c(Cl-)>c(NH4+),c(OH-)>c(H+) |
| D.c(Cl-)>c(NH4+),c(H+)>c(OH-) |
下列说法正确的是 ( )
| A.90℃时,纯水的pH等于7 |
| B.已知一种c (H+)=1×10-3mol/L的酸和一种c (OH-)=1×10-3mol/L碱溶液以等体积混合后,溶液呈酸性,其原因是浓的弱酸和稀碱反应所致 |
| C.配制FeCl3溶液,为了抑制水解,常加稀硫酸 |
| D.在Na2S溶液中,离子浓度的关系是:c (Na+)>c (S2-)>c (HS-)>c (OH-)>c (H+) |
下列说法正确的是 ( )
| A.增大反应物浓度,可增大单位体积内活化分子的数目,从而使反应速率增大 |
| B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.pH值为7的溶液一定呈中性 |
| D.pH=3的盐酸和pH=11的氨水溶液,溶质的浓度和导电能力均相同 |
下列说法正确的是
| A.向0.1 mol/L Na2CO3溶液中滴加酚酞,溶液变红色 |
| B.Al3+、NO、Cl-、CO、Na+可大量共存于pH=2的溶液中 |
| C.乙醇和乙酸都能溶于水,都是电解质 |
| D.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同 |
常温离子液体(又称常温熔融盐),是当前化学研究的热点和前沿。1914年报道的第一种离子液体硝酸乙基铵[(C2H5NH3)NO3]的熔点为12℃。已知C2H5NH2的化学性质与NH3相似,下列有关硝酸乙基铵的说法中,正确的是
| A.该离子液体可以作为电池的电解质 |
| B.硝酸乙基铵水溶液呈碱性 |
| C.(C2H5NH3)NO3能与NaOH反应产生NH3 |
| D.硝酸乙基铵水解的离子方程式可表示为:C2H5NH3++H2O=C2H5NH2+H3O+ |
已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]―,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍。因此,必须对含铬的废水进行处理,可采用以下还原法,在酸性介质中用FeSO4等将+6价铬还原成+3价铬。
具体流程如下: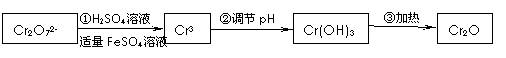
有关离子完全沉淀的pH如下表:
| 有关离子 |
Fe2+ |
Fe3+ |
Cr3+ |
| 完全沉淀为对应氢氧化物的pH |
9.0 |
3.2 |
5.6 |
(1)写出Cr2O72―与FeSO4溶液在酸性条件下反应的离子方程式 。
(2)还原+6价铬还可选用以下的 试剂(填序号)。
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀。
在操作②中调节pH应分2次进行,第1次应先调节溶液的pH范围约在 (填序号)最佳,第2次应调节溶液的pH范围约在 (填序号)最佳
A.3~4 B.6~8 C.10~11 D.12~14
用于调节溶液的最佳试剂为: (填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 |
HA物质的量浓度 (mol·L-1) |
NaOH物质的量浓度 (mol·L-1) |
混合溶液的pH |
| ① |
0.1 |
0.1 |
pH=9 |
| ② |
c |
0.2 |
pH=7 |
| ③ |
0.2 |
0.1 |
pH<7 |
请回答:
(1)从第①组情况分析,HA是强酸还是弱酸 。该组所得混合溶液中由水电离出的c(OH-) = mol·L-1。
(2)第②组情况表明,c 0.2(选填“大于”、“小于”或“等于”)。该混合液中离子浓度c(A-)与c(Na+)的大小关系是 。
(3)从第③组实验结果分析,说明此时HA的电离程度 NaA的水解程度(选填“大于”、“小于”或“等于”),该混合溶液中各离子浓度由大到小的顺序是 。
(4)由上述所涉及的溶质组成以下四组等体积溶液:
甲:0.1mol/LNaA; 乙:0.1mol/LNaA和0.1mol/LHA;
丙:0.1mol/LHA; 丁:0.1mol/LNaA和0.1mol/LNaOH;
则A-离子浓度由大到小的顺序为 > > > 。(填写序号)
下列叙述中,不正确的是
| A.0.1 mol?L-1 CH3COOH溶液加水稀释,n(H+)增大 |
| B.0.2 mol?L-1盐酸与等体积0.05 mol?L-1 Ba(OH)2溶液混合后,溶液pH为1 |
| C.向含等浓度的KCl和KI的混合溶液,滴加少量AgNO3溶液生成黄色沉淀,说明同温度下Ksp(AgCl)大于Ksp(AgI) |
| D.若NH4HCO3溶液、NH4HSO4溶液和NH4NO3溶液中c(NH4+)相等,则 |
c(NH4HSO4) < c(NH4NO3) < c(NH4HCO3)
下列反应的离子方程式正确的是
| A.物质的量浓度相等的碳酸氢钡溶液和氢氧化钠溶液等体积混合 Ba2+ + 2HCO3- + 2OH- = BaCO3↓+CO32- + 2H2O |
|
| B.NaHSO4溶液中滴加入Ba(OH)2溶液至中性 电解 |
C.以石墨作电极电解氯化镁溶液:2Cl-+2H2O ="==" 2OH-+H2↑+Cl2↑ |
D.碳酸氢钠溶液加入氯化铝溶液 3HCO3-+Al3+ 3CO2+Al(OH)3 3CO2+Al(OH)3 |
已知:弱酸HCN(aq)与NaOH(aq)反应的△H = +12.1kJ/mol; HCl(aq)与NaOH(aq)反应的
△H =-55.6kJ/mol 。则HCN在水溶液中电离的△H等于:
| A.-67.7Kj/mol | B.+67.7 kJ/mol | C.+43.5 kJ/mol | D.-43.5kJ/mol |
有体积相同、pH相等的烧碱溶液和氨水,下列叙述中正确的是
| A.两溶液溶质物质的量浓度相同 |
| B.用同浓度的盐酸中和时,消耗盐酸的体积相同 |
| C.两溶液中OH-离子浓度相同 |
| D.加入等体积的水稀释后,它们的pH仍相等 |
试题篮
()