2015年某市决定开工建设垃圾焚烧发电厂,以改善目前填埋方式处理垃圾对环境产生的不良影响。其建成后既能利用垃圾,也能利用前期填埋垃圾产生的沼气,作为焚烧的原料。
(1)认为这样做的好处是 。(至少答两点)
(2)前期填埋的垃圾中易腐败的有机物在一定条件下被细菌分解为沼气,沼气的成分是__________(填名称)。写出沼气燃烧的化学方程式: 。
汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染物,治理的方法之一是在汽车的排气管上装上“催化转换器”(用钯、铂合金作催化剂)。它的特点是使 CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)写出CO与NO反应的化学方程式____________________。
(2)“催化转换器”的缺点是在一定程度上提高了空气的酸度。其原因是___________________。
(3)控制城市污染源的方法可以有___________________。
保护环境、保护地球是人类共同的呼声。
① “阅兵蓝”为2015年科技热词。较多排放下列气体不利于蓝天出现的是 (填字母)。
a.NO2 b.N2 c.CO2
② 天然水中含有的细小悬浮颗粒可用 (填字母)作混凝剂进行吸附沉降。
a.Cl2 b.KAl(SO4)2·12H2O c.NaClO
③ 工业废水中含有的Cr3+可用熟石灰作沉淀剂,在pH为8~9 时生成沉淀而除去,生成的沉淀化学式为 。
(2) 食品和药品关系人的生存和健康。
① 下列人体必需元素中,过多摄入 (填字母,下同)元素会引起甲状腺疾病,在牙膏中添加含 元素的化合物可以防治龋齿,儿童缺乏 元素会引发佝偻病。
a.碘b.氟c.钙d.铜
② 下列是生活常用的物质:
a.碳酸氢钠 b.青霉素 c.葡萄糖 d.苯甲酸钠
e.柠檬黄 f.阿司匹林 g.维生素C
上述物质中可用作食品着色剂的是 (填字母,下同);可直接进入血液补充能量的是 ;可用作食品防腐剂的是 ;属于抗生素的是 。
(3) 材料是人类赖以生存和发展的重要物质基础。
① 下列属于复合材料的是 (填字母)。
a.有机玻璃 b.钢化玻璃 c.玻璃钢 d.石英玻璃
② 1928年美国杜邦公司首先合成了尼龙,由尼龙制成的尼龙丝耐磨、柔韧、有光泽,可作为丝绸的代替品,尼龙属于 (填字母)。
a.有机高分子材料 b.无机非金属材料 c.金属材料
③ 制造下列物质时,需要石灰石的是 (填字母)。
a.水泥b.光导纤维 c.陶瓷
④ 钢铁是人类生产和生活中非常重要的材料,但每年因锈蚀而损失的数量十分惊人。铁器件在潮湿的空气中会发生 腐蚀(填“化学”或“电化学”),为防止铁质地下管道的腐蚀可在其表面附着 (填“锌块”或“石墨”)。
(1)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①维生素C能增强人体对疾病的抵抗能力,促进人体生长发育,中学生每天要补充60mg的维生素C。下列物质含有丰富维生素C的是 (填字母)。
A.牛肉 B.辣椒 C.鸡蛋
②青少年及成人缺乏某种微量元素将导致甲状腺肿大,而且会造成智力损害,该微量元素是 (填字母)
A.碘 B.铁 C.钙
③蛋白质是人体必需的营养物质,它在人体内最终分解为 (填字母)。
A.葡萄糖 B.氨基酸 C.脂肪酸
(2)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是 。
②玻璃是重要的硅酸盐产品。生产玻璃时,石灰石与石英反应的化学方程式为 。
③铁是人们生活中常用的金属材料,请列举两种防止铁制品被腐蚀的方法: , 。
(3)保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处。
①pH< 的雨水称为酸雨;向煤中加入适量的 ,可以大大减少燃物产物中SO2的量。
②对汽车加装尾气催化净化装置,可以使其中的NO、CO相互反应转化成无毒的气体,其原理可以用化学方程式表示为 。
③天然水中杂质较多,常需加入明矾,ClO2等物质处理后才能饮用。加入ClO2的作用是 ;加入明矾后, 水解的离子方程式是 。
水解的离子方程式是 。
大气污染物根据组成成分,可分为_________、_________( )、_________( )、_________、_________,以及_________(常用作_________,商品名为_________)等。
呵护生存环境,共建和谐社会。
(1)2010年10月世界气候大会在坎昆召开,各国共商大计,控制温室气体的排放,下列属于温室气体的是 (填序号)。
① SO2 ② CO2 ③ N2
(2)自行车的部分构件有:①钢圈 ②轮胎 ③车灯外壳。其中属于合金的是 ;属于有机合成材料的是 (每空只填一种构件的序号)。
(3)废旧的钢圈、轮胎应投入如图所示 (填“A”或“B”)标志的垃圾桶中。
SO2和NOx都是大气污染物。
(1)直接排放含SO2的烟气会形成酸雨,危害环境。用化学方程式表示SO2形成硫酸型酸雨的过程 。
(2)右表是某小组同学测得的不同天气情况下的某县城空气中SO2的平均含量。请你分析雨后或风速较大时SO2平均含量较低的原因:
①雨后:_________________;
②风速较大时:____________________。
(3)洗涤含SO2的烟气。以下物质不能作为洗涤剂的是________(填字母序号)。
a.熟石灰 b.纯碱 c.CaCl2 d.NaHSO3
(4)煤燃烧前需进行脱硫处理,某种脱硫技术的基本原理如下:
①该技术的第一步反应的离子方程式为 。
②处理1 kg含80% FeS2的黄铁矿,第二步消耗O2(标况)的体积为 L(保留一位小数)。
(5)某研究性学习小组为模拟光化学烟雾的形成,用紫外线照射装在密闭容器内的被污染空气样品,所得物质的浓度随时间的变化如图所示。由图可知,光化学烟雾是指等污染物气体和颗粒物所形成的烟雾。
(6)氧化—还原法消除NOx的转化如下:
①反应Ⅰ为NO+O3=NO2+O2,生成11.2 L O2(标况)时,转移电子的物质的量是 mol。
②反应Ⅱ中,反应的化学方程式是 。
(7)利用氨水可以将SO2和NO2吸收,原理如下图所示:
NO2被吸收的离子方程式是 。
防治环境污染,改善生态环境己成为全球的共识。
(1)垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有 (填字母)标志的垃圾筒内。
(2)工业废水需处理达标后才能排放。下列废水处理的方法合理的是 (填字母)。
a.用中和法除去废水中的酸 b.用混凝法除去废水中的重金属离子
c.用氯气除去废水中的悬浮物 d.用氧化还原法除油类、氰化物
(3)为了减少煤燃烧产生的SO2对大气造成的污染,可向煤中加入适量石灰石。石灰石与煤燃烧时产生的SO2及空气中的O2反应,生成CaSO4和CO2,写出该反应的化学方程 。
(4)为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量。为控制大气中二氧化硫的排放,常采取的措施是对化石燃料进行 。对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为 。
当前环境问题,如酸雨、温室效应、臭氧层破坏、光化学烟雾、有毒物质的污染等,已成为世界各国普遍关注和研究的问题。请用序号回答:
(1)导致酸雨的主要气体是 。 ① N2 ② CO2 ③ SO2
(2)使臭氧层受到破坏的主要气体是 。 ①氟氯代烷 ② H2 ③二氧化碳
(3)造成居室污染的气体是______。 ① N2 ② CO ③ CO2
(4)解决能源短缺问题的一种方法是 。①开发新能源②加速煤、石油的开采
(1)防治环境污染、改善生态环境已成为全人类的共识。
①下列各项中,完成空气质量报告时不需要监测的是 (填字母)。
a.氮的氧化物 b.硫的氧化物 c.可吸入颗粒物 d.氟氯代烃 e.二氧化碳
②水是一种宝贵的自然资源。下列物质可用于水体消毒的是 ___(填字母)。
a.明矾 b.氯化铁 c.漂白粉
③垃圾焚烧是产生 __的主要途径之一(填字母)。
a.二噁英 b.SO2 c.NH3
(2)材料是人类赖以生存和发展的重要基础物质。
①潜水员乘坐的潜水钟以钢铁为主要制造材料。钢铁容易在潮湿空气中发生 腐蚀,其正极的电极反应式是 。
②随着科学技术的发展,科学家研制了氮化硅等许多耐高温的物质,它们属于___(填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
③在尼龙、棉花、涤纶这三种物质中,属于天然纤维的是__ 。
(3)营养平衡、合理用药是保证人体健康和生活质量的重要途径。
①有些药片常用淀粉作为黏合剂,淀粉进入人体后在人体内酶的催化作用下逐步水解,写出淀粉水解的方程式___________________,检验淀粉水解产物的试剂是______________。
②糖类、油脂、蛋白质都能为人体提供能量,等质量的糖类、油脂、蛋白质为人体提供能量最多的是________________。
③“服用维生素C,可使食物中的Fe3+变为Fe2+”这句话指出,维生素C在这一反应中作_________剂。
④阿司匹林( )与氢氧化钠反应可制得可溶性阿司匹林,疗效更好。写出阿司匹林与氢氧化钠的反应方程式_______________________________。
)与氢氧化钠反应可制得可溶性阿司匹林,疗效更好。写出阿司匹林与氢氧化钠的反应方程式_______________________________。
(4)合理饮食和正确使用药物,是人体健康的重要保证。
①1838年,林则徐在广东虎门销毁大量的鸦片,打击了当时烟贩的嚣张气焰。下列药物中属于毒品的是 。
A.砒霜B.阿司匹林 C.甲基苯丙胺(冰毒)
②均衡的膳食结构可以保障身体健康,但并不是所有的食物均可以被人体吸收利用。下列营养物质不能被人体吸收利用的是 。
A.蛋白质B.纤维素C.无机盐
③微量元素在人体内含量极少,其质量不到体重的万分之一,但它们对维持生命活动、促进健康和生长发育有重要的作用。碘被称之为“智力元素”,下列物质 是目前在碘盐中添加的含碘化合物。
A.碘酸钾 B.碘单质 C. 碘化钾
(5)合理使用材料,改善人类生活。
①橡胶是制造轮胎的重要原料,天然橡胶通过硫化处理,使它的分子转化为 结构(填“线型”或“体型”),从而增大橡胶的强度;向其中加入 可以增大轮胎的耐磨性。
②玻璃制品在日常生活中的使用量很大,普通玻璃的原料有石英、 、石灰石,通常的玻璃呈浅绿色,是因为含有 (填离子)。彩色玻璃中是因为添加某些金属氧化物,红色玻璃是因为添加 (填化学式)。
③氧气和四氯化硅蒸气在旋转的高温炉中发生罝换反应,其产物之一可制得光导纤维,试写出该反应的化学方程式 。
研究化肥的合成、废水的处理等有现实的重要意义。
(1)工业生产中,以NH3为原料制硝酸,写出工业生产硝酸最后一步的化学方程式 。
(2)甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同:
已知:CO+H2O CO2+H2;
CO2+H2;
按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,则对原料的利用率最高。现有甲、乙、丙三家工厂生产原料如下:
甲厂以焦炭和水为原料;
乙厂以天然气和水为原料;
丙厂以石脑油(主要成分为C5H12)和水为原料。
请根据上述信息判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高:________(填“甲”、“乙”或“丙”)。
(3)将工厂废气中产生的SO2通过下列流程,可以转化为有应用价值的硫酸钙等。
①写出反应Ⅰ的化学方程式:_________________________________。
②生产中,向反应Ⅱ的溶液中加入强还原性的对苯二酚等物质,目的是_____________。
③检验经过反应Ⅲ得到的铵态氮肥中SO42-所用试剂是_______________________。
(4)为减少环境污染,工业上也常用Na2CO3溶液吸收制取HNO3产生的尾气中的NO2,生成NaNO3、NaNO2和一种气体,写出反应的化学方程式 。
当前环境污染问题越来越严重,如酸雨、温室效应、臭氧层破坏、有毒物质的污染、汽车尾气的污染、水体污染等已成为世界各国普遍关注和研究的问题。
请回答:
(1)引起温室效应的主要气体是———————————(填序号,下同)。①SO2②CO2
(2)造成居室污染的物质是——————————————。①甲醛②氮气
(3)造成水体污染的原因是——————————————。
①生活污水的任意排放②工业废水的任意排放
(4)为了治理汽车尾气的污染问题,可以在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成CO2和N2,写成该反应的化学方程式:__________________ 。
分析城市空气样本,主要污染物为可吸入颗粒物pm2.5、SO2、NOx等,其主要来源为燃煤和机动车尾气排放等。
(1)某同学为检测样本中所含成份,将样本用蒸馏水处理制成待测试样,设计实验及实验现象如下: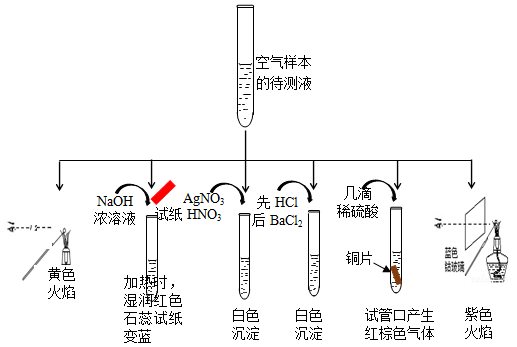
① 该实验能确认存在的阳离子是 。
② 该实验检测出样本中有NO3-,根据是(用化学方程式解释) 。
③ 根据该实验能否确定样本中含有SO32-, (填“能”或“否”) ,若要确定SO32-,所需的实验药品可以是 。
(2)燃煤厂为减少SO2的排放,可采取的措施是:
① 洗涤含SO2的烟气,下列物质可作洗涤剂的是______。
a.浓NH3∙H2O b.NaHCO3 c.FeCl3 d.NaHSO3
② 将煤转化为清洁气体燃料,过程如图所示: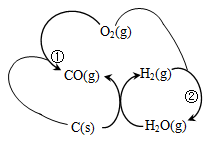
已知:反应①生成1molCO(g)的反应热△H= -110.5KJ/mol反应②生成1molH2O(g)的反应热△H= -241.6KJ/mol焦炭与水蒸气反应的热化学方程式是________________。
(3) 汽车尾气处理系统可将CO和NO转化成无毒物质,其化学反应方程式是________________
(4)为将CO和NO转化为无毒物质,某同学设计了如图装置。
①电极a是________极;
②甲的化学式是 ;
③电极b的电极反应式是____________。
2011年12月13日,加拿大正式宣布将退出《京都议定书》,这使CO2的排放问题再次成为了热点。当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
I.最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,在一定条件下与H2反应,使之变为可再生燃料甲醇。其流程如下:
①上述流程中碳酸钾溶液所起的作用是 。
②在分解池中发生的反应为 (写出化学方程式)。
Ⅱ.碳酸钾是重要的无机化工、医药、轻工原料之一,主要用于医药、玻璃、染料等工业, 可用作气体吸附剂,干粉灭火剂,橡胶防老剂等。
已知:CO2、碳酸盐、碳酸氢盐的部分性质如下:
CO2(过量)+OH-=HCO3-HCO3-+OH-=CO32-+H2O
CO32-与H+反应生成CO2分两步:
CO32-+H+=HCO3-;HCO3-+H+=H2O+CO2↑
①小王同学在实验室用如图所示的装置和药品制取K2CO3溶液。
他所制得的溶液中可能含有的杂质是 。
②该同学在数字实验室中用传感器对碳酸钾和碳酸氢钾的混合物样品进行成分测定,他分别称取三份不同质量的混合物样品,配成稀溶液,然后分别逐滴加入相同浓度的50 ml硫酸,测得如下数据:
实验编号 1 2 3
混合物的质量/g 3.76 4.70 8.46
硫酸溶液的体积/mL 50.00 50.00 50.00
生成二氧化碳的物质的量/mol 0.03 0.0375 0.03
试计算:该混合固体中K2CO3与KHCO3的物质的量之比是 所用硫酸的物质的量浓度为 mol•L-1。
为了人类的可持续发展,我们应综合利用资源.保护环境,跟自然和谐相处:
(1)科学家研制出有“自我修复能力”的塑料。塑料属于 (选填 “无机”、“合成”或“复合”)材料,为我们到来了方便,但废弃塑料处理不当会对环境造成不利的影响,人们把废弃塑料给环境带来的危害称为“ ”,发电厂是利用垃圾焚烧产生的 转变为电能。
(2)发射“嫦娥三号”的长三甲火箭燃料是偏二甲肼(X),反应的化学方程式为:X+2N2O4=3N2+2CO2+4H2O,则X的化学式为 。
A.H2 B.CH4 C.C2H8N D.C2H8N2
(3)2014年3月22日是第二十二个“世界水日”,它的主题是“水与能源”。关于水的知识有下列话题,请按要求填空:
①自来水生产过程中,可用 方法除去水中不溶性杂质。
②在生产生活中水是最常用的溶剂,实验室用蔗糖配制一定溶质质量分数的溶液时,可能涉及以下操作:
Ⅰ、上图操作中有错误的是 (填序号)。
Ⅱ、改正错误后,表示正确的操作顺序是 (填序号)。
A.⑤②①③④ B.⑤①②③④ C.⑤③②④① D.⑤③①④②
Ⅲ、保护水环境、珍爱水资源,是每个公民应尽的责任和义务。下列做法不利于保护水资源的是 (填序号)。
A.大量使用化肥农药 B.工业废水处理达标后再排放
C.使用含磷洗衣粉D.生活污水直接排放
试题篮
()