对于反应aA+bB==dD+eE,若已知40g A可恰好与21g B完全反应生成28g D,则B与E的摩尔质量比为
| A.7a:10d | B.10a:7d | C.10b:7e | D.7e:11b |
在1500C加热高氯酸铵发生分解反应:2NH4ClO4=N2+Cl2+2O2+4H2O,在1500C时其气态生成物组成的混合气的平均相对分子质量为
| A.71.75 | B.29.375 | C.14.69 | D.无法计算 |
在一个密闭的容器内有四种物质,高温下发生反应,一段时间后
| |
a |
b |
c |
d |
| 反应前质量(g) |
8 |
10 |
1 |
25 |
| 反应后质量(g) |
未测 |
24 |
2 |
16 |
若a的相对分子质量为2n,d的相对分子质量为3n,则该反应的化学方程式中a与d的化学计量数比为
A.1:1 B.1:2 C.1:3 D.2:3
学习化学要准确掌握化学基本概念和研究方法。按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表:
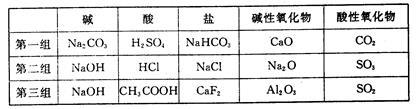
找出上述三组分类中的错误,错误物质的化学式为 。
(2)下列2个反应,按要求填写相关量。
①2Na2O2+ 2H2O=4NaOH+O2反应中,每消耗lmol Na2O2生成 g O2;
②除去NaCl溶液中少量的Na2SO4杂质,要判断所加BaCl2溶液是否过量,可向滤液中加入X溶液,X可以是 (填代号)
A.NaOH B.AgNO3 C.HCl D.Na2SO4
(3)配平下面化学方程式,回答下列问题:
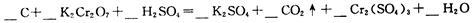
①H2SO4在上述反应中表现出来的性质是(填选项编号) .
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
②若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为_____L。
(4)在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,按要求回答下列问题:
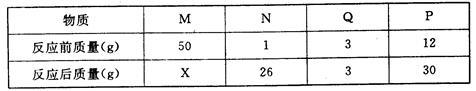
该变化的基本反应类型是 反应,Q物质的作用为 。
一定量的质量分数为14%的氢氧化钾溶液,若将其蒸发掉50 g水后,其溶质质量分数恰好扩大一倍,体积变为62.5 mL,则浓缩后溶液的物质的量浓度为
| A.2.2 mol/L | B.4 mol/L |
| C.5 mol/L | D.6.25 mol/L |
下列表示溶液中发生反应的化学方程式错误的是
A.MnO 2 +4HCl(浓)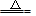 MnCl2 +Cl 2↑+2H2 O MnCl2 +Cl 2↑+2H2 O |
| B.K2Cr2O7 +6FeSO4 +7H2SO4 =Cr2(SO4)3 +3Fe2(SO4)3 +K2SO4 +7H2O |
| C.2Al+2NaOH+2H2O=2NaAlO2 +3H2↑ |
| D.2KMnO 4 +HCOOK+KOH=2K2MnO4 +CO2 ↑+H 2O |
有硫酸镁溶液500 mL,它的密度是1.20 g/cm3,其中镁离子的质量分数是4.8%,则有关该溶液的说法不正确的是
| A.硫酸根离子的质量分数是19.2% |
| B.溶质的质量分数是24.0% |
| C.溶液的物质的量浓度是2.4 mol/L |
| D.溶质和溶剂的物质的量之比是1∶40 |
(12分)某合金可能由铜与镁、锌中的一种组成,现欲测定其组成,进行如下实验:取该合金样品10.0 g放入烧杯中,然后将56.0 g溶质质量分数为14.0%的稀硫酸平均分四次依次加入该烧杯中,每次均充分反应。实验数据记录如下表:
试求:
(1)该合金中铜的质量分数是__________。
(2)该合金除了铜外,另一种金属的是什么呢?(写出过程)
(3)第三次加入硫酸充分反应后,所得溶液中溶质的质量分数是多少?(写出计算过程,结果精确到0.1%)
将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下。下列说法错误的是
| 物 质 |
a |
b |
c |
d |
| 反应前质量/g |
6.40 |
3.20 |
4.00 |
0.50 |
| 反应后质量/g |
待测 |
2.56 |
7.20 |
0.50 |
A.a和b是反应物,d可能是催化剂
B.反应后a物质的质量为4.64g
C.a和b两种物质中所包含的元素种类与c物质中的元素种类相同
D.若物质a与物质b的相对分子质量之比为2﹕1,反应中a与b的化学计量数(系数)之比为2﹕l
向一定量的饱和NaOH溶液中加入少量Na2O固体,恢复到原来温度时,下列说法中正确的是
| A.溶液中的Na+总数不变 | B.单位体积内的OH-数目不变 |
| C.溶质的质量分数不变 | D.溶液的质量不变 |
根据下图中A、B两种固体物质的溶解度曲线,回答下列问题:
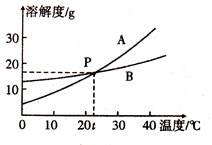
(1)10oC时,将10gB溶于100g水中,形成溶液的质量是 ,将它变成饱和溶液可采用的一种方法是 。
(2)P点的含义是 。在30oC时,A、B两物质饱和溶液的溶质质量分数的大小关系为A B(填“>”“<”或“=”)。当A中含有少量B 时,提纯A所采用的方法为 。
推理是一种重要的学习和研究方法。下列推理正确的是( )
| A.单质中只含一种元素,所以只含一种元素的物质一定是单质。 |
| B.化学变化前后物质的质量总和不变,所以1gH2和1gO2一定能够生成2gH2O |
| C.碱性溶液能使酚酞溶液变红,所以能使酚酞溶液变红的物质一定呈碱性 |
| D.中和反应有盐和水生成,所以有盐和水生的反应一定是中和反应 |
我国北方某盐湖生产的纯碱(Na2CO3)产品中常含少量的氯化钠,为测定该产品中碳酸钠的质量分数,现称取6g样品于烧杯内,滴加稀盐酸至烧杯内溶液的PH=7,消耗稀盐酸的质量为36.5g,同时测得反应后溶液的总质量为40.3g。请计算:
(1)反应生成的气体质量为 g。
(2)该样品中碳酸钠的质量分数。(结果精确至0.1%)
结构决定物质的性质、变化,请结合下图回答问题。
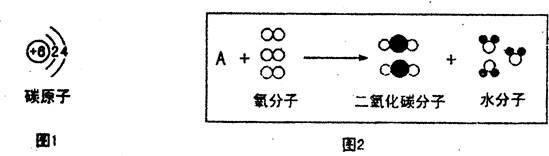
(1)由图1可知,在常温下,碳的化学性质不活泼的微观原因是 ;
(2)图2中A的化学式可能是 ,写出与图2反应微观本质不同的一个化学方程式 。
试题篮
()