在一定温度和压强条件下发生了反应:CO2(g)+3H2 (g) CH3OH(g)+H2O(g) △H<0,反应达到平衡时,改变温度(T)和压强(p),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(p)的关系判断正确的是
CH3OH(g)+H2O(g) △H<0,反应达到平衡时,改变温度(T)和压强(p),反应混合物CH3OH“物质的量分数”变化情况如图所示,关于温度(T)和压强(p)的关系判断正确的是

| A.P3>P2 T3>T2 | B.P2>P4 T4>T2 |
| C.P1>P3 T3>T1 | D.P1>P4 T2>T3 |
Bodensteins研究了下列反应:2HI(g) H2(g) + I2(g) △H=+11kJ/mol
H2(g) + I2(g) △H=+11kJ/mol
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
| t/min |
0 |
20 |
40 |
60 |
80 |
120 |
| x(HI) |
1 |
0.91 |
0.85 |
0.815 |
0.795 |
0.784 |
| x(HI) |
0 |
0.60 |
0.73 |
0.773 |
0.780 |
0.784 |
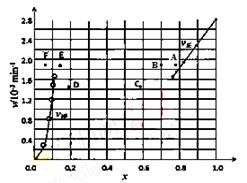
由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为:
A.B F B.A E C.B E D.A D
关于下列各图的叙述正确的是
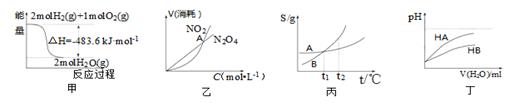
A.甲表示H2与O2发生反应过程中的能量变化,则H2的标准燃烧热为△H=-483.6kJ·mol-1
B.乙表示恒温恒容条件下发生的可逆反应2NO2 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将tl℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH
体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+ O2 2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率p%,则乙容器中SO2的转化率为
2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率p%,则乙容器中SO2的转化率为
| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
25℃时,水的电离达到平衡:H2O H++OH―;ΔH>0,下列叙述正确的是
H++OH―;ΔH>0,下列叙述正确的是
| A.向水中加人稀氨水,平衡逆向移动,c(OH―)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加人少量固体NaCl,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
在恒压容器a和恒容容器b中,分别充入体积比为1∶3的N2和H2。若开始时两容器的体积相等,且在相同的条件下达到平衡时,两容器的N2的转化率应当是( )
| A.a中大 | B.b中大 | C.a、b一样大 | D.无法判断 |
将一定量的Ag2SO4固体置于容积不变的容器中,在某温度下发生下列反应:
Ag2SO4(s) Ag2O(s)+SO3(g)、2SO3(g)
Ag2O(s)+SO3(g)、2SO3(g) 2SO2(g)+O2(g) ,经10分钟反应达到平衡,此时c(SO3)="0.4" mol/L,c(O2)="0.05" mol/L,下列叙述不正确的是( )
2SO2(g)+O2(g) ,经10分钟反应达到平衡,此时c(SO3)="0.4" mol/L,c(O2)="0.05" mol/L,下列叙述不正确的是( )
| A.SO3的分解率为20% | B.10分钟内ν(SO2)=0.01mol/(L·min) |
| C.容器内气体的密度为40g/L | D.加压,容器内固体的质量不变 |
对于反应2NO2(g) N2O4(g)达到平衡后,在温度不变时欲使c(NO2)/c(N2O4)比值增大,可以采取( )
N2O4(g)达到平衡后,在温度不变时欲使c(NO2)/c(N2O4)比值增大,可以采取( )
| A.体积不变,增加NO2的量 | B.体积不变,增加N2O4的量 |
| C.使体积扩大到原来的2倍 | D.使体积不变充入N2 |
已知反应:CO(g) +3H2 (g)  .CH4 (g)+H2O(g)。起始以物质的量之比为1:1充人反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为)。下列有关说法正确的是
.CH4 (g)+H2O(g)。起始以物质的量之比为1:1充人反应物,不同压强条件下,H2的平衡转化率随温度的变化情况如图所示(M、N点标记为)。下列有关说法正确的是
| A.上述反应的△H<0 |
| B.N点时的反应速率一定比M点快 |
| C.降低温度,H2的转化率可达到100% |
| D.工业用此法制取甲烷应采用更高的压强 |
在密闭容器中进行如下反应:X2(g)+Y2(g) 2Z(g),已知
2Z(g),已知 、
、 、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A.Z为0.3mol/L | B. 为0.4mol/L 为0.4mol/L |
C. 为0.2mol/L 为0.2mol/L |
D. 为0.4mol/L 为0.4mol/L |
将BaO2放入密闭的真空容器中,反应2BaO2(s) 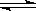 2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是( )
2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是( )
| A.平衡常数减小 | B.BaO量不变 | C.氧气浓度不变 | D.BaO2量减少 |
已知:C(s)+CO2(g)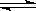 2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向逆方向进行的是
2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向逆方向进行的是
| A.升高温度和增大压强 | B.降低温度和减小压强 |
| C.降低温度和增大压强 | D.升高温度和减小压强 |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是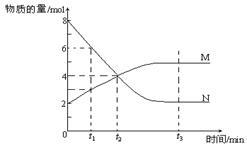
A.反应的化学方程式为:2 M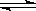 N N |
| B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.t1时,N的浓度是M浓度的2倍 |
四位同学在学习“化学反应速率和化学平衡”后,联系工业生产实际所发表的观点,你认为不正确的是
| A.化学反应速率理论是研究怎样在一定时间内快出产品 |
| B.化学平衡理论是研究怎样使用有限原料多出产品 |
| C.化学反应速率理论是研究怎样提高原料转化率 |
| D.化学平衡理论是研究怎样使原料尽可能多地转化为产品 |
试题篮
()