下列关于化学平衡的说法错误的是
| A.化学平衡描述的是可逆反应 |
| B.可逆反应达到化学平衡状态时,正、逆反应速率都为0 |
| C.可逆反应达到化学平衡状态时,v(正)=v(逆)≠0 |
| D.可逆反应达到化学平衡状态时,各组成成分浓度保持不变 |
某温度下 H2(g)+I2(g) 2HI(g)的平衡常数K="O.25" ,该温度下在甲、乙、丙三个恒容密闭容器中充入H2 (g)、 I2 (g),起始浓度如下表所示:
2HI(g)的平衡常数K="O.25" ,该温度下在甲、乙、丙三个恒容密闭容器中充入H2 (g)、 I2 (g),起始浓度如下表所示:
下列判断不正确的是( )
| A.平衡时甲中和丙中H2的转化率相同 |
| B.平衡时乙中I2的转化率小于40% |
| C.平衡时乙中c(HI)比甲中的2倍大 |
| D.反应平衡时,丙中气体颜色最深,乙中气体颜色最浅 |
已知反应:2CH3COCH3(l)  CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如右图所示。下列说法正确的是( )
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如右图所示。下列说法正确的是( )
| A.b代表0℃下CH3COCH3的Y-t 曲线 |
B.反应进行到20min末,CH3COCH3的 |
| C.升高温度可缩短反应达平衡的时间并能提高平衡转化率 |
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的 |
在一定温度下,向容积固定不变的密闭容器中充入a mol PCl5,发生如下反应:
PCl5(g) PCl3(g)+Cl2(g);达平衡后再向容器中充入amol PCl5,再次达到平衡后,与原平衡比较,下列叙述不正确的是 ( )
PCl3(g)+Cl2(g);达平衡后再向容器中充入amol PCl5,再次达到平衡后,与原平衡比较,下列叙述不正确的是 ( )
| A.混合气体的密度增大 |
| B.相对平均分子质量增大 |
| C.PCl5的转化率提高 |
| D.PCl5的质量分数增大 |
下列事实不能用勒夏特列原理解释的是( )
| A.配制FeSO4溶液时在溶液中加入稀硫酸 |
| B.温度控制在450℃有利于二氧化硫的催化氧化 |
| C.增大压强有利于合成氨反应 |
D.工业制取金属钾Na(l)+ KCl(l)  NaCl(l)+K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来 NaCl(l)+K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来 |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是
A.反应的化学方程式为:N  2M 2M |
B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率等于逆反应速率 | D.t3后,若升高温度则反应速率不一定增大 |
下列关于化学平衡状态的说法中正确的是( )
A 改变外界条件不能改变化学反应的平衡状态
B 当可逆反应在一定条件下达到反应限度时即达到了化学平衡
C 当可逆反应达到平衡状态时,该反应立刻停止不再进行
D当可逆反应达到化学平衡状态时,反应物和生成物的浓度一定相等
硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下,下列说法正确的是
| A.温度一定时,Ksp(SrSO4)随c(SO42-)的增大而减小 |
| B.三个不同温度中,313K时Ksp(SrSO4)最大 |
| C.283K时,图中a点对应的溶液是饱和溶液 |
| D.283K下的SrSO4饱和溶液升温到363K后变为不饱和溶液 |
在一定温度下,向a L密闭容器中加入1molX气体和2 molY气体,发生如下反应:X(g) + 2Y(g)  2Z(g) 此反应达到平衡的标志是( )
2Z(g) 此反应达到平衡的标志是( )
| A.正反应和逆反应的速率都为零 |
| B.容器内各物质的浓度不随时间变化 |
| C.容器内X、Y、Z的浓度之比为1∶2∶2 |
| D.单位时间消耗0.1molX同时生成0.2molZ |
对化学反应限度的叙述,错误的是
| A.任何可逆反应都有一定的限度 |
| B.化学反应达到限度时,正逆反应速率相等 |
| C.化学反应的限度与时间的长短无关 |
| D.化学反应的限度是不可改变的 |
对于可逆反应2SO2+O2 2SO3,在混合气体中充入一定量的18O2,足够长的时间后,18O原子
2SO3,在混合气体中充入一定量的18O2,足够长的时间后,18O原子
| A.只存在于O2中 | B.只存在于O2和SO3中 |
| C.只存在于O2和SO2中 | D.存在于O2、SO2和SO3中 |
对苯二酚是摄影业中常用显影剂,它在水中电离出的阴离子对已曝光的AgBr有显影作用,有关变化可表示为: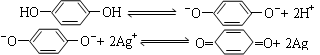
则在以对苯二酚为主要成分的显影液中,能使显影速度明显加快的添加剂是
| A.KBr | B.Na2CO3 | C.CH3COOH | D.H2O |
高温下,某反应达到平衡,平衡常数K=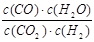 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
| A.该反应是焓变为正值 | B.该反应化学方程式为CO+H2O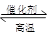 CO2+H2 CO2+H2 |
| C.升高温度,逆反应速率减小 | D.恒温下,缩小容器体积,H2浓度一定减小 |
一定条件下,下列不能用勒夏特列原理解释的是
| A.工业生产硫酸的过程中使用适当过量氧气,以提高SO2的转化率 |
| B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后气体颜色变深 |
| C.实验室用排饱和NaHCO3溶液的方法收集CO2气体 |
| D.新制氯水中,滴加硝酸银溶液,溶液颜色变浅,产生白色沉淀 |
向紫色Cr2(SO4)3溶液中,加入NaOH溶液至析出蓝灰色沉淀,此时,溶液中存在着如下平衡:Cr3+(紫色) +3OH-  Cr(OH)3(蓝灰色)
Cr(OH)3(蓝灰色)  CrO2- (绿色)+H+ + H2O,将上述悬浊液等分两份a和b。向a试管中加入适量的NaOH溶液,向b试管中加入适量的H2SO4溶液。a、b试管中溶液颜色最终分别为
CrO2- (绿色)+H+ + H2O,将上述悬浊液等分两份a和b。向a试管中加入适量的NaOH溶液,向b试管中加入适量的H2SO4溶液。a、b试管中溶液颜色最终分别为
| |
A |
B |
C |
D |
| a试管 |
紫色 |
蓝灰色 |
蓝色 |
绿色 |
| b试管 |
绿色 |
绿色 |
紫色 |
紫色 |
试题篮
()