一定温度下,下列叙述是可逆反应A(g)+3B(g)  2C(g)在定容密闭容器中达到平衡的标志的是:( )
2C(g)在定容密闭容器中达到平衡的标志的是:( )
①C的生成速率与C的分解速率相等;
②单位时间内amol A生成,同时生成3amolB;
③A、B、C的浓度不再变化;
④混合气体的总压强不再变化;
⑤混合气体的平均摩尔质量不再变化;
⑥用A、B、C的物质的量浓度变化表示的反应速率之比为1:3:2;
⑦A、B、C的分子数目比为1:3:2;
⑧混合气体的密度不再变化
A.②⑤ B.①③④⑤ C.②⑥⑦⑧ D.⑤⑥⑧
某温度下,某反应达平衡时平衡常数K= 。恒容时,温度升高,H2的浓度减小。下列说法正确的是
。恒容时,温度升高,H2的浓度减小。下列说法正确的是
| A.恒温恒容下,增大压强,H2的浓度一定减小 |
| B.该反应的焓变为正值 |
| C.升高温度,逆反应速率减小 |
D.该反应的化学方程式为CO+H2O CO2+H2 CO2+H2 |
一定条件下,体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) Z(g),经60 s达到平衡,生成0.3 mol Z。下列说法正确的是
Z(g),经60 s达到平衡,生成0.3 mol Z。下列说法正确的是
| A.以X浓度变化表示的反应速率为0.001 mol/(L·s) |
| B.将容器体积变为20 L,Z的平衡浓度变为原来的 |
| C.其他条件不变时,若增大压强,则物质Y的转化率减小 |
| D.其他条件不变时,若升高温度,X的体积分数增大,则该反应的ΔH>0 |
在一定温度下,容积一定的密闭容器中发生反应A(s)+2B(g) C(g)+D(g),当下列物理量不再发生变化时,表明反应已达平衡的是
C(g)+D(g),当下列物理量不再发生变化时,表明反应已达平衡的是
①混合气体的密度②混合气体的压强③B的物质的量浓度④混合气体的总物质的量
| A.①② | B.①③ | C.②③ | D.①④ |
某温度下,将2 mol A和1 mol B放入一密闭容器中,发生反应:A(g)+B(g) 2C(s)+2D(g),5 min后反应达到平衡,测得生成C为0.8 mol,下列相关表述正确的是
2C(s)+2D(g),5 min后反应达到平衡,测得生成C为0.8 mol,下列相关表述正确的是
A.该反应的化学平衡常数表达式是K=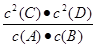 |
| B.该条件下B的平衡转化率是40% |
| C.增大该体系的压强,A的转化率增大 |
| D.若向平衡体系中加入少量生成物C,则正、逆反应速率均增大 |
在一个容积为2L的密闭容器中,加入0.8molA2气体和0.6molB2气体,一定条件下发生如下反应:A2(g)+ B2(g)====2AB(g)ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说明不正确的是 ( )

| A.图中a点的值为0.15 |
| B.该反应的平衡常数K=0.03 |
| C.温度升高,平衡常数K值减小 |
| D.平衡时A2的转化率为62.5% |
可以证明可逆反应N2+3H2 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
①一个N≡N键断裂的同时,有6个N﹣H键断裂
②v(H2)=0.6mol•L﹣1•min﹣1,v(NH3)=0.4mol•L﹣1•min﹣1
③保持其他条件不变时,体系压强不再改变;
④NH3、N2、H2的体积分数都不再改变;
⑤恒温恒容时,混合气体质量保持不变。
| A.②③④ | B.①②④ | C.①③④ | D.③④⑤ |
已知反应2A(g)=2B(g)+C(g)△H<0,达平衡时,要使c(A)增大同时使v(正)增大,应改变的条件为( )
A.减小容器容积 B.增大容器容积 C.减小B的浓度 D.降温
有一处于平衡状态的反应A(g) + 3B(g) 2C(g);△H< 0,为了使平衡向生成C的方向移动,应选择的条件是( )
2C(g);△H< 0,为了使平衡向生成C的方向移动,应选择的条件是( )
| A.高温低压 | B.低温低压 | C.低温高压 | D.高温高压 |
可以证明可逆反应N2+3H2 2NH3已达到平衡状态的是( )
2NH3已达到平衡状态的是( )
①一个N≡N键断裂的同时,有6个N﹣H键断裂
②v(H2)=0.6mol•L﹣1•min﹣1,v(NH3)=0.4mol•L﹣1•min﹣1
③保持其他条件不变时,体系压强不再改变;
④NH3、N2、H2的体积分数都不再改变;
⑤恒温恒容时,混合气体质量保持不变。
| A.②③④ | B.①②④ | C.①③④ | D.③④⑤ |
已知反应2A(g)=2B(g)+C(g)△H<0,达平衡时,要使c(A)增大同时使v(正)增大,应改变的条件为( )
A.减小容器容积 B.增大容器容积 C.减小B的浓度 D.降温
有一处于平衡状态的反应A(g) + 3B(g) 2C(g);△H< 0,为了使平衡向生成C的方向移动,应选择的条件是( )
2C(g);△H< 0,为了使平衡向生成C的方向移动,应选择的条件是( )
A 高温低压 B 低温低压 C 低温高压 D 高温高压
试题篮
()