E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:
xM(g) Mx (g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是 ( )
Mx (g),反应物和生成物的物质的量随时间的变化关系如下图。下列说法正确的是 ( )
A.该反应的化学方程式是2HF (HF)2 (HF)2 |
| B.平衡时混合气体的平均摩尔质量是33.3 |
C.t1时刻,保持温度不变,再充入1molM,重新达到平衡时, 将增大 将增大 |
| D.M的沸点比同主族下一周期元素的气态氢化物沸点低 |
反应 X(气)+ Y(气) 2Z(气);△H=Q(Q<0)在一定条件下,反应物Y的转化率与反应时间(t)的关系如下图所示。若使曲线a变为曲线b可采取的措施是
2Z(气);△H=Q(Q<0)在一定条件下,反应物Y的转化率与反应时间(t)的关系如下图所示。若使曲线a变为曲线b可采取的措施是
| A.加催化剂 | B.降低温度 | C.增大压强 | D.增大Y的浓度 |
某温度下,反应 2CH3OH(g)  CH3OCH3(g) + H2O(g)的平衡常数为400。此温度下,在容积一定的密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)的平衡常数为400。此温度下,在容积一定的密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 |
CH3OH |
CH3OCH3 |
H2O |
| 浓度/(mol·L-1) |
0.44 |
0.6 |
0.6 |
下列说法正确的是
A.CH3OH的起始浓度为1.04 mol/L
B.此时逆反应速率大于正反应速率
C.平衡时,CH3OH的浓度为0.04 mol/L
D.平衡时,CH3OH的转化率小于80%
相同温度度,体积均为0.25L的两个恒容容器中发生可逆反应:X2(g)+3Y2(g)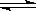 2XY3(g)△H=-92.6kJ·mol-1,实验测得反应在起始、达到平衡时的有关数据如下表所示:
2XY3(g)△H=-92.6kJ·mol-1,实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器编号 |
起始时各物质物质的量/mol |
达平衡时体系能量的变化 |
||
| X2 |
Y2 |
XY3 |
||
| ① |
1 |
3 |
0 |
放热46.3 kJ |
| ② |
0.8 |
2.4 |
0.4 |
Q(Q>O) |
下列叙述不正确的是
| A.容器①、②中反应的平衡常数相等 |
| B.容器①、②中达到平衡时各物质的百分含量相同 |
| C.达平衡时,两个容器中XY3的物质的量浓度均为2 mol·L-1 |
| D.若容器①体积为0.20L.则达平衡时放出的热量大于46.3kJ |
已知:t℃下的某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为: ,有关该平衡的说法中正确的是( )
,有关该平衡的说法中正确的是( )
| A.升高温度,平衡常数K变大 |
| B.增大压强,W(g)物质的量分数变小 |
| C.升温,若混合气体的平均相对分子质量变小,则逆反应放热 |
| D.增大Z浓度,平衡向正反应方向移动 |
25 ℃时,水的电离达到平衡:H2O  H+ + OH- ΔH > 0 ,下列叙述正确的是
H+ + OH- ΔH > 0 ,下列叙述正确的是
| A.向水中加人稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加人少量固体CH3COONa ,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
某恒温密闭容器发生可逆反应Z(?)+W(?) X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是
X(g)+Y(?) ΔH ,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中不正确的是
| A.Z和W在该条件下一定不为气态 |
| B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量可能相等也可能不相等 |
| C.若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度相等 |
| D.若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大 |
在A.B两个大小相同,温度相同的密闭容器中,充入x mol和y mol的SO3(g)(x>y),分别发生分解反应:2SO3(g)  2SO2(g)+O2(g),达到平衡时,其分解率分别为a%和b%,a b关系正确的是( )
2SO2(g)+O2(g),达到平衡时,其分解率分别为a%和b%,a b关系正确的是( )
A.a=b B.a<b C. a>b D.无法比较
把NO2气体装入带活塞的圆筒中慢慢压缩,下列叙述正确的是( )
| A.体积减半,压强为原来二倍 |
| B.体积减半,压强增大,但小于原来的2倍 |
| C.体积减半,N2O4的百分含量增大1倍 |
| D.体积减半,则NO2浓度减小 |
在下列的平衡系中,所用措施,不能使反应向右移动达到新平衡的是( )
A.I-3(aq) I2 + I-(aq)(加入四氯化碳) I2 + I-(aq)(加入四氯化碳) |
B.Ag+(aq)+ Cl-(aq) AgCl(s)(加入固体AgNO3) AgCl(s)(加入固体AgNO3) |
C.Fe(SCN)2+(aq) Fe3+(aq) + SCN-(aq)(加入固体NaSCN) Fe3+(aq) + SCN-(aq)(加入固体NaSCN) |
D.BaSO4(s) Ba2+(aq)+ SO42-(aq)(加入水) Ba2+(aq)+ SO42-(aq)(加入水) |
在容积不变的密闭容器中有反应:X(g) + Y(g)  z(g),若Z(g)的物质的量浓度c(Z)与温度T的关系如图所示(曲线上的任意一点都表示平衡状态)。则下列说法不正确的是
z(g),若Z(g)的物质的量浓度c(Z)与温度T的关系如图所示(曲线上的任意一点都表示平衡状态)。则下列说法不正确的是
| A.A点与B点相比,B点的c (X)大 |
| B.A点与C点的化学反应速率:前者<后者 |
| C.在反应进行到D点时,V正〉V逆 |
| D.该反应的正反应是吸热反应 |
在一定温度下反应2NO2(g ) N2O4 ( g ) 已达到平衡,缩小此密闭容器的容积,则混合气体颜色的变化是
N2O4 ( g ) 已达到平衡,缩小此密闭容器的容积,则混合气体颜色的变化是
| A.变深 | B.变浅 | C.先变深再稍变浅 | D.先变浅再稍变深 |
在其他条件不变的情况下,能使合成氨反应进行程度增大的方法是
| A.升高温度 | B.减小压强 | C.使用催化剂 | D.及时分离出氨气 |
反应CO(g)+H2O(g) 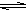 CO2(g)+H2(g) ΔH=-41.2kJ·mol-1,在800℃时的化学平衡常数K=1.0。某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
CO2(g)+H2(g) ΔH=-41.2kJ·mol-1,在800℃时的化学平衡常数K=1.0。某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO |
H2O |
CO2 |
H2 |
| 0.5 mol |
8.5 mol |
2.0 mol |
2.0 mol |
此时反应中正、逆反应速率的关系式是
A.v(正)>v(逆) B.v(正)<v(逆) C.v(正)=v(逆) D.无法判断
定条件下,存在可逆反应X(g)+2Y(g)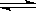 3Z(g),若X、Y、Z起始浓度分别为
3Z(g),若X、Y、Z起始浓度分别为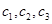 (均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.2mol/L,0.06mol/L,则下列判断不合理的是
(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.2mol/L,0.06mol/L,则下列判断不合理的是
A.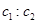 =l:2 =l:2 |
B.达平衡状态时,生成Z的速率是生成X速率的3倍 |
| C.X、Y的转化率不相等 | D.C2的取值范围为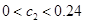 |
试题篮
()