将2mol SO2和2mol SO3气体混合于固定容积的容器内,在一定条件下,发生反应:2SO2 + O2 2SO3,达平衡时SO3为n mol。相同温度下分别按下列配比,平衡后SO3的物质的量大于n mol的是( )
2SO3,达平衡时SO3为n mol。相同温度下分别按下列配比,平衡后SO3的物质的量大于n mol的是( )
| A.2mol SO2和1mol O2 | B.2mol SO2和1mol O2和2mol SO3 |
| C.4mol SO2和1mol O2 | D.3mol SO2和0.5mol O2和1mol SO3 |
某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)  2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则( )
2C(g)达到平衡时,各物质的物质的量之比为n(A)∶n(B)∶n(C)=2∶2∶1。保持温度不变,以2∶2∶1的物质的量之比再充入A、B、C,则( )
A.平衡不移动
B.再达平衡时,n(A)∶n(B)∶n(C)仍为2∶2∶1
C.再达平衡时,C的体积分数增大
D.再达平衡时,正反应速率增大,逆反应速率减小
现有反应:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH=-43kJ/mol,在850℃时,K=1,今在某密闭容器中充入1.0molCO、3.0molH2O、1.0molCO2、xmolH2,下列说法不正确的是( )
CO2(g)+H2(g) ΔH=-43kJ/mol,在850℃时,K=1,今在某密闭容器中充入1.0molCO、3.0molH2O、1.0molCO2、xmolH2,下列说法不正确的是( )
A. ,该反应的平衡常数 ,该反应的平衡常数 |
B. 达到平衡时,通入CO,CO转化率将增大 达到平衡时,通入CO,CO转化率将增大 |
C. 时,若 时,若 ,则起始时平衡向逆反应方向移动 ,则起始时平衡向逆反应方向移动 |
D. 时,若要使上述反应开始时向正反应方向进行,则 时,若要使上述反应开始时向正反应方向进行,则 应满足 应满足 |
下图为某化学反应的速率与时间的关系示意图。在t1 时刻升高温度或增大压强,速率的变化都符合示意图的反应是( )
| A.2SO2(g)+O2(g) ⇌2SO3(g);ΔH<0 |
| B.4NH3(g)+5O2(g) ⇌4NO(g)+6H2O(g);ΔH<0 |
| C.H2(g)+I2(g) ⇌2HI(g); ΔH>0 |
| D.C(s)+H2O(g) ⇌CO(g)+H2(g);ΔH>0 |
反应CO(g)+2H2(g)  2CH3OH(g)在恒容密闭容器中进行。为探究温度、CO2等因素对该反应的影响,进行了4组实验,结果如右下表。下列说法不正确的是
2CH3OH(g)在恒容密闭容器中进行。为探究温度、CO2等因素对该反应的影响,进行了4组实验,结果如右下表。下列说法不正确的是
| 组序号 |
1 |
2 |
3 |
4 |
|
| 反应温度/℃ |
225 |
235 |
225 |
235 |
|
| 反应前气体的物质的量/mol |
CO2 |
0 |
0 |
0.2 |
0.2 |
| CO |
3.0 |
3.0 |
2.8 |
2.8 |
|
| H2 |
7.0 |
7.0 |
7.0 |
7.0 |
|
| 平衡时CH3OH的体积分数/% |
4.9 |
8.8 |
36.5 |
50.7 |
A.该反应的△H>0
B.当容器中压强不变时,反应达到平衡
C.CH3OH含量增大的原因是CO2起了催化作用
D.少量CO2能提高平衡时CH3OH的体积分数
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如右图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如右图所示。下列判断正确的是( )
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D.25℃时,该反应的平衡常数K=2.2 |
可逆反应:2NO2 2NO+O2 在密闭容器中反应,达到平衡状态的标志是( )
2NO+O2 在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2的同时,生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
| A.①④ | B.②③⑤ | C.①③④ | D.①②③④⑤ |
汽车尾气的无害化处理已成为当今汽车工业的一项重要课题,其基本原理是实现2NO(g)+2CO(g) N2(g)+2CO2(g)的反应。关于该反应,下列说法正确的是( )
N2(g)+2CO2(g)的反应。关于该反应,下列说法正确的是( )
| A.只要使用合理的催化剂及载体,就可完全清除NO和CO |
| B.该反应达到平衡时v(NO)正=v(CO)逆 |
| C.假设该反应在密闭容器中进行,一段时间后达到平衡时c(NO)=c(CO) |
| D.使用性能好的催化剂可使反应的平衡常数增大 |
在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
Ni(s)+4CO(g) Ni(CO)4(g),已知该反应平衡常数与温度的关系下表:
Ni(CO)4(g),已知该反应平衡常数与温度的关系下表:
| 温度℃ |
25 |
80 |
230 |
| 平衡常数 |
5×104 |
2 |
1.9×10-5 |
下列说法正确的是
A.上述生成Ni(CO)4(g)的反应为吸热反应
B.25℃时反应Ni(CO)4(g) Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5
C.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时v(正)>v(逆)
D.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2mol/L
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A (g)+xB(g)  2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是( )
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是( )
| A.8min前A的平均反应速率为0.08mol/(L·s) |
| B.30min时扩大容器的体积,40min时升高温度 |
| C.反应方程式中的x=1,正反应为吸热反应 |
| D.30min和54min的反应的平衡常数相等4 |
已知某化学反应的平衡常数表达式为K=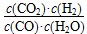 ,在不同的温度下该反应的平衡常数值分别为:
,在不同的温度下该反应的平衡常数值分别为:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
1.67 |
1.11 |
1.00 |
0.60 |
0.38 |
下列有关叙述不正确的是
A.该反应的化学方程式是:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
B.上述反应的正反应是放热反应
C.如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830 ℃,此时测得CO为0.4 mol时,该反应为平衡状态
D.某温度下,如果平衡浓度符合下列关系式: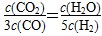 ,判断此时的温度是1000 ℃
,判断此时的温度是1000 ℃
mA(g)+nB(g)  pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
①体系的压强不再改变 ②绝热体系的温度不再改变 ③各组分的浓度不再改变
④各组分的质量分数不再改变 ⑤反应速率vA: vB: vC: vD = m:n:p:q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应
| A.③④⑤⑥ | B.②③④⑥ | C.①③④⑤ | D.①③④⑥ |
工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g) Si(s)+4HCl(g);ΔH=+Q kJ·mol-1(Q>0)
Si(s)+4HCl(g);ΔH=+Q kJ·mol-1(Q>0)
某温度、压强下,将一定量的反应物通入密闭容器进行该反应,下列叙述正确的是
| A.反应过程中,若增大压强因为反应速率增大,所以能提高SiCl4的转化率 |
B.已知,一定温度下,反应的平衡常数(k)为定值,若向已经达到平衡状态的容器中再次加入四种物质,若 >k,平衡就要向正反应方向移动 >k,平衡就要向正反应方向移动 |
| C.反应至4 min时,若HCl的浓度为0.12 mol·L-1,则H2的反应速率为0.03 mol/(L·min) |
| D.当反应吸收热量为0.025Q kJ时,生成的HCl可被100 mL 1 mol·L-1的NaOH溶液恰好完全吸收 |
试题篮
()