向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g) SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量高于生成物的总能量 |
| D.△t1=△t2时,SO2的转化率:a~b段大于b~c段 |
相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g) + 3H2(g)  2NH3(g) ΔH="-92.4" kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g) ΔH="-92.4" kJ/mol。实验测得起始、平衡时的有关数据如下表:
| 容器编号 |
起始时各物质的物质的量/mol |
平衡时反应中的能量变化 |
||
| N2 |
H2 |
NH3 |
||
| ① |
1 |
3 |
0 |
放出热量 a kJ |
| ② |
2 |
3 |
0 |
放出热量 bkJ |
| ③ |
2 |
6 |
0 |
放出热量 ckJ |
下列叙述正确的是
A.放出热量关系:a<b<92.4 B.三个容器内反应的平衡常数:③>①>②
C.达平衡时氨气的体积分数:①>③ D.N2的平衡转化率:②>①>③
铁的氧化物可用于脱除煤气中的H2S,有关反应原理如下:
①Fe3O4(s)+3H2S(g)+H2(g)⇌3FeS(s)+4H2O(g)
②Fe2O3(s)+2H2S(g)+H2(g)⇌2FeS(s)+3H2O(g)
③FeO(s)+H2S(g)⇌FeS(s)+H2O(g)
温度与上述各反应的平衡常数的关系如图所示。下列有关说法正确的是
| A.反应①、②、③中铁的氧化物都是氧化剂 |
| B.反应①、②、③的正反应都是放热反应 |
| C.反应①、②、③中,温度越高H2S的的脱除率越高 |
| D.反应①、②、③中,压强越大H2S脱除率越高 |
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g) △H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
2SO3(g) △H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是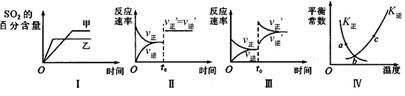
| A.图I表示温度对化学平衡的影响,且甲的温度较高 |
| B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响 |
| C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |
| D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |
下列对化学平衡移动的分析中,不正确的是
①已达平衡的反应C(s)+H2O(g)⇌CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g)⇌2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积减小的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动.
| A.①④ | B.①②③ | C.②③④ | D.①②③④ |
在一定的温度下, 向一密闭容器中放入 1 mol A 和 1 mol B, 发生下列反应:A(g) + B(g)  C(g) + 2D(g),达到平衡状态时,C的含量为 m%,保持温度和体积不变,若按照下列配比在上述容器放入起始物质,达到平衡状态时C的含量仍然为m%的是
C(g) + 2D(g),达到平衡状态时,C的含量为 m%,保持温度和体积不变,若按照下列配比在上述容器放入起始物质,达到平衡状态时C的含量仍然为m%的是
| A.2mol A + 1mol B |
| B.1mol C + 1mol D |
| C.2mol C + 2mol D |
| D.0.5mol A +0.5mol B +0.5mol C +1mol D |
化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是( )
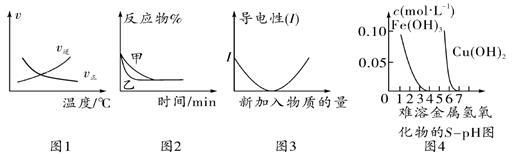
A.根据图1可判断可逆反应“A2(g)+3B2(g) 2AB3(g)”的 ΔH<0 2AB3(g)”的 ΔH<0 |
B.图2可能表示压强对可逆反应 A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| C.图3可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D.根据图4,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu至pH在4左右 |
已知反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达到平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )

| A.由图甲知,A点SO2的平衡浓度为0.4 mol·L-1 |
| B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2 |
| C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
| D.压强为0.50 MPa时,不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
在一个容积为6L的密闭容器中,放入3LX(g)和2LY(g),在一定条件下发生反应:4X(g)+nY(g) 2Q(g)+6R(g)达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小1/3,则该反应中的n值是
2Q(g)+6R(g)达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小1/3,则该反应中的n值是
| A.3 | B.4 | C.5 | D.6 |
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 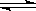 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是:
| A.b>f |
| B.平衡常数K(1000℃)<K(810℃) |
| C.915℃、2.0MPa该反应的平衡常数为Kp=4.5MPa |
| D.1000℃、3.0MPa时E的转化率为83% |
经一定时间后,可逆反应aA+bB cC中物质的含量A%和C%随温度的变化曲线如下图所示,下列说法正确的是
cC中物质的含量A%和C%随温度的变化曲线如下图所示,下列说法正确的是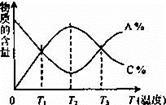
| A.该反应在T1、T3温度时达到化学平衡 |
| B.升高温度,平衡会向正反应方向移动 |
| C.该反应的逆反应是放热反应 |
| D.该反应在T2温度时达到化学平衡 |
向甲、乙两个容积均为1L的恒容容器中分别充入2molA、2molB和1molA、1molB。相同条件下发生如下反应:A(g)+B(g)  xC(g) △H<0。测得两容器中c(A)随时间t的变化如图所示。下列说法错误的是( )
xC(g) △H<0。测得两容器中c(A)随时间t的变化如图所示。下列说法错误的是( )

A.x可能等于2也可能等于3
B.若向平衡后的乙容器充入C,则再次达到平衡时A的体积分数减小
C.若升高甲容器的温度,可使甲容器中各物质的体积分数与乙容器相同
D.若其它条件不变,使乙容器体积变为2L,则平衡时乙容器中:0.25mol/L<c(A)<0.5mol/L
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s) NH3(g)+HI(g) ②2HI(g)
NH3(g)+HI(g) ②2HI(g) H2(g)+I2(g)。达到平衡时,c(H2)="1" mol·L-1,c(HI)="4" mol·L-1,则此温度下反应①的平衡常数为( )
H2(g)+I2(g)。达到平衡时,c(H2)="1" mol·L-1,c(HI)="4" mol·L-1,则此温度下反应①的平衡常数为( )
| A.22 | B.24 | C.20 | D.25 |
试题篮
()