(11分)恒温、恒压的条件下,将N2和H2按体积比1:3混合充入一密闭容器中,发生下列反应 N2 + 3 H2 2NH3,达平衡时,测得气体体积为起始气体体积的0.75倍,求:(1)平衡时N2的转化率;
2NH3,达平衡时,测得气体体积为起始气体体积的0.75倍,求:(1)平衡时N2的转化率;
(2)平衡时混合气体中NH3的体积分数;
(3)平衡时混合气体的相对分子质量与起始气体的相对分子质量之比.
(请写出计算过程)
在一体积固定的密闭容器中加入反应物A、B,发生反应:A(g)+2B(g)=3C(g)。反应2 min后,A的浓度从开始时的1.0 mol·L-1降到0.8 mol·L-1。已知反应开始时B的浓度是1.2 mol·L-1。求:(1)2 min末B、C的浓度。(2)以单位时间内A的浓度的减小来表示2 min内该反应的平均速率。
将N2和H2按一定比例混合,其密度是相同状况下H2的3.6倍,取出0.5 mol该混合气体充入密闭容器里,使之发生反应并在一定条件下达到平衡,已知反应达平衡后容器内压强是相同条件下反应前的0.76倍,试求:
(1)反应前混合气体中N2和H2的体积比。
(2)达平衡时混合气体中氨的物质的量。
(3)平衡时N2的转化率。
在一密闭的2L容器里装有4 mol SO2和2 mol O2,在一定条件下开始反应生成SO3。2 min末测得容器中有3.6 mol SO2,试计算:
(1)2 min末SO3的浓度
(2)2 min内SO2的平均反应速率
(3)O2的转化率
某状态下将1molO2、2molSO2和1molSO3的混合气体压入装有V2O5的密闭容器中平衡时测得混合气体对H2的相对密度为28.5。
求:①反应前混合气体的平均分子量;
②平衡混合气体的平均分子量;
③根据上述计算结果,写出原混合气发生反应的化学方程式;
④求反应的转化率。
“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
| CO |
H2O |
H2 |
CO |
|||
| 1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
| 2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
| 3 |
900 |
a |
b |
c |
d |
t |
① 实验1条件下平衡常数K= (保留小数点后二位数字)。
② 实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值 (填具体值或取值范围)。
③ 实验4,若900℃时,在此容器中加入10molCO、5molH2O、2molCO2、5molH2,则此时v(正) v(逆)(填“<”、“>”、“=”)。
(2)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10—9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10—4mo1/L,则生成沉淀所需CaCl2溶液的最小浓度为 。
(3)已知BaSO4(s) + 4C(s) ="4CO(g)" + BaS(s) △H1 =+571.2kJ/mol,
BaSO4(s) + 2C(s) = 2CO2(g) + BaS(s) △H2="+226.2" kJ/mol。
则反应C(s) + CO2(g) = 2CO(g)的△H3= kJ/mol。 (4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为: 和 。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为 。(Li的相对原子质量约为7.0)
(4)寻找新能源是解决温室效应的一条重要思路。磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池,总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,则该电池放电时的正极和负极反应式分别为: 和 。若用该电池电解蒸馏水(电解池电极均为惰性电极),当电解池两极共有3360mL气体(标准状况)产生时,该电池消耗锂的质量为 。(Li的相对原子质量约为7.0)
在3升的密闭容器中,充入6molX(g)和4molY(g),在一定条件下发生应:
4X(g)+3Y(g)  2Q(g)+nR(g), 2min内达平衡,此时容器内温度不变,混合气体的压强比原来增加了5%,X的浓度减小了1/3。
2Q(g)+nR(g), 2min内达平衡,此时容器内温度不变,混合气体的压强比原来增加了5%,X的浓度减小了1/3。
(1)试求n值 (2)2min内Y的反应速率
某温度下,将H2 和I2 各0.10mol的气态混合物充入10L的 密闭容器中,充分反应,经2分钟达到平衡,测得c(H2)=0.0080 mol•L-1。
密闭容器中,充分反应,经2分钟达到平衡,测得c(H2)=0.0080 mol•L-1。
(1)求:①H2转化为HI的转化率;②该反应的平衡常数。
(2)在上述温度下,该容器中若通入H2 和I2蒸气各0.20mol,试求达到化学平衡状态时各物质的浓度。
(9分)在某温度下,将H2和I2各0.1 mol的气态混合物充入2 L的密闭容器中,充分反应,达到平衡后,测得C(HI)=0.02mol/L。
(1)求该反应的平衡常数;
(2)在上述温度下,陔容器中若通入H2和I2各4.0 mol的气态混合物,求达到化学平衡状态时各物质的浓度。
在密闭容器中,将2.0 mol CO与10mol H2O混合加热到800℃,达到下列平衡:CO(g)+H2O(g) 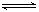 CO2(g)+H2(g) K=1.0,则CO的转化率为________
CO2(g)+H2(g) K=1.0,则CO的转化率为________
在800℃,若上述反应体系中各物质的浓度分别为c(CO)=2.0mol•L-1,c(H2O)=6.0mol•L-1,c(CO2)=3.0mol•L-1,c(H2)= 4.5mol•L-1,则此时该反应向_________ 方向移动。
在一固定容积的密闭容器中,a mol/LN2和b mol/L H2反应,一定条件下经过2min达到平衡,生成c mol/L NH3.
求:(1)用H2表示的速率是多少?(2)N2的转化率是多少?
把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应:3A(g)+B(g) 2C(g)+xD(g),经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算
2C(g)+xD(g),经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算
(1)x (2) B的转化率
(3) 平衡时A的浓度 (4) 恒温达平衡时容器内的压强与开始时压强比
在一定温度下,将0.2mol的碘化氢充入1L的密闭容器中,充分反应,达到平衡后,测得c(H2)=0.08mol/L.
(1)求该反应的平衡常数。
(2)在上述温度下,该容器中若充入碘化氢0.4mol,求达到 平衡时碘化氢的转化率和氢气的物质的量浓度。2HI(g)  H2(g) + I2(g)
H2(g) + I2(g)
在一定温度下,将2mol A和2molB 两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g)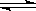 xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,试求:
xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8mol D,并测得C的浓度为0.4 mol·L-1,试求:
(1)x值
(2)B的平衡浓度
(3)A的转化率
(4)用A表示的化学反应速率
在1.0密闭容器中放入0.10molA(g)
,在一定温度进行如下反应应:

反应时间()与容器内气体总压强(
)的数据见下表:
| 时间 |
0 |
1 |
2 |
4 |
8 |
16 |
20 |
25 |
30 |
| 总压强 |
4.91 |
5.58 |
6.32 |
7.31 |
8.54 |
9.50 |
9.52 |
9.53 |
9.53 |
回答下列问题:
(1)欲提高的平衡转化率,应采取的措施为。
(2)由总压强和起始压强
计算反应物
的转化率
的表达式为。
平衡时的转化率为,列式并计算反应的平衡常数
。
(3)①由总压强和起始压强
表示反应体系的总物质的量
总和反应物
的物质的量
,
总=
,
=
。
②下表为反应物浓度与反应时间的数据,计算
=
| 反应时间 |
0 |
4 |
8 |
16 |
| 0.10 |
a |
0.026 |
0.0065 |
分析该反应中反应反应物的浓度变化与时间间隔(
)的规律,得出的结论是,
由此规律推出反应在12时反应物的浓度
为
。
试题篮
()