已知部分化合物的溶度积常数见下表:
| 化学式 |
Ksp |
化学式 |
Ksp |
| AgBr |
5.0×10-13 |
Ag2CO3 |
8.1×10-12 |
| Ag3PO4 |
1.4×10-16 |
CaCO3 |
2.8×10-9 |
| AgOH |
2.0×10-8 |
Ca3(PO4)2 |
2.0×10-29 |
现有某种KNO3溶液,其中混有少量KBr和Ca(H2PO4)2杂质,可供选择的试剂有:①AgNO3,②K2CO3,③KOH,④HNO3。若规定不得重复使用试剂,且最后溶液中只允许含有K+、NO3-和少量H+、OH-,则加入试剂顺序正确的是
| A.③①②④ | B.①③②④ | C.②①③④ | D.①②③④ |
已知25℃时,AgⅠ饱和溶液中c(Ag+)为1.22×10-8mol·L-1,AgCl的饱和溶液中c(Ag+)为1.30×10-5 mol·L-1。若在5mL含有KCl和KI浓度均为0.01 mol·L-1的混合溶液中,滴加8 mL 0.01 mol·L-1的AgNO3溶液,则下列叙述中不正确的是
| A.反应后溶液中离子浓度大小关系为:c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| B.溶液中先产生的是AgI沉淀 |
| C.AgCl的KSP的数值为1.69×10-10 |
| D.若在AgCl悬浊液中滴加KI溶液,白色沉淀会转变成黄色沉淀 |
已知25℃时,AgI饱和溶液中c(Ag+)为1.23×10-8 mol·L-1,AgCl的饱和溶液中c(Ag+)为1.25×10-5 mol·L-1。若在5mL含有KCl和KI各为0.01 mol·L-1的溶液中,加入8mL
0.01 mol·L-1AgNO3溶液,下列叙述正确是( )
| A.混合溶液中c (K+)>c (NO3-) >c (Ag+) >c (Cl-)>c (I-) |
| B.混合溶液中c (K+)>c (NO3-) >c (Cl-) >c (Ag+)>c (I-) |
| C.加入AgNO3溶液时首先生成AgCl沉淀 |
D.混合溶液中 约为1.02×103 约为1.02×103 |
已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是( )
| A.所得溶液中的c(H+)=1.0×10-13 mol·L-1 |
| B.所得溶液中由水电离产生的c(OH-)=1.0×10-13 mol·L-1 |
| C.所加的烧碱溶液pH=13.0 |
| D.所得溶液中的c(Mg2+)=5.6×10-10 mol·L-1 |
在一混合溶液中含有KCl、KBr、K2CrO4,其浓度均为0.01 mol·L-1,向溶液中逐滴加入0.01 mol·L-1AgNO3溶液时,最先和最后沉淀的物质是( )
(AgCl、 AgBr、 Ag2CrO4的Ksp分别为1.77×10-10、5.35×10-13、1.12×10-12)
| A.AgBr、AgCl | B.Ag2CrO4、AgCl |
| C.AgBr、Ag2CrO4 | D.同时沉淀 |
已知:,
,
,则下列难溶盐的饱和溶液中,
浓度大小顺序正确的是()
| A. |
|
B. |
|
| C. |
|
D. |
|
向盛有0.1mol/LAgNO3溶液的试管中滴加0.1mol/LNa2S溶液至沉淀完全,再向上层清液中滴加足量NaCl溶液,产生的现象或生成的物质是( )
| A.黑色沉淀完全转化为白色沉淀 | B.既有氯化银也有硫化银 |
| C.不能由黑色沉淀转化为白色沉淀 | D.只有氯化银白色沉淀 |
某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是:
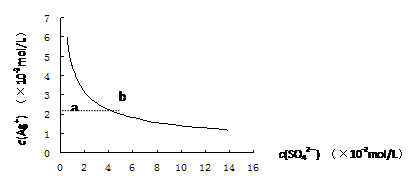 |
| A.含有大量SO42-的溶液中肯定不存在Ag+ |
| B.Ag2SO4的溶度积常数(Ksp)为1×10-4 |
| C.0.02mol/L的AgNO3溶液与0.2mol/L的Na2SO4溶液等体积混合不会生成沉淀 |
| D.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
已知同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出S2-的能力而言,FeS>H2S>CuS,则下列离子方程式错误的是 ( )
A.Mg2++ +2Ca2++4OH- +2Ca2++4OH- Mg(OH)2↓+2CaCO3↓+2H2O Mg(OH)2↓+2CaCO3↓+2H2O |
B.Cu2++H2S CuS↓+2H+ CuS↓+2H+ |
C.Zn2++S2-+2H2O Zn(OH)2↓+H2S↑ Zn(OH)2↓+H2S↑ |
D.FeS+2H+ Fe2++H2 S↑ Fe2++H2 S↑ |
温室下取0.2mol/L的盐酸与0.2mol/LMOH等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答下列问题
(1)混合溶液中由水电离出的c(H+)_______0.2mol/L盐酸中水电离出的c(H+)(填“<”、“>”、“=”)。
(2)求出混合溶液中下列算式的精确计算结果(填具体数字,忽略混合后溶液体积的变化),c(Cl—)-c(M+)=_____________mol/L,c(H+)-c(MOH)="_______________" mol/L
(3)室温下如果取0.2mol/LMOH溶液与0.1mol/L盐酸等体积混合,测得混合溶液的pH<7,则说明MOH的电离程度________MCl的水解程度(填“<”、“>”、“=”),溶液中各离子浓度由大到小的顺序为_____________________________
某无色透明溶液只可能含有下列离子中的若干种:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、AlO2-、Cl-、CO32-等,取该溶液进行如下实验:
①用红色石蕊试纸检测该溶液,试纸显蓝色;
②取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇到空气立即变为红
棕色;
③取溶液少许,滴加盐酸的过程中有白色沉淀出现过
④取溶液少许,滴入氯化钡溶液产生白色沉淀,该沉淀能部分溶解在足量的稀盐酸中
⑤取实验④后的澄清溶液,滴入AgNO3溶液产生白色沉淀,再加入过量的稀硝酸,
沉淀不消失。
请回答下列问题:
(1)在实验①中,下图所示的操作中正确的是___________(填代号)
(2)原溶液中肯定存在的离子是_______________,可能存在的离子是_________,在可能存在的离子中,只要对前述某一实验步骤中的试剂进行改进,改进的方法是____
_ 。
(3)用离子方程式表示:①中溶液能导致试纸变蓝色的原因_____________________;②产生沉淀的原理_____________________________
水体中重金属铅的污染问题备受关注。水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、 、
、 ,各形态的浓度分数α随溶液pH变化的关系如下图所示:
,各形态的浓度分数α随溶液pH变化的关系如下图所示:
1表示Pb2+,2表示Pb(OH)+,3表示Pb(OH)2,4表示 ,5表示
,5表示
(1)Pb(NO3)2溶液中 ___________2(填“>”“=”或“<”);往该溶液中滴入氯化铵溶液后,
___________2(填“>”“=”或“<”);往该溶液中滴入氯化铵溶液后,  增大,可能的原因是_____________。
增大,可能的原因是_____________。
(2)往Pb(NO3)2溶液中滴入稀NaOH溶液,pH=8时溶液中存在的阳离子(Na+除外)有___________,pH=9时主要反应的离子方程式为______________。
难溶化合物的饱和溶液存在溶解平衡,例如:AgCl(s) Ag++Cl-,Ag2CrO4(s)
Ag++Cl-,Ag2CrO4(s) 2Ag++
2Ag++ 。在一定温度下,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c(
。在一定温度下,已知:Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=[c(Ag+)]2·c( )=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算回答:
)=1.9×10-12,现用0.01 mol·L-1 AgNO3溶液滴定0.01 mol·L-1 KCl和0.001 mol·L-1 K2CrO4混合溶液,通过计算回答:
(1)Cl-、 谁先沉淀?
谁先沉淀?
(2)当刚出现Ag2CrO4沉淀时,溶液中Cl-的物质的量浓度是多少?(设混合溶液在反应中体积不变)
试题篮
()