已知298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得PH=13.0,则下列说法不正确的是
| A.所得溶液中的c(H+)=1.0×10-13mol·L-1 |
| B.加入Na2CO3固体,可能生成沉淀 |
| C.所加的烧碱溶液pH=13.0 |
| D.所得溶液中的c(Mg2+)=5.6×10-10mol·L-1 |
在一定温度下,硫酸铜晶体的培养皿中存在下列平衡: Cu2++SO42-+x H2O  CuSO4·xH2O,当向硫酸铜溶液(析有硫酸铜晶体)中加少量无水硫酸铜粉末后,下列说法中正确的是( )
CuSO4·xH2O,当向硫酸铜溶液(析有硫酸铜晶体)中加少量无水硫酸铜粉末后,下列说法中正确的是( )
| A.溶液中Cu2+浓度增大 | B.溶液中Cu2+数目不变 |
| C.硫酸铜晶体体积增大 | D.溶液的蓝色变浅 |
已知Ca(OH)2的溶解度随温度升高而降低。将某温度下饱和澄清石灰水①加入少量生石灰后恢复到原来温度;②降低温度。这两种情况下,前后均保持不变的是
| A.溶液的质量 | B.Ca(OH)2的溶解度 |
| C.溶液中Ca2+离子的数目 | D.溶液中溶质的质量分数 |
氢氧化镁固体在水中溶解,有下列平衡:Mg(OH)2(s)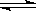 Mg2++ 2OH―,加入下列哪种固体物质可使Mg(OH)2固体的质量减少
Mg2++ 2OH―,加入下列哪种固体物质可使Mg(OH)2固体的质量减少
| A.Na2CO3 | B.MgCl2 | C.NH4Cl | D.NaCl |
下列说法中不正确的是( )
| A.Ksp只与难溶电解质本身的性质和温度有关 |
| B.在一定温度下的AgCl饱和溶液中,C(Ag+)和C(Cl-)的乘积是一个常数 |
| C.在一定温度下,向AgCl饱和溶液中加入盐酸时,Ksp值变大 |
| D.由于Ksp(FeS)>Ksp(CuS),所以FeS沉淀在一定条件下可以转化为CuS沉淀 |
将足量AgCl分别放入:①5ml水②10ml0.2 mol·L-1MgCl2溶液③20ml0.5 mol·L-1NaCl溶液④40ml0.1 mol·L-1盐酸中溶解至溶液饱和,各溶液Ag+的浓度分别为a、b、c、d,它们由大到小的排列顺序是
| A.a>b>c>d | B.d>b>c>a | C.a>d>b>c | D.c>b>d>a |
已知相同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2,就溶解或电离出S2-的能力而言:FeS>H2S>CuS,则下列离子方程式错误的是
A.Zn2++S2-+2H2O=Zn(O H)2↓+H2S↑ H)2↓+H2S↑ |
B.Mg2++2HCO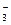 +2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O +2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O |
| C.FeS+2H+=Fe2++H2S↑ |
| D.Cu2++H2S=CuS↓+2H+ |
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1) CuSO4 +Na2CO3 主要: Cu2+ + CO32─ + H2O = Cu(OH)2↓ + CO2↑
次要:Cu2+ + CO32─= CuCO3↓(几乎不发生反应。下同)
(2) CuSO4 +Na2S 主要: Cu2+ + S2─ =" " CuS↓
次要: Cu2+ + S2─ + 2H2O = Cu(OH)2↓ + H2S↑
则下列几种物质的溶解度大小的比较中,正确的是( )
| A.CuS <Cu(OH)2<CuCO3 | B.CuS >Cu(OH)2>CuCO3 |
| C.Cu(OH)2>CuCO3>CuS | D.Cu(OH)2<CuCO3<CuS |
已知下列反应:①NH3+H+=NH4+ ②Ag++2NH3=Ag(NH3)2+ ③Ag++Cl-=AgCl
前者都比后者更容易发生。下列事实或现象预期错误的是
| A.氯化银可溶于氨水 | B.银氨溶液中加入氯化钠溶液有白色沉淀 |
| C.银氨溶液中加入盐酸有白色沉淀 | D.银镜反应的残留液可用稀硝酸处理 |
下表是五种银盐的溶度积常数(25℃)
| 化学式 |
AgCl |
Ag2SO4 |
Ag2S |
AgBr |
AgI |
| 溶度积 |
1.8×10—10 |
1.4×10—5 |
6.3×10—50 |
7.7×10—13 |
8.51×10—16 |
下列说法错误的是
| A.五种物质在常温下溶解度最大的是Ag2SO4 |
| B.将氯化银溶解于水后,向其中加入Na2S,则可以生成黑色沉淀 |
| C.氯化银、溴化银和碘化银三种物质在常温下的溶解度按氯、溴、碘的顺序减小 |
| D.向100mL0.1mol·L—1的Na2SO4溶液中加入1 mL0.1mol·L—1的AgNO3溶液,有白色沉淀生成 |
下列表述中,不正确的是
| A.用稀盐酸洗涤AgCl沉淀比用水洗涤,损耗AgCl少 |
| B.等体积的 pH均等于3的盐酸和AlCl3溶液中,已电离的水分子数前者一定小于后者 |
| C.高效催化剂可使水分解,同时释放能量 |
| D.明矾用于净水和氯气用于自来水的杀菌消毒,两个反应遵循的化学原理不同 |
已知常温下: 。则下列叙述正确的是 ( )
。则下列叙述正确的是 ( )
| A.AgCl在饱和NaCl溶液中的KSP比在纯水中的KSP小 |
B.向AgCl的悬浊液中加入NaBr溶液,白色沉淀转化为淡黄色,说明 |
| C.将0.001mol·AgNO3溶液滴入0.001mol·L-1KCl和0.001mol·L-1K2CrO4混合溶液中,产生Ag2CrO4 |
| D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动 |
向5mL 0.2 mol/L的盐酸中加入5mL0.18 mol/L AgNO3溶液生成沉淀,则生成沉淀后溶液中Ag+的物质的量浓度为(已知 Ksp(AgCl)=1.8×10-10)
| A.1.8×10-6mol/L | B.1.8×10-7mol/L | C.1.8×10-8mol/L | D.不存在 |
25℃时,向AgCl的白色悬浊液中依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最后生成黑色沉淀。已知有关物质的颜色和溶度积如下表:
| 物质 |
AgCl |
AgI |
Ag2S |
| 颜色 |
白 |
黄 |
黑 |
| Ksp(25℃) |
1.8×10-10 |
1.5×10-16 |
1.8×10-50 |
下列叙述中不正确的是
| A.溶度积小的沉淀可以转化为溶度积更小的沉淀 |
| B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生 |
| C.25℃时,AgC1固体在等体积、等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同 |
| D.25℃时,AgC1固体在等体积、等物质的量浓度的NaCl、CaCl2溶液中的c(Ag+)相同 |
试题篮
()