在以稀硫酸为电解质溶液的铜——锌原电池中,已知其电极反应分别为
锌片:Zn-2e-= Zn2+;铜片:2H+ +2e-= H2↑。下列判断正确的是
| A.溶液的酸性逐渐增强 |
| B.铜片逐渐溶解 |
| C.溶液中H+向锌片作定向移动 |
| D.锌片是负极并被氧化 |
根据下式所示的氧化还原反应设计一个原电池: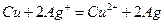
(1)装置可采用烧杯和盐桥,画出此原电池的装置简图。
①注明原电池的正极和负极;
②注明外电路中电子的流向。
(2)写出两个电极上的电极反应。
如图所示,杠杆A、B两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,小心地向水槽中滴入CuSO4浓溶液 。(该过程中不考虑两球浮力的变化)下列说法正确的是 ( )
。(该过程中不考虑两球浮力的变化)下列说法正确的是 ( )
A.若杠杆由绝缘体材料制成,一段时间后,
杠杆一定B端高A端低
B.若杠杆由导体材料制成,一段时间后,
杠杆一定B端高A端低
C.若杠杆由导体材料制成,一段时间后,
杠杆一定A端高B端低
D.杠杆一定A端高B端低,与其材质无关
根据反应为 2Cu+O2+CO2+H2O=Cu2(OH)2CO3,
设计如下图所示原电池,下列说法错误的是 
| A.X可以是银或石墨 |
| B.电子从铜电极经外电路流向X电极 |
| C.Y是硫酸铜溶液 |
| D.X极上的电极反应式为 O2+2H2O+4e- = 4OH- |
在理论上不能用于设计原电池的化学反应是
| A.NaCl(aq)+ AgNO3(aq)= AgCl(s)+ NaNO3(aq )△H<0 |
| B.2CH3OH (l) +3O2(g) = 2CO2(g) + 4H2O (l)△H<0 |
| C.2FeCl3(aq)+Fe(s) = 3FeCl3(aq) △H < 0 |
| D.2H2 (g) + O2 (g) = 2H2O (l) △H < 0 |
(1)下列装置属于原电池的是 ; 
Zn Zn Cu Zn Cu Cu Cu Fe Cu
稀硫酸 稀硫酸 酒精 稀硫酸 稀硫酸
① ② ③ ④ ⑤
(2)在选出的原电池中,______ 是负极,发生______ 反应 ,______ 是正极 ,该极的现象___________________________;
(3)此原电池反应的化学方程式为___________________________。
将铜片和铝片用导线连接后插入盛有浓硝酸的烧杯中组成原电池,此原电池的负极及其电极反应分别是
| A.Al, Al- 3e-=Al3+ | B.Cu, Cu-2e-=Cu2+ |
| C.Al, 2H++2e-=H2↑ | D.Cu, 2H++NO3-+e-=NO2↑+H2O |
有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与C构成原电池时,电极反应式为:
C 2—+2e—→C,B—2e—→B2+则A、B、C、D金属性由强到弱的顺序为( )
A.A>B>C>D B.A>B>D>C C.D>A>B>C D.D>C>A>B
在如图所示的装置中,a的金属活泼性在氢前,b为碳棒,关于此装置的各种叙述不正确的是( )
| A.a是正极,b是负极 |
| B.碳棒上有气体放出 |
| C.a极上发生了氧化反应 |
| D.溶液中H+从a极移动到b极 |
2008年10月8日,瑞典皇家科学院宣布美籍华裔科学家钱永健获得2008年度诺贝尔化学奖.少年时代,他就对化学产生了浓厚的兴趣.16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获具有“少年诺贝尔奖”之称的著名奖项.下列说法正确的是( )
| A.金属腐蚀就是金属失去电子被还原的过程 |
| B.将水库中的水闸(钢板)与外加直接电源的负极相连,正极连接到一块废铁上可防止水闸被腐蚀 |
| C.由原电池原理知所有的合金都比纯金属更易被腐蚀 |
| D.铜板上的铁铆钉处在潮湿的空气中发生:Fe→Fe3++3e-,从而形成铁锈,但此过程铜不被腐蚀 |
纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液。放电时两个电极反应分别为:Zn+2OH-→Zn(OH)2+2e- Ag2O+H2O+2e-→2Ag+2OH- 下列说法中正确的是( )
| A.锌是正极,氧化银是负极 | B.锌发生还原反应,氧化银发生氧化反应。 |
| C.溶液中OH-向正极移动,K+、H+向负极移动。 | |
| D.在电池放电的过程中,电解质溶液的酸碱性基本保持不变。 |
如右图所示,A、B、C三个装置中的三个烧杯分别盛有足量的CuCl2溶液。 
A(左Zn右Cu) B(左C右Pt) C(左Zn右Cu)
(1)、A、B、C三个装置中属于原电池的是_____ (填标号,下同),属于电解池的是___ _________。
(2)、A池中Zn是_______极,发生_______反应(填“氧化”或“还原”,下同),电极反应式为_________; Cu是_____极, 发生_____反应, 电极反应式为 ,A中总反应的化学方程式为 。
(3)、B池中C是_____极,发生_____反应,电极反应为 ;Pt是_____极,发生______反应,电极反应为 。B池中总反应的化学方程式为 ________________。
(4) C池中Zn是_____极,发生______反应,电极反应为_______________;Cu是 极, 发生 反应, 电极反应为 反应过程中,溶液浓度________(填“变大”“变小”或“不变”)。
试题篮
()