在理论上可设计成原电池的化学反应是( )
| A.C(s)+H2O(g)===CO(g)+H2(g) ΔH>0 |
| B.Ba(OH)2·8H2O(s)+2NH4Cl(s)===BaCl2(aq)+2NH3·H2O(l)+8H2O(l) ΔH>0 |
| C.CaC2(s)+2H2O(l)―→Ca(OH)2(s)+C2H2(g) ΔH<0 |
| D.CH4(g)+2O2(g)―→CO2(g)+H2O(l) ΔH<0 |
原电池的总反应的离子方程式是Zn+Cu2+=Zn2++Cu,该反应的原电池组成正确的是
| |
A |
B |
C |
D |
| 正极 |
Zn |
Ag |
Cu |
Cu |
| 负极 |
Cu |
Cu |
Zn |
Zn |
| 电解质溶液 |
CuCl2 |
H2S04 |
CuSO4 |
FeCl2 |
原电池产生电流的本质原因是
| A.原电池中溶液能电离出自由移动的离子 |
| B.有导线将两个活动性不同的电极连接 |
| C.正极发生了氧化反应,而负极发生了还原反应 |
| D.电极上进行的氧化还原反应中会有电子的转移 |
右图为铜锌原电池示意图,下列说法正确的是
| A.电子由铜片通过导线流向锌片 |
| B.烧杯中溶液逐渐呈蓝色 |
| C.锌片逐渐溶解 |
| D.该装置能将电能转变为化学能 |
根据下图,下列判断中正确的是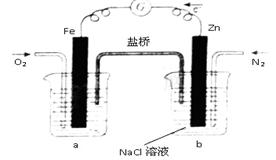
| A.烧杯b中发生还原反应 |
| B.烧杯a中的溶液pH升高 |
| C.烧杯a中发生的反应为2H+ +2e-="==" H2 |
| D.烧杯b中发生的反应为2Cl--2e-="==" Cl2 |
关于原电池说法不正确的是:( ) 
| A.右图所示原电池中,Cu为正极 |
| B.右图所示原电池中,开关闭合时,化学能主要转变为电能;断开时,化学能主要转变为热能 |
| C.在原电池中,负极上发生氧化反应,正极上发生还原反应 |
| D.在原电池中,电子从负极经过电解质溶液流向正极 |
下图是某同学做完Zn—Cu原电池实验后所做的读书卡片记录,其中描述合理的组合是
| A.①②③ | B.②③④ | C.④⑤⑥ | D.③④⑤ |
下列说法中正确的是
| A.在原电池中,物质在负极发生氧化反应 |
| B.在原电池中,电子由正极流向负极 |
| C.在电解池中,物质在阴极发生氧化反应 |
| D.在电解池中,与电源正极相连的电极是阴极 |
如图所示,电流表G发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液。则A、B、C为( )
A. A是Zn,B是Cu,C是稀H2SO4
B. A是Cu,B是Zn,C是稀H2SO4
C. A是Fe,B是Ag,C是稀AgNO3溶液
D. A是Ag,B是Fe,C是稀AgNO3溶液
如图所示,电流表G发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液。则A、B、C为( )
A、 A是Zn,B是Cu,C是稀H2SO4
B、 A是Cu,B是Zn,C是稀H2SO4
C、 A是Fe,B是Ag,C是稀AgNO3溶液
D、 A是Ag,B是Fe,C是稀AgNO3溶液
关于锌、铜和稀H2SO4构成的原电池的下列说法中正确的是
| A.锌溶解的速率比锌直接与同浓度硫酸反应快 |
| B.电子从铜片经导线流向锌片 |
| C.负极的反应式为2H++2e-===H2↑ |
| D.反应一段时间后,溶液的pH降低 |
试题篮
()