如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片。经观察,装置中有如下现象:开始时插在小试管中的导管内的液面下降,一段时间后导管内的液面回升,略高于U型管中的液面。以下有关解释合理的是
| A.生铁片中的碳是原电池的负极,发生还原反应 |
| B.雨水酸性较强,生铁片始终发生析氢腐蚀 |
| C.墨水液面回升时,生铁片发生吸氧腐蚀 |
| D.U型管中溶液pH逐渐减小 |
某原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu,此反应的原电池正确的是( )
| [ |
正极 |
负极 |
电解质溶液 |
| A |
Cu |
Zn |
HCl |
| B |
Zn |
Cu |
CuSO4 |
| C |
Ag |
Zn |
CuSO4 |
| D |
Cu |
Zn |
ZnCl2 |
科研人员设想用如图所示装置生产硫酸,下列说法正确的是( )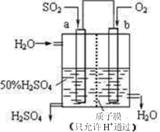
| A.a为正极,b为负极 | B.生产过程中H+向a电极区域运动 |
| C.电子从b极向a极移动 | D.负极反应式为: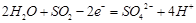 |
下列各组材料中,不能组成原电池的是
| |
A |
B |
C |
D |
| 电极材料 |
Zn片、石墨 |
Cu片、Ag片 |
Cu片、Zn片 |
Fe片、Cu片 |
| 插入的溶液 |
H2SO4溶液 |
AgNO3溶液 |
蔗糖溶液 |
稀盐酸 |
下列说法中正确的是
| A.原电池中的电极一定要由两种不同的金属组成 |
| B.原电池中电子流出的一极是正极,发生氧化反应 |
| C.原电池两极均发生氧化还原反应 |
| D.原电池中阳离子向正极移动 |
将Al片和Cu片用导线相连,一组插入浓盐酸中,一组插入稀氢氧化钠溶液中,分别形成原电池,则在这两原电池中,正极分别为( )
| A.Cu片、Cu片 | B.Cu片、Al片 | C.Al片、Al片 | D.Al片、Cu片 |
下列各组的电极材料和电解液,不能组成原电池的是( )
| A.铜片、石墨棒,稀硫酸 | B.铜片、石墨棒,硝酸银溶液 |
| C.锌片、铜片,稀盐酸 | D.铜片、银片,FeCl3溶液 |
两种金属A与B组成原电池时,A是正极。下列有关推断正确的是( )
| A.A的金属性强于B |
| B.电子不断由A电极经外电路流向B电极 |
| C.A电极上发生的电极发应是还原反应 |
| D.A的金属活动性一定排在氢前面 |
把A、B、C、D四块金属片浸入稀硫酸中,分别用导线两两相连可以组成原电池。A、B相连时A为负极;C、D相连时,电流由D→C;A、C相连时,C极上产生大量气泡,B、D相连时,D极发生氧化反应。这四种金属的活动性顺序是( )
A.A>B>C>D B.A>C>D>B C.C>A>B>D D.B>D>C>A
关于如图所示装置的叙述,正确的是( )。
| A.氢离子在铜片表面被氧化 |
| B.铜片质量逐渐减少 |
| C.电子从锌片经导线流向铜片 |
| D.铜是阳极,铜片上有气泡产生 |
试题篮
()