已知空气—锌电池的电极反应为: 锌片:Zn + 2OH――2e-=" ZnO" + H2O 石墨:1/2O2+H2O + 2e- = 2OH- 据此判断,锌片是:
| A.负极,并被氧化 | B.负极,并被还原 |
| C.正极,并被氧化 | D.正极,并被还原 |
有关原电池的工作原理中的下列说法中不正确的是( )
| A.电池负极发生氧化反应 |
| B.电池正极发生还原反应 |
| C.电子流向是从负极流向正极(外电路) |
| D.电流方向是从负极流向正极(外电路) |
原电池是将化学能转化为电能的装置,但其构成具有一定的条件,这些条件是 ( )。
①电极(负极与正极:金属活动性不同)、②电解质溶液、③闭合回路、④灯泡
| A.①②③④ | B.①②③ |
| C.①②④ | D.②③④ |
某化学兴趣小组将锌片和铜片出入番茄中制成水果电池(如右下图)下列说法中正确的是( )
| A.一段时间后,锌片质量会变小 | B.铜片上发生氧化反应 |
| C.电子由铜片通过导线流向锌 | D.锌电极是该电池的正极 |
原电池电极的“正”与“负”不仅与电极材料的性质有关,也与电解质溶液有关.下列说法中正确的是
| A.由Fe、Cu和FeCl3溶液组成的原电池中,负极反应式为:Cu-2e-===Cu2+ |
| B.由Al、Cu和稀硫酸组成的原电池中,负极反应式为:Cu-2e-===Cu2+ |
| C.由Al、Mg和NaOH溶液组成的原电池,负极反应式为:Al+4OH--3e-===AlO+2H2O |
| D.由Al、Cu和浓HNO3溶液组成的原电池中,负极反应式为:Al-3e-===Al3+ |
右图是某学生设计的一个原电池,若要装置中电流计发生偏转,则M、N两极的组成
材料是 ( )
| A.Zn、Zn | B.Zn、Cu | C.Cu、Cu | D.石墨、石墨 |
将反应2Fe3++2I- 2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是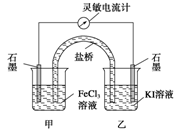
| A.反应开始时,乙中石墨电极上发生氧化反应 |
| B.电流计读数为零时,达到化学平衡状态 |
| C.乙池中若换为Fe电极和FeCl2溶液,则电流计指针向相 反方向偏转 |
| D.电流计读数为零后,在甲中溶入FeCl3固体,乙中石墨电极仍为负极 |
下图是一原电池的装置,关于它的说法正确的是
| A.装置中铜是负极 |
| B.铜表面的反应为:2H++2e-=H2↑ |
| C.电流的方向是从铁经导线流向铜 |
| D.构成原电池后,铁与硫酸铜的反应速率加快 |
铜锌原电池(如图)工作时,下列叙述正确的是
A 正极反应为:Zn—2e-=Zn2+ B电池反应为:Zn+Cu2+=Zn2+ +Cu
C 在外电路中,电流从负极流向正极 D 盐桥中的K+移向ZnSO4溶液
下列叙述中正确的是
| A.构成原电池正极和负极的材料必须是两种金属 |
| B.由Cu、Zn作电极与CuSO4溶液组成的原电池中,Cu是负极 |
| C.马口铁(镀锡铁)破损时与电解质溶液接触,锡先被破坏 |
| D.铜锌原电池工作时,若有13 g锌被溶解,电路中就有0.4 mol电子通过 |
在理论上不能用于设计原电池的化学反应是 ( )
| A.HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l) |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) |
C.2FeCl2+Cl2=2FeCl 3 3 |
| D.3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O |
在理论上不能用于设计原电池的化学反应是
| A.HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l)△H < 0 |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H < 0 |
| C.4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)△H < 0 |
| D.2H2(g)+O2(g)=2H2O(l)△H < 0 |
有A、B、C、D四块金属片,进行如下实验:①将A、B用导线连接后,同时浸入稀硫酸溶液中,B极上有气泡产生;②C、D用导线连接后,同时浸入稀硫酸溶液中,电流由D 导线
导线 C;③A、C相连后,同时浸入稀硫酸溶液中,C极上产生大量气泡;④B、D用导线连接后,同时浸入稀硫酸溶液中,D极上发生氧化反应。据此判断四种金属的活动性顺序为( )
C;③A、C相连后,同时浸入稀硫酸溶液中,C极上产生大量气泡;④B、D用导线连接后,同时浸入稀硫酸溶液中,D极上发生氧化反应。据此判断四种金属的活动性顺序为( )
A. A>B>C>D B. A>C> D>B C. C>A>B>D D. B>D>C>A
D>B C. C>A>B>D D. B>D>C>A
下列叙述正确的是( )
①原电池是把化学能转化成电能的一种装置②原电池正极发生氧化反应,负极发生还原反应③不能自发进行的氧化还原反应,通过原电池的装置均可以实现④碳棒不能用来作原电池的电极⑤反应Cu+2Ag+=2Ag+Cu2+,能以原电池的形式来实现
| A.①⑤ | B.①④⑤ | C.②③④ | D. ②⑤ ②⑤ |
试题篮
()