下列说法不正确的是
| A.原电池负极被氧化 |
| B.任何化学反应都能设计成原电池 |
| C.化学反应的速率和限度均可通过改变化学反应条件而改变 |
| D.化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变 |
“原电池技术是航天科技的核心技术之一”;理论上不能设计为原电池的化学反应是
A.CH4+2O2 CO2+2H2O CO2+2H2O |
B.2H2+O2 2H2O 2H2O |
| C.HNO3+NaOH=NaNO3+ H2O | D.CuSO4+Fe=" Cu" +Fe SO4 |
对下图所示的铜锌原电池说法不正确的是( )
| A.铜片作负极 | B.锌片上发生氧化反应 |
| C.铜片上有气泡产生 | D.导线中有电流通过 |
下列关于原电池的叙述中,正确的是
| A.原电池中,正极就是阳极,负极就是阴极 | B.形成原电池时,在负极上发生氧化反应 |
| C.原电池工作时,溶液中的阳离子向负极移动 | D.电子从负极流向正极 |
在理论上不能用于设计原电池的化学反应是( )
| A.H2SO4+BaCl2==2HCl+BaSO4↓ |
B.2CH3CH2OH+3O2 2CO2+4H2O 2CO2+4H2O |
| C.4Fe(OH)2+2H2O+O2==4Fe(OH)3 |
| D.3Cu+8HNO3==3Cu(NO3)2+2NO↑+4H2O |
银锌电池广泛用作各种电子仪器的电源,其电极分别为Ag2O、Zn,电解质溶液为KOH溶液,总反应为Ag2O+Zn+H2O=2Ag+Zn(OH)2。下列说法中错误的是
| A.工作时,负极上发生反应的物质是Zn |
| B.溶液中OH-向正极移动,K+、H+向负极移动 |
| C.工作时,负极区溶液氢氧根浓度减小 |
| D.正极上发生的反应是Ag2O+H2O+2e-=2Ag+2OH- |
有关下图所示原电池的叙述不正确的是
| A.电子沿导线由Cu片流向Ag片 |
| B.正极的电极反应是Ag++e-=Ag |
| C.Cu片上发生氧化反应,Ag片上发生还原反应 |
| D.盐桥中盛装的是含琼脂的饱和氯化钾溶液,钾离子流向银半电池 |
下列各组材料中,不能组成原电池的是( )
| |
A |
B |
C |
D |
| 两极材料 |
Zn片、石墨 |
Cu片、Ag片 |
Zn片、Cu片 |
Fe片、Cu片 |
| 插入溶液 |
H2SO4溶液 |
AgNO3溶液 |
蔗糖溶液 |
稀盐酸 |
如图为番茄电池,下列说法正确的是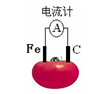
| A.一段时间后,铁极质量会变大 | B.溶液中的H+ 向石墨电极移动 |
| C.电子由石墨电极通过导线流向铁极 | D.铁电极是该电池的正极 |
关于原电池的说法正确的是( )
| A.电流从原电池的负极流向正极 |
| B.电子从发生还原反应的电极流出 |
| C.原电池是将化学能转变为电能的一种装置 |
| D.原电池的两个电极,一定是由活动性不同的两种金属组成 |
把A、B、C、D四块金属浸入稀硫酸中,分别用导线两两相连可以组成原电池。A、B相连时A为负极;C、D相连时,电流由D→C;B、C相连时B极发生氧化反应。这四种金属的活动性顺序是( )
A. A﹥B﹥C﹥D B. A﹥C﹥D﹥B C. C﹥A﹥B﹥D D. B﹥D﹥C﹥A
原电池产生电流的本质原因是( )
| A.原电池中溶液能电离出自由移动的离子 |
| B.有导线将两个活动性不同的电极连接 |
| C.正极发生了氧化反应,而负极发生了还原反应 |
| D.两电极上分别进行的氧化、还原反应中会有电子的转移 |
试题篮
()