科研人员设想用如图所示装置生产硫酸,下列说法正确的是
| A.A为正极,B为负极 |
| B.生产过程中A电极质量减轻 |
| C.电子从B极向A极移动 |
| D.负极反应式为:SO2-2e-+ 2H2O = SO42-+ 4H+ |
等质量的两份锌粉a、b分别加入到两份相同体积相同物质的量浓度且过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,下列各图为产生H2的体积v(L)与时间t(min)的关系,其中正确的是
关于下图所示装置(盐桥含KCl)的叙述,正确的是
| A.铜离子在铜片表面被氧化 |
| B.铜作阳极,铜片上有气泡产生 |
| C.电流从锌片经导线流向铜片 |
| D.右侧烧杯中,SO42-的物质的量几乎不变,K+的数目增多 |
某原电池装置如图所示。下列有关叙述中,正确的是
| A.Fe作正极,发生氧化反应 |
| B.负极反应:Al-3e-+3OH-===Al(OH)3↓ |
| C.工作一段时间后,盛有稀硫酸溶液的杯中pH不变 |
| D.盐桥中的Cl-向左边烧杯中移动,使该烧杯中溶液保持电中性 |
对下列装置的叙述错误的是
| A.X如果是硫酸铜,a和b分别连接直流电源正、负极,一段时间后铁片质量增加 |
| B.X如果是氯化钠,则a和b连接时,该装置可模拟生铁在食盐水中被腐蚀的过程 |
| C.X如果是硫酸铁,则不论a和b是否用导线连接,铁片均发生氧化反应 |
| D.X如果是氢氧化钠,将碳电极改为铝电极,a和b用导线连接,此时构成原电池铁作负极 |
某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是
| A.X和Y与电流表连接,Cu极为正极,发生氧化反应 |
| B.X和Y与电流表连接,盐桥中的阴离子移向CuSO4溶液 |
| C.X和Y分别与电源“—”、“+”极相连,Cu极质量减轻 |
| D.X和Y分别与电源“+”、“—”极相连,Zn极电极反应为4OH——4e-=O2↑+2H2O |
干电池原理示意图如下,电池总反应为:Zn+2NH4+=Zn2++2NH3↑+H2↑,下列说法正确的是
| A.碳为电池的正极 |
| B.Zn极上发生还原反应 |
| C.Zn2+移向该电池的负极 |
| D.反应2NH4++2e-=2NH3↑+H2↑在负极上发生 |
某学生用锌片、铜片、发光二极管、滤纸、导线等在玻璃片制成如图所示的原电池,当滤纸用醋酸溶液润湿时,二极管发光。下列有关该电池的说法正确的是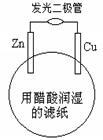
| A.铜片上的电极反应:Cu2+ + 2e- = Cu |
| B.外电路中电子由铜片经导线流向锌片 |
| C.电池工作时电能直接转化为化学能 |
| D.该电池工作时,若有13克锌被溶解,则铜片上产生标况下4.48 LH2 |
用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是
| A.不用稀硫酸,改用98%浓硫酸 | B.加热 |
| C.滴加少量CuSO4溶液 | D.不用铁片,改用铁粉 |
下列有关能量转换的说法正确的是
| A.原电池是将电能转化为化学能的过程 |
| B.煤燃烧是化学能转化为热能的过程 |
| C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 |
| D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 |
根据下列事实:①X+Y2+=X2++Y;②Z+2H2O(冷水)=Z(OH)2+H2↑;③Z2+的氧化性比X2+弱;④由Y、W做电极组成的原电池,电极反应为W2++2eˉ = W,Y-2eˉ=Y2+。可知X、Y、W、Z的还原性由强到弱的顺序是
| A.X>Z>Y>W | B.Z>W>X>Y | C.Z>X>Y>W | D.Z>Y>X>W |
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是
①Zn是负极
②电子由Zn经外电路流向Cu
③Zn -2e-==Zn2+
④Cu2+在溶液中由Cu棒向Zn棒迁移
| A.①② | B.①②③ | C.②③④ | D.①②③④ |
试题篮
()