由碳棒,铁片和200mL 1.5mol/L的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,则:
①总电池反应的离子方程式为 。
②有 mol电子通过了电线?
③此时溶液中H+的物质的量浓度为 (不考虑溶液体积变化)。
由铜片、锌片与200 mL硫酸组成的原电池中,若锌片只发生电化学腐蚀,则当在铜片上共放出0.15 mol气体时,H2SO4恰好全部用完。产生这些气体消耗锌多少克?所用硫酸的物质的量浓度是多少?
(每空2分共8分)在由铜锌组成的原电池(电解质是稀硫酸)中,有位同学在铜电极收集到了12 g的气体,(1) 铜锌原电池的正、负极的电极反应:
正极:_______________________________ 负极:____________________________
(2) 铜电极产生12 g气体的过程中有___ __g的锌溶解。
(3) 铜电极产生12 g气体的过程中有___ __mol的电子发生了转移。
将甲、乙两铂片插入200 g 10% CuSO4溶液中进行电解,当阳极析出0.16 g气体时,求:
(1)阴极析出多少克铜?剩余CuSO4溶液中溶质的质量分数是多少?
(2)需要多少电荷量?
在由铜片、锌片和200 mL稀硫酸组成的原电池中,若锌片只发生电化学腐蚀,当在铜片上放出3.36 L(标准状况)的H2时,硫酸恰好用完,则:
①求产生这些气体时消耗的锌的质量是多少克?
②通过导线的电子的物质的量?
③求原稀硫酸的物质的量浓度。
由等质量的锌片、铜片组成的Zn—Cu—H2SO4原电池,工作一段时间后,锌片的质量减少了2.6g。求:
(1)生成氢气的体积(标准状况);
(2)若将电解质溶液改为硫酸铜溶液,当电池两极的质量差为12.9 g时,从电池中流出的电子数目。
在盛有500mL 0.4mol/LH2SO4混合溶液的大烧杯中。用锌、铜作电极,用导线连接形成原电池,当电极锌消耗6.5g时,试完成:
(1)写出电极反应式:负极_______________;正极_____________________。
(2)电极上共析出氢气的质量。
在由铜锌组成的原电池(电解质是稀硫酸)中,有位同学在铜电极收集到了标准状况下22.4L的气体,
(1)  铜锌原电池的总反应的离子方程式为:________________________________________________________________________
铜锌原电池的总反应的离子方程式为:________________________________________________________________________
(2) 铜电极产生标准状况下22.4L气体的过程中有多少克的锌溶解?
(9分)将铜片、锌片和250mL稀硫酸组成原电池,当在铜片上放出6.72L(标准状况下)的气体时,H2S04恰好反应完全。
(1)该原电池的负极反应式为
(2)原稀硫 酸的物质的量浓度是 mol·L-1
酸的物质的量浓度是 mol·L-1
(3)列式计算锌片减少 的质量。
的质量。
(12分)
Ⅰ.已知常温下,AgCl的Ksp=1.8×10-10,AgBr的Ksp=4.9×10-13。
(1)现向AgCl的悬浊液中:
①加入AgNO3固体,则c(Cl-) (填“变大”、“变小”或“不变”,下同);
②若改加更多的AgCl固体,则c(Ag+) ;
③若改加更多的KBr固体,则c(Ag+) ,c(Cl-) ;
(2)有关难溶盐的溶度积及溶解度有以下叙述,其中正确的是 ;
| A.将难溶电解质放入纯水中,溶解达到平衡时,升高温度, Ksp 一定增大 |
| B.两种难溶盐电解质,其中Ksp小的溶解度也一定小 |
| C.难溶盐电解质的Ksp与温度有关 |
| D.向AgCl的悬浊液中加入适量的水,使AgCl再次达到溶解平衡,AgCl的Ksp不变,其溶解度也不变 |
Ⅱ.最近有人制造了一种燃料电池使汽油氧化直接产生电流,其中一个电极通入空气,另一个电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-。回答下列问题:
(1)以辛烷为汽油的代表物,则这个电池放电时必发生反应的化学方程式是 。
(2)这个电池负极的电极反应式为C8H18 + 25O2- -50e-==8CO2 + 9H2O,,正极的电极反应式为 。固体电解质里O2-的移动方向是 ,向外电路释放电子的电极是 。
由Zn—Cu—H2SO4组成的原电池,工作一段时间后,锌片的质量减少了6.5g。求:
(1)原电池的_______极生成氢气_______L(标准状况)。
(2)已知:1mol氢气完全燃烧放出285.8kJ的热量。将(1)中获得的氢气燃烧,可以得到_________kJ的热量。
(3)若将电解质溶液改为硫酸铜溶液,当电池输出相同的电量时,电池两极的质量差为_____________。
(正常进度)
(1)写出以30%KOH溶液为电解质溶液,甲烷燃料电池的负极电极反应式______。
(2)在标准状况下,甲烷和氧气的混合气体224mL,充分燃烧后,将生成的气体通入100mL 0.02mol/L的石灰水,得到0.1g白色沉淀。求混合气体中甲烷和氧气的体积比。
利用铜棒、锌片和200ml稀硫酸组成原电池,将化学能转化为电能,当铜棒上共产生3.36L(标准状况)气体时,硫酸恰好全部被消耗。请回答下列问题:
(1)该原电池的正极反应式为:
(2)计算原稀硫酸的物质的量浓度。
(3)若将铜棒换成铁片,仍按题给方式组合起来,能否组成原电池呢? (填“能”或“不能”)若能组成原电池,此原电池的负极反应式是
(1) 将铁片和铜片用导线连接并插入足量的CuSO4溶液中,当导线上有0.2mol电子通过时,从理论上分析铁片和铜片的质量变化(写出计算过程);
(2) 将(1)的反应中的铜片和导线去掉,也能发生反应,同样发生0.2mol电子转移时,铁片上的质量又如何变化?(简要地写出计算过程)
随着我国工业化水平的不断发展,解决水、空气污染问题成为重要课题。
(1)汽车尾气的大量排放是造成空气污染的重要因素之一,发展燃料电池汽车可以有效地解决上述问题。直接甲醇燃料电池(DMFC)不会产生有害产物,能量转换效率比内燃机要高2~3倍,电池结构如图所示,c处通入的物质为为______,外电路中电子从______到______(填“A”或“B”)移动,写出电池负极的电极反应方程式 
(2)工业废水中常含有一定量的Cr2O72-,会对人类及生态系统产生很大损害,电解法是处理铬污染的常用方法。该法用Fe做电极电解含Cr2O72-的酸性废水,电解时,在阴极上有大量气泡生成,并产生Cr(OH)3、Fe(0H)3沉淀。
①反应中,1molCr2O72-完全生成Cr(OH)3沉淀,外电路通过电子的物质的量为_________ mol。
②常温下,Cr(OH)3的溶度积 ,当Cr3+浓度小于10
,当Cr3+浓度小于10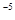 mol
mol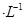 时可认为完全沉淀,电解完全后,测得溶液的pH=6,则该溶液过滤后为___________(填“能”或“否”)直接排放。
时可认为完全沉淀,电解完全后,测得溶液的pH=6,则该溶液过滤后为___________(填“能”或“否”)直接排放。
(3)含氨废水易引发水体富营养化。向NH4Cl溶液中加入少量NaOH固体,溶液中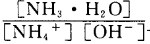 ________(填“增大”“减小”或“不变”);25
________(填“增大”“减小”或“不变”);25 时,NH3•H2O的电离平衡常数
时,NH3•H2O的电离平衡常数 ,该温度下,1mol
,该温度下,1mol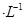 的NH4Cl溶液中
的NH4Cl溶液中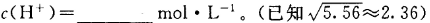
试题篮
()