已知煤的近代结构模型如图所示:
(1)从煤的结构模型来看,煤是工业上获得___________烃的重要来源.
(2)我国大约70%的煤是直接用于燃烧的,从煤的结构模型来看,在提供热量的同时产生大量的___________等气体物质,造成严重的大气污染.
(3)“型煤”技术不仅可以减少87%的废气排放量,烟尘排放量也可减少80%,致癌物苯并[α]芘的排放量也减少,同时节煤20%~30%.“型煤”技术的原理是利用固硫剂在燃烧过程中生成稳定的硫酸盐.下列物质中适宜于做固硫剂的是___________.
| A.氯化钙 | B.氧化钙 | C.硫酸钙 | D.氢氧化钙 |
(4)某“型煤”生产厂利用石灰石作固硫剂,试用化学方程式表示其“固硫”过程.
(5)除上述的“型煤”技术外,为了解决煤燃烧所造成的污染问题和提高煤的利用价值,煤资源的综合利用方法还有___________,___________,___________等.
煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:
| 温度/℃ |
400 |
500 |
800 |
| 平衡常数Kc |
9.94 |
9 |
1 |
试回答下列问题
(1)上述正向反应是: ▲ 反应(选填:放热、吸热)。
(2)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有 ▲ (选填A、B、C、D、E)。
| |
A |
B |
C |
D |
E |
| n(CO2) |
3 |
1 |
0 |
1 |
1 |
| n(H2) |
2 |
1 |
0 |
1 |
2 |
| n(CO) |
1 |
2 |
3 |
0.5 |
3 |
| n(H2O) |
5 |
2 |
3 |
2 |
1 |
(3)已知在一定温度下:C(s)+CO2(g)  2CO(g)平衡常数K;
2CO(g)平衡常数K;
C(s) + H2O(g)  CO(g)+H2(g) 平衡常数K1;
CO(g)+H2(g) 平衡常数K1;
CO(g)+H2O(g) H2(g)+CO2(g) 平衡常数K2 ,
H2(g)+CO2(g) 平衡常数K2 ,
则K、K1、K2之间的关系是: ▲ 。
(4)若在500℃时进行,若CO、H2O的起始浓度均为0.020 mol/L,在该条件下,CO的最大转化率为: ▲ 。
(5)若在800℃进行,设起始时CO和H2O(g)共为5mol,水蒸气的体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y= ▲ 。
(6)在VL密闭容器中通入10molCO和10mol水蒸气,在T℃达到平衡,然后急速除去水蒸气(除水蒸气时各物质的物质的量不变),将混合气体燃烧,测得放出的热量为2842kJ(已知CO燃烧热为283kJ/mol,H2燃烧热为286kJ/mol),则T℃平衡常数K= ▲ 。
石油化工专家闵恩泽院士获2007年度国家最高科学技术奖,他是石油化工技术自主创新的先行者和绿色化学的开拓者,他研制的多种石油炼制催化剂极大地降低了我国石油化工产品的成本。

⑴使用催化剂进行石油裂化及裂解获得的主要产品是 。
⑵“绿色化学工艺”的理想状态是反应物中原子利用率为100%。工业上,通过绿色化学工艺用CO、CH3OH和一种不饱和脂肪链烃合成CH2=C(CH3)COOCH3,该不饱和脂肪链烃的名称为 。
⑶右图表示某石油炼制反应进行过程中能量(单位为kJ·mol-1)的变化示意图。试在答题纸对应的图像中用虚线表示在反应中使用催化剂后能量的变化情况。
⑷科研人员在实验室中按下列流程在催化反应器中装载不同的催化剂,探究不同催化剂对石油裂解反应的催化性能。
| 石油气体 (一定温度) |
 |
催化反应器 |
 |
检 测 |
 |
尾气处理 |
①该探究实验的条件控制非常重要,检测装置中选择的检测试剂及必须注意的问题是 。
②从安全的角度考虑,本实验尾气处理的方法是 。
石油是一种极其重要的资源,是发展国民经济和国防建设重要物资。B的产量通常用来衡量一个国家的石油化工水平,A是生活中常见的有机物,易溶于水并有特殊香味。

Ⅰ.有关物质转化关系如图1所示:
(1)足量烃B通入溴水的实验现象是 。
(2)反应②属于 反应(填有机反应类型)。
(3)写出反应④的化学方程式 。
Ⅱ.某化学兴趣小组对反应③进行探究活动,设计如图2装置进行实验:
(4)在实验中球形干燥管除起冷凝外,另一个重要作用是 。
(5)反应结束后b中的现象是 。
2015年9月20日“长征六号”运载火箭成功将20颗微小卫星送入太空,创造了中国航天一箭多星的新纪录。“长征六号”运载火箭采用无毒环保的过氧化氢一煤油为推进剂。
(1)石油经过 可获得汽油、煤油、柴油、重油等,通过将重油_______可获得更多的汽油、煤油等轻质油。
(2)煤油中的主要组成元素是 (填元素符号)。
(3)在H2O2水溶液中加入少量MnO2粉末时迅速产生大量气泡,该气体能使带火星的木条复燃,该反应中,还原产物是 (填化学式),每产生1mol气体时转移电子的物质的量为__________。
(4)H2O2不稳定,下列各表为在不同条件下1h内H2O2的分解率(均以质量分数为30%的H2O2溶液开始实验):

①在60℃、pH=3.1条件下,H2O2的分解速率为__________mol/(L·min)(已知30%的H2O2溶液的密度为1.11 g/cm3,反应过程中溶液体积变化忽略不计,计算结果保留两位有效数字)。
②结合表中的规律,推测H2O2在下列条件下分解速率依次增大的顺序为_____________(填标号)。
a.30℃、pH =13.0,H2O2溶液的质量分数为30%
b.70℃、pH=9.0,H2O2溶液的质量分数为30%
c.70℃、pH =13.0,H2O2溶液的质量分数为30%
汽油(假设其成分以辛烷计)中加入一定比例的乙醇能提高汽油的燃烧效率,节约能源、减少污染。
(1)加入一定比例乙醇的汽油完全燃烧,比等质量的未加乙醇的汽油完全燃烧,所消耗O2的物质的量 (选填“大”、“小”、“相等”)。
(2)若取22.8 g未加乙醇的汽油,使之完全燃烧,产生的CO2在标准状况下的体积为 。
(3)若取50.2 g掺入乙醇的汽油,与足量O2反应,测得生成CO2的质量为149.6 g。计算所取汽油中乙醇的物质的量是多少?
煤的液化是将煤进行深加工的重要工业过程,请结合下图回答相关问题
(1)煤的液化是将煤转化为 的过程。
(2)煤的液化分为两种分别是 和 ,上图中展示的是 。
(3)该流程中将净化后的氢气和一氧化碳在催化剂的作用下合成 、 及化学品等,该过程中可以循环使用的是 。
(4)这种煤的液化操作条件比较温和,几乎不依赖于煤的种类,关键是 的选择。
鄂尔多斯市已探明煤炭储量1496亿多吨,约占全国总储量的1/6。煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题。
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为 和 。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理为
FeS2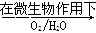 Fe2++SO42-
Fe2++SO42-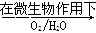 Fe3+
Fe3+
这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为 ,第二步反应的离子方程式为 。
(3)工业煤干馏得到的产品有焦炭、 。
(4)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]= ,实际生产要将r值维持在1.7~2.2之间,原因是 。
煤和石油是重要的能源,也是化工生产的重要原料。
(1)工业上分馏石油的设备是________,通过该设备制备出的液体燃油有__________________________。
(2)使用催化剂进行石油裂化及裂解获得的主要产品是_____________________________。
(3)煤燃烧产生的废气直接排放到空气中,可能导致的环境污染问题是_______ _____________________。
(4)下图是对煤燃烧产生的废气进行常温脱硫处理的流程示意图。
①废气脱硫过程中,主要反应的化学方程式为__________________________、__________________________。
②在煤中直接添加一种物质,可有效减少煤燃烧产生的SO2,该物质是_________________________。
③石膏在工业生产中的用途是________(写出一种用途即可)。
(5)煤经过________(填加工方法)可以得到炉煤气、煤焦油和焦炭。煤焦油经过________(填加工方法)可得到芳香族化合物。煤也可以用氢化法转化成燃油,氢化法的本质是___________________________。
已知煤的近代结构模型如图所示。
回答下列问题:
(1)从煤的结构模型来看,煤是工业上获得____________的重要来源。
(2)我国大约70%的煤是直接用于燃烧的。从煤的结构模型来看,在提供热量的同时产生大量的____________、____________等气体物质,造成严重的大气污染。
(3)“型煤”技术不仅可以减少87%的废气排放量,烟尘排放量也可减少80%,致癌物苯并[α]芘的排放量也减少,同时节煤20%~30%。“型煤”技术的原理是利用固硫剂在燃烧过程中生成稳定的硫酸盐。某“型煤”生产厂利用石灰石作固硫剂,试用化学方程式表示其固硫过程________________、________________。
(4)为了解决煤燃烧所造成的污染问题和提高煤的利用价值,煤资源的综合利用方法还有____________、____________、____________等。
煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题:
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为________和________。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理为FeS2 Fe2++SO42—
Fe2++SO42— Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_____________________________,
Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_____________________________,
第二步反应的离子方程式为____________________。
(3)工业煤干馏得到的产品有焦炭、________。
(4)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=________,实际生产要将r值维持在1.7~2.2之间,原因是__________________________________________。
煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题:
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为 和 。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下图所示:
这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为 ,
第二步反应的离子方程式为 。
(3)工业煤干馏得到的产品有焦炭、 、 等。
(4)湿式石灰石—石膏法脱硫工艺是烟气脱硫技术中最成熟的一种方法。其工艺流程是:烟气经锅炉预热器出来,进入电除尘器除掉大部分粉煤灰烟尘,再经过一个专门的热交换器,然后进入吸收塔,烟气中的SO2与含有石灰石的浆液进行气液接触,通入空气后生成石膏,经脱硫的烟气,应用循环气体加热器进行再加热,进入烟囱,排入大气。
①写出湿法石灰石—石膏法脱硫所涉及的化学反应方程式:__________________________________。
②用石灰石浆液作SO2吸收剂而不用熟石灰吸收SO2的原因是:______________________________。
③上述过程中得到的石膏,如果含氯化合物(主要来源于燃料煤)超过杂质极限值,则石膏产品性能变坏。工业上消除可溶性氯化物的方法是___________________________________________________。
(5)某化学兴趣小组为了测定烟气脱硫所得石膏的组成(CaSO4·xH2O)即测定x值,做如下实验:将石膏加热使之脱水,加热过程中固体的质量与时间的变化关系如图所示。数据表明当固体的质量为2.72g后不再改变。①石膏的化学式为_______________。②图像中AB段对应化合物的化学式为_________________。
在2014年国家科学技术奖励大会上,甲醇制取低碳烯烃技术(DMTO)获国家技术发明奖一等奖。DMTO主要包括煤的气化、液化、烯烃化三个阶段。
(1)煤的气化:用化学方程式表示出煤的气化的主要反应________________________:
(2)煤的液化:下表中有些反应是煤液化过程中的反应:
①a__________0(填“>”、“<”、“=”),c与a、b之间的定量关系为__________。
②K3=__________,若反应③是在容积为2 L的密闭容器巾进行(500℃)的,测得某一时刻体系内 物质的量分别为6 mol、2 mol、10 mol、10 mol,则此时CH3OH的生成速率(填“>”、“<”、“=”) CH3OH的消耗速率。
物质的量分别为6 mol、2 mol、10 mol、10 mol,则此时CH3OH的生成速率(填“>”、“<”、“=”) CH3OH的消耗速率。
(3)烯烃化阶段:如图l是某工厂烯烃化阶段产物中乙烯、丙烯的选择性与温度、压强之间的关系(选择性:指生成某物质的百分比,图中I、Ⅱ表示乙烯,Ⅲ表示丙烯)。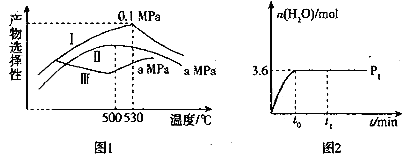
①为尽可能多地获得乙烯,控制的生产条件为__________。
②一定温度下某密闭容器中存在反应,  。在压强为P1时,产物水的物质的量与时间的关系如图2所示,若t0时刻,测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为_________(保留三位有效数字),若在t1时刻将容器容积快速扩大到原来的2倍,请在图中绘制出此变化发生后至反应达到新平衡时水的物质的量与时问的关系图。
。在压强为P1时,产物水的物质的量与时间的关系如图2所示,若t0时刻,测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为_________(保留三位有效数字),若在t1时刻将容器容积快速扩大到原来的2倍,请在图中绘制出此变化发生后至反应达到新平衡时水的物质的量与时问的关系图。
试题篮
()