某有机物A 的分子式为C4H10O,且1molA能与足量金属钠反应生成0.5mol H2(标准状况),
(1)试写出A可能的结构简式
(2)任选一种结构写出在铜作催化剂加热条件下的氧化反应方程式
某有机物的相对分子质量为60,1 mol该有机物完全燃烧,生成36 g H2O和44.8 L CO2(标准状况下)。
(1)求分子式
(2)又知此有机物具有弱酸性,能与金属钠反应,也能与碱溶液反应,试写出它可能的结构简式。
已知4.6克无水乙醇在氧气中完全燃烧,只生成8.8克CO2 和5.4克H2O,则无水乙醇中含有哪几种元素?写出其化学式?完成乙醇燃烧的化学方程式。
0.2 mol有机物和0.4 mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g)。产物经过浓硫酸后,浓硫酸的质量增加10.8 g;再通过灼热CuO充分反应后,固体质量减轻3.2 g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6 g。
(1)判断该有机物的化学式。
(2)若0.2 mol该有机物恰好与4.6 g金属钠完全反应,试确定该有机物的结构简式。
有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是________________;
(2)X与金属钠反应放出氢气,反应的化学方程式是
________________________________________________(有机物用结构简式表达);
(3)X与高锰酸钾酸性溶液反应可生成Z;在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W,若184 g X和120 g Z反应能生成106 g W,计算该反应的产率。(要求写出计算过程)
mg的饱和一元醇,在氧气中完全燃烧后,产生14.4g水和13.44L(标准状况下)二氧化碳气体.
(1)试确定该醇的化学式.
(2)m的值是多少?
有0.2mol的有机物和0.4mol的 在密闭容器中燃烧后的产物为
在密闭容器中燃烧后的产物为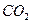 、CO和
、CO和 (气),产物通过浓
(气),产物通过浓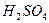 后,质量增加10.8g,再通过灼热的CuO,充分反应后,氧化铜质量减轻了3.2g;最后气体再通过碱石灰完全吸收,质量增加17.6g。
后,质量增加10.8g,再通过灼热的CuO,充分反应后,氧化铜质量减轻了3.2g;最后气体再通过碱石灰完全吸收,质量增加17.6g。
(1)试推断该有机物的分子式 。
(2)若0.2mol的该有机物恰好与9.2g的金属钠完全反应,则有机物的结构简式为 ;名称为 。
0.2mol 有机物和 0.4mol O2在密闭容器中燃烧后的产物为 CO2、CO 和 H2O(g)。 燃烧后的这些产物经过浓H2SO4后,质量增加 10.8g;再通过灼热的 CuO 充分反 应后,固体质量减轻 3.2g,最后气体再通过碱石灰被完全吸收,质量增加 17.6g。
(1)推断该有机物的分子式。
(2)若 0.2mol 该有机物在与过量的金属钠完全反应后放出 4.48LH2(标准状 况),试确 定有机物的结构简式。
某工业反应混合液中仅可能含有的组分是:乙醚(C4H10O)、乙醇(C2H6O)和水,经分析,液体中C、H、O各原子数之比为16∶42∶5。
(1)若混合液中只含两种组分,则所有可能的组合是:
_______________________________________________________________________________。
(2)若混合液中含有三种组分,在628 g混合液中有1 mol H2O,此时乙醇和乙醚的物质的量各是多少?
有机物A由碳、氢、氧三种元素组成。现取3g A与4.48L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重3.6g,碱石灰增重4.4g。回答下列问题:
(1)3gA中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
试题篮
()