主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3 倍。X、Y和Z分属不同的周期,他们的原子序数之和是W原子序数的5倍。在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高。请回答下列问题:
⑴W元素原子的L层电子排布式为 ,W3分子的空间构型为 ;
⑵化合物M的化学式为 ,其晶体结构与NaCl相同,而熔点高于NaCl。M熔
点较高的原因是 ;
⑶将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯。在碳酸二甲酯分子中O—C—O的键角约为 ;
⑷X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X︰Y︰Z= 。
试根据上表填空:
| A |
|
|
||||||||||||||||
| |
B |
|
|
C |
D |
E |
F |
|
||||||||||
| G |
H |
I |
J |
|
L |
K |
M |
|||||||||||
| |
|
|
|
|
|
|
N |
|
|
Q |
|
|
|
|
|
|
|
|
(1)请写出元素Q的基态原子电子排布式 ;元素N在周期表中的位置 周期 族。
(2)基态D原子核外有 个未成对电子;D2分子中分别有 个, 个π键。
(3)化合物DA5中既含离子键,又含共价键和配位键,请写出它的电子式 。
(4)表四中的元素能形成XY2型的共价分子有CE2、CL2、BK2、LE2四种,其分子的空间构型中有一种与其他三种不同,它是 (填化学式);而形成XY3型的共价分子也有四种,它们分别是DA3、DF3、DK3、LE3,其分子的空间构型中也有一种与其他三种不同,它是 (填化学式),它是由_ 键(填“极性”或“非极性”,下同)构成的 分子。
(5)第三周期8种元素按单质熔点高低的顺序如右图所示,其中序号“8”所代表的元素是 (填元素符号);其中气态氢化物稳定性最强的元素是 (填下图中的序号)。
(6)科学家证实,IK3属于共价化合物,分子式为I2K6,其结构式为下列四种中的一种,你认为正确的结构式是____________。
(7)向Q的硫酸盐溶液中加入足量的DA3的水溶液过程中,请写出发生反应的离子方程式 ;最后生成配离子的结构式为 。
下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
(1)T3+的核外电子排布式是:
(2)Q、R、M的第一电离能由大到小的顺序是 (用元素符号表示)
(3)根据下列说法填空:
①G单质的熔点高于J单质,是因为
②将J2M2溶于水,要破坏 (离子键、极性共价键、非极性共价键)
③RE3沸点高于QE4,是因为
④一个Q2E4分子中E的 轨道与Q的 轨道形成σ键。
(4)G与R单质直接化合生成一种离子化合物G3R。该晶体具有类似石墨的层状结构。每层中,G原子构成平面六边形,每个六边形的中心有一个R原子。层与层之间还夹杂一定数量的原子。请问这些夹杂的原子应该是 (填G或R的元素符号)
最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子,其分子结构如图所示,已知断裂1molN—N吸收167kJ热量,生成1molN≡N放出942kJ热量,则下列说法正确的是
| A.N4属于一种新型化合物 |
| B.N4与N2互为同位素 |
| C.N4沸点比P4(白磷)高 |
| D.1molN4气体转变为N2将放出882kJ热量 |
目前已知化合物中数量、品种最多的是IVA碳的化合物(有机化合物),下列关于其原因的叙述中不正确是( )
| A.碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键 |
| B.碳原子性质活泼,可以跟多数元素原子形成共价键 |
| C.碳原子之间既可以形成稳定的单键,又可以形成稳定的双键和三键 |
| D.多个碳原子可以形成长度不同的链、支链及环,且链、环之间又可以相互结合 |
目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍行业发展蕴藏着巨大潜力。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于 晶体;基态Ni原子的电子排布式为 。
(2)配合物分子内的作用力有 (填编号)。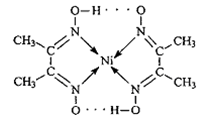
| A.氢键 | B.离子键 | C.共价键 | D.金属键 E.配位键 |
(3)很多不饱和有机物在Ni催化下可以与H2发生加成反应。如
①CH2=CH2、②CH≡CH、③苯、④HCHO等,
其中分子属于平面结构的有 (填物质序号),预测HCHO分子的立体结构为 形。
(4)氢气是新型清洁能源,镧(La)和镍(Ni)的合金可做储氢材料。该合金的晶胞如图所示,晶胞中心有一个镍原子,其他镍原子都在晶胞面上,镧原子都在晶胞顶点上。该晶体的化学式为 。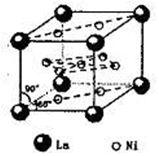
氮元素可以形成多种化合物。回答以下问题:
(1)基态氮原子的价电子排布式是_________________。
(2)C、N、O三种元素第一电离能从大到小的顺序是____________。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是_______________;N2H4分子中氮原子轨道的杂化类型是___________。
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g) △H=-1038.7kJ·mol-1
若该反应中有4mol N-H键断裂,则形成的π键有________mol。
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在__________(填标号)
a. 离子键 b. 共价键 c. 配位键 d. 范德华力
(4)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。
下列分子或离子中,能被该有机化合物识别的是_________(填标号)。
a. CF4 b. CH4 c. NH4+ d. H2O
固体A的化学式为NH5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,该物质适当加热就分解成两种气体,试完成:
(1)固体A属于__________晶体,它的电子式为__________。
(2)A溶于水后溶液呈__________性(填“酸”“碱”或“中”),其原因是(用化学方程式表示)______________________________。
(3)A与铜或铜的某些化合物在一定条件下可合成CuH,CuH是一种难溶物,它能在氯气中着火,还能与盐酸反应放出气体,请写出这两种反应的化学方程式___________________ 。
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2) 3的说法正确的是
| A.分子中N、O间形成的共价键是非极性键 |
| B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 |
| D.15.2g该物质含有6.02×1022个原子 |
【化学—选修3:物质结构与性质】
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素的核外电子数和电子层数相等,也是原子半径最小的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2 =" 1451" kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式
(2)B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈 形
(3)某同学根据上述信息,推断C基态原子的核外电子排布为,
该同学所画的电子排布图违背了
(4)G位于 族 区,价电子排布式为
(5)DE3 中心原子的杂化方式为 ,用价层电子对互斥理论推测其空间构型为
(6)检验F元素的方法是 ,请用原子结构的知识解释产生此现象的原因是
(7)F元素的晶胞如下图所示,若设该晶胞的密度为a g/cm3,阿伏加德罗常数为NA,
F原子的摩尔质量为M,则F原子的半径为 cm
某同学对“CO2是共价化合物和NH4Cl是离子化合物”, 有下列四点感悟,其
中不正确的是( )
| A.离子化合物中可能含共价键 | B.共价化合物中一定不含离子键 |
| C.离子化合物中不一定含金属元素 | D.离子化合物中一定不含共价键 |
(13分)(1)A、B、D为短周期元素,请根据信息回答问题:
| 元素 |
A |
B |
D |
| 性质或结构信息 |
工业上通过分离液态空气获得其单质,单质能助燃 |
气态氢化物的水溶液显碱性 |
原子有三个电子层,简单离子在本周期中半径最小 |
①第一电离能:A B(填“>”、“=”、“<”),基态D原子的电子排布式为 。
②B和D由共价键形成的某化合物BD在2200℃开始分解,BD的晶体类型为 。
(2)发展煤的液化技术被纳入“十二五规划”,中科院山西煤化所关于煤液化技术的高效催化剂研发项目取得积极进展。已知:煤可以先转化为一氧化碳和氢气,再在催化剂作用下合成甲醇(CH3OH),从而实现液化。
①某含铜离子的离子结构如右图所示:
在该离子内部微粒间作用力的类型有: (填字母)。
A.离子键 B.极性键 C.非极性键 D.配位键 E.范德华力 F.氢键
②煤液化获得甲醇,再经催化得到重要工业原料甲醛(HCHO),甲醇的沸点为65℃,甲醛的沸点为-21℃,两者均易溶于水。甲醇的沸点比甲醛高是因为甲醇分子间存在着氢键,而甲醛分子间没有氢键。甲醇和甲醛均溶于水,是因为它们均可以和水形成分子间氢键。请你说明甲醛分子间没有氢键的原因是 。
③甲醇分子中,进行sp3杂化的原子有 ,甲醛与H2发生加成反应,当生成1mol甲醇时,断裂的∏键的数目为
T、X、Y、Z、Q、R、W为周期表前四周期的元素,原子序数依次递增。已知:
①W的原子序数为29,其余元素均为短周期主族元素;
②T原子所处的周期数、族序数分别与其原子序数相等;
③X的基态原子电子占据三种能量不同的轨道,且每种轨道中的电子数相同;
④Z的基态原子价电子排布为ns2npn+2;
⑤在该元素所在的周期中,Q的基态原子的第一电离能最小;
⑥R的单质常温常压下是气体,其基态原子的M层上有1个未成对的p电子;
(1)X、Y、Q三种元素的电负性由大到小的顺序是 (用元素符号表示)。
(2)与W同周期的元素中,原子最外层电子数与W元素原子相同的元素还有 (填元素符号)。由W2+制取[W(YT3)4]2+的离子方程式为 。
(3)T、X、Z三种元素组成的一种化合物M是蚂蚁分泌物和蜜蜂的分泌液中含有的物质,俗称蚁酸,它的分子式为XT2Z2,则该分子的X原子采取 杂化,1mol M分子中δ键和π键的个数比为 。
(4)X和Y原子结合形成的X3Y4晶体,其晶体结构与金刚石类似,但硬度比金刚石大,其原因是 。
Ⅰ.顺铂是美国教授B Rosenberg等人于1969年发现的第一种具有抗癌活性的金属配合物,它的化学式为Pt(NH3)2Cl2。
(1)与NH3互为等电子体的分子、离子有 、 (各举一例)。
(2)碳铂是1,1-环丁二羧酸二氨合铂(Ⅱ)的简称,是第二代铂族抗癌药物,其他毒副作用低于顺铂。碳铂的结构如下图:
碳铂中含有的作用力有 (填字母)。
| A.极性共价键 | B.非极性共价键 | C.配位键 | D.离子键 |
E.金属键 F.σ键 G.π键
(3)碳铂中C原子的杂化方式有 。
(4)铂(Pt)单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
晶胞中铂(Pt)原子的配位数为 。
Ⅱ.原子序数小于36的元素A和B,在周期表中既处于同一周期又位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。请写出A2+在基态时外围电子(价电子)排布式为 , B元素在周期表中的位置为 。
下表为长式周期表的一部分,其中的编号代表对应的元素。
| ① |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |
② |
|
|
|
|
|
|
|
|
|
|
|
③ |
④ |
⑤ |
⑥ |
|
| |
⑦ |
|
|
|
|
|
|
|
|
|
|
|
|
|
⑧ |
|
|
| |
|
|
|
|
⑨ |
|
|
|
|
⑩ |
|
|
|
|
|
|
|
(1)写出上表中元素⑨原子的外围电子排布式 。
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为:
(3)按要求完成下列各题
a.第一电离能:元素④ 元素⑤(选填“>”、“=”、“<”)。
b.与元素④所形成的单质互为等电子体的分子、离子的化学式 、 (各写一种)。
c.元素④的气态氢化物X的水溶液在微电子工业中,可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为________________________________
d.由X与氧气、KOH溶液构成原电池,负极会产生元素④的单质。则其负极反应式为_____________________________。
(4)由元素③和⑧形成的液态化合物Z,是非极性的直线形分子。0.2mol的Z在O2中完全燃烧,生成两种气态氧化物,298K时放出热量215kJ。该反应的热化学方程式为_________________________
(5)在测定①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是: 。
(6)元素⑩所形成的单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。已知该原子的半径为d pm,相对原子质量为M,NA代表阿伏加德罗常数,请回答:

晶体中该原子的配位数为 ,一个晶胞中包含的原子数目为 ;该晶体的密度为 g·cm-3(用字母表示,不必化简)。
试题篮
()