核能源已日益成为当今世界的主要能源。
(1)核能原料UO2可通过三碳酸铀酰铵(NH4)4[UO2(CO3)3]直接煅烧还原制得。UO2晶体属CaF2型面心立方结构(CaF2的晶胞示意图如图),则UO2晶体U4+的配位数为 ;三碳酸铀酰铵中含有化学键类型有 ;
| A.离子键 | B.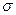  键 键 |
C.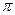 键 键 |
D.氢键 E.配位键 |
根据价层电子对互斥理论推测CO32—的空间构型为 ;写出一种与CO32—互为等电子体且属于非极性分子的微粒的化学式 。
(2)为了获得高浓度235U,科学家们采用“气体扩散法”;到目前为止,UF6是唯一合适的化合物。UF6在常温常压下是固体,在56.4℃即升华成气体。UF6属于 晶体。
(3)放射性碘是重要的核裂变产物之一,因此放射性碘可以为核爆炸或核反应堆泄漏事故的信号核素。写出131I基态原子的价电子排布式 。
下列对化学反应的认识正确的是
| A.化学反应过程中,一定有化学键的断裂和形成 |
| B.化学反应过程中,某离子被沉淀完全时,该离子在溶液中的浓度即为0 |
| C.化学反应过程中,分子的种类和数目一定发生改变 |
| D.放热反应的反应速率,一定比吸热反应的反应速率快 |
1-1 2011年是国际化学年,是居里夫人获得诺贝尔化学奖100周年。居里夫人发现的两种化学元素的元素符号和中文名称分别是 和 。
1-2 向TiOSO4水溶液中加入锌粒,反应后溶液变为紫色。在清夜中滴加适量的CuCl2水溶液,产生白色沉淀。生成白色沉淀的离子方程式是 ;继续滴加CuCl2水溶液,白色沉淀消失,其离子方程式是 。
1-3 20世纪60年代维也纳大学V.Gutmann研究小组报道,三原子分子A可由SF4和NH3反应合成;A被AgF2氧化得到沸点为为27℃的三元化合物B。A和B分子中的中心原子与同种端位原子的核间距几乎相等;B分子有一根三种轴和3个镜面。画出A和B的结构式(明确示出单键和重键,不在纸面上的键用楔形键表示,非键合电子不必标出)。
1-4 画出Al2(n-C4H9)4H2和Mg[Al(CH3)4]2的结构简式。
1-5 已知EӨ(FeO42—/Fe3+) =" 2.20" V,EӨ(FeO42—/Fe(OH)3) =" 0.72" V。
①写出氯气和三氯化铁反应形成高铁酸根的离子方程式。 。
②写出高铁酸钾在酸性水溶液中分解的离子方程式。 。
③用高铁酸钾与镁等组成碱性电池,写出该电池的电极反应 。
(8分)在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂的化学式是__________;X与氢元素形成的化合物的电子式是__________。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是__________;D与E能形成一种非极性分子,该分子的结构式为__________;D所在族元素的氢化物中,沸点最低的是__________。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是__________。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为
________________________________________________________________________。
氢化钠(NaH)是一种白色的离子化合物,其中钠元素显+1价;氢化钠与水反应放出氢气。下列叙述中,不正确的是
| A.NaH中存在-1价的氢离子,还原性比氢原子强 |
| B.NaH与H2O反应时水作氧化剂,反应放出热量 |
| C.NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同 |
| D.微粒半径:H+>H>H- |
【化学—物质结构与性质】
氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要作用。
请回答下列问题。
(1)砷原子外围电子排布式为 。
(2)熔沸点:NH3 PH3(>、<、=)原因是
(3)N、P、As三种元素电负性由小到大的顺序为 ,NCl3分子中中心原子的杂化方式为 。
(4)汽车尾气中CO和NO 经催化剂作用变成N2和CO
经催化剂作用变成N2和CO 2,此反应中三种元素第一电离能由小到大的顺序为 ,在这四种物质中含有极性键的非极分子内
2,此反应中三种元素第一电离能由小到大的顺序为 ,在这四种物质中含有极性键的非极分子内 键和
键和 键的比为 。
键的比为 。
(5)K3[Fe(CN)6]配合物中微粒的相互作用力有 ,配位体为 。
| A.氢键 | B.离子键 | C.共价键 | D.配位键[E.范德华力 |
(6)CO、NH3都能提供孤电子对与Cu+形成配合物。Cu+与NH3形成的配合物可表示为
[Cu(NH3)n]+。该配合物中,Cu+的4s轨道及4p轨道通过sp杂化接受NH3提供的孤电子 对,则[Cu(NH3)n]+中n的值为
对,则[Cu(NH3)n]+中n的值为  。
。
下列四种判断:①两种弱酸相互反应生成两种强酸;②两种弱酸盐相互作用后生成两种强酸盐;③一种弱酸和一种盐溶液作用后,得到一种强酸和一种盐;④两种酸溶液混合后,溶液的酸性减弱。其中有具体例证的是( )
| A.①②③④ | B.①②③ | C.②③④ | D.①③④ |
下列有关物质性质比较正确的是
| A.密度:水>1—溴丙烷 | B.沸点:新戊烷>正戊烷 |
| C.羟基活性:酚羟基>醇羟基 | D.水中溶解度:乙酸乙酯>乙醇 |
类推的思维方法在化学学习与研究中常会产生错误的结论。因此类推出的结论最终要经过实践的检验才能确定其正确与否。下列几种类推结论中正确的是
| A.从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构 |
| B.NaCl与CsCl化学式相似,故NaCl与CsCl的晶体结构也相似 |
| C.苯不能使酸性高锰酸钾溶液褪色,故苯的同系物也不能使酸性高锰酸钾溶液褪色 |
| D.CO2通入Ca(ClO)2溶液生成CaCO3和HClO,SO2通入Ca(ClO)2溶液也生成CaSO3和HClO |
形成物质世界多样性的原因有( )
①元素种类 ②同位素 ③化学键成键方式 ④同分异构现象 ⑤同素异形现象
| A.仅①②③ | B.仅②④⑤ | C.仅①③ | D.①②③④⑤ |
快乐是什么?精神病学专家通过实验发现:在大脑的相应部位——“奖赏中心”,给予柔和的电击,便会处于似乎极度快乐的状态.人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统.
多巴胺结构如图:
(1)多巴胺分子式: .
(2)试判断多巴胺能发生的化学反应 .
| A.加成 | B.取代 | C.氧化 | D.水解 |
(3)写出与多巴胺互为同分异构体且满足下列三个条件的所有物质的结构简式:
①属于1、3、5三取代苯 ②苯环上直接连有一个羟基和一个氨基
③分别能与钠和氢氧化钠反应,消耗钠与氢氧化钠的物质的量之比为2:1
.
(4)多巴胺可由香兰素与硝基甲烷缩合,再经锌汞齐还原水解而得.合成过程表示如下:
(Ⅰ) 写出下列反应类型:反应① ,反应⑤ .
(Ⅱ) A的结构简式: .
(Ⅲ) 写出②的化学方程式: .
[化学——选修物质结构与性质](15分)
原子序数依次增大A、B、C、D、E、F(A、B、C、D、E、F分别代表元素符号)六种短周期元素。元素A的原子半径在短周期中最小,元素C的单质在空气中含量最多, 比
比 少一个电子层,E所在周期的各元素单质沸点变化如下图(元素按原子序数递增顺序连续排列),B、C两种元素分别能与A形成等电子的
少一个电子层,E所在周期的各元素单质沸点变化如下图(元素按原子序数递增顺序连续排列),B、C两种元素分别能与A形成等电子的 甲、乙两种分子,且两种
甲、乙两种分子,且两种
分子中各原子的个数见下表:
| 化合物 |
甲 |
乙 |
| 原子个数比 |
B:A=1:4 |
C:A=1:3 |
(1)元素F的基态原子的电子排布式为 。
(2)分子甲的空间构型为 ,该分子中B的
原子轨道发生的是 杂化。
(3)E单质属于 晶体,E与A元素形成 分子(填“极性”或“非极性”)
(4)D在F中燃烧的产物属于 晶体,其晶体中与 最近且等距离的
最近且等距离的 有 个。
有 个。
(5)C元素的第一电离能( ) 氧元素的第一电离能(
) 氧元素的第一电离能( )(填“<”或“>”或“=”)。
)(填“<”或“>”或“=”)。
试题篮
()