今有Ba(NO3)2、AgNO3、Fe(NO3)3的混合液,欲将Ba2+、Ag+、Fe3+
分离,分别得到三种元素的不溶物,按下图所示实验:
(1)加入的试剂(写化学式):X______,Y______,Z______。生成的沉淀(写化学式):A______,B______,C______。
(2)写出反应①②③的离子方程式:①____________,②____________,③____________。
实验室可利用乙二醇、铜或铜的化合物制备乙二醛,右图是某兴趣小组设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,试管C中装有水(加热装置未画出)。试回答:
(1)两套装置中的A、B处都需加热,
A处用水浴加热,B处用 ▲ 加热,A处用水浴加热的主要优点是 ▲ 。
(2)若按甲装置进行实验,B管处装铜粉,则通入A管的X是 ▲ ,
B中反应的化学方程式为 ▲ 。
(3)若按乙装置进行实验,则B管中应装 ▲ ,B中反应的化学方程式为 ▲ 。
(4)实验完成时先打开D处的铁夹,再撤去酒精灯,试说明这样做的目的是 ▲ 。
(1)下列实验设计或操作合理的是__________。
a.实验室制溴苯时选用的试剂可以是溴水、苯和铁屑。
b.配制银氨溶液时,将氨水逐滴加到 AgNO3溶液中,边加边振荡,直至沉淀恰好完全消失。
c.将10滴溴乙烷加入到1mL10%的烧碱溶液中,加热片刻后,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子。
d.实验室制乙炔时,为了减慢反应速率,可用饱和食盐水代替蒸馏水。
(2)溴水是中学化学实验中常用的一种试剂,用溴水可鉴别出下列各组物质,试写出发生反应的化学方程式。
①苯酚与乙醇
②乙烯与乙烷
工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1)题26图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是;溶液的出口为(填字母);精制饱和食盐水的进口为(填字母);干燥塔中应使用的液体是。

(2)多晶硅主要采用还原工艺生产,其副产物
的综合利用收到广泛关注。
①可制气相白炭黑(与光导纤维主要原料相同),方法为高温下
与
和
反应,产物有两种,化学方程式为。
②可转化为
而循环使用。一定条件下,在20L恒容密闭容器中的反应:
达平衡后,
与
物质的量浓度分别为0.140mol/L和0.020mol/L,若
全部来源于离子交换膜法的电解产物,理论上需消耗纯
的质量为kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气 (标准状况)。
(标准状况)。
MgSO4·7H2O医药上用作泻剂。工业上用氯碱工业的一次盐泥为原料生产。已知一次盐泥中含有镁、钙、铁、铝、锰的硅酸盐和碳酸盐等成分。主要工艺如下: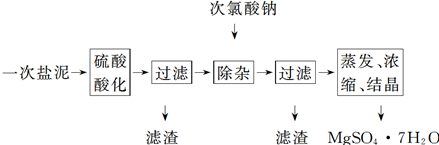
(1)用硫酸调整溶液pH为1~2,硫酸的作用是________________________________________。
(2)加次氯酸钠溶液至pH为5~6并加热煮沸约5~10 min,滤渣中主要含MnO2和另两种沉淀:__________________、____________(写化学式)。其中次氯酸钠溶液将MnSO4转化为MnO2的离子方程式为________________________ ___
(3)若除杂后过滤,发现滤液发黄,需采取的措施是____ ____
(4)过滤后晶体常用丙酮代替蒸馏水洗涤的目的是________________________________________
(5)晶体中结晶水含量的测定:准确称取0.20 g MgSO4·7H2O样品,放入已干燥至恒重的瓷坩埚中,置于马沸炉中,在200 ℃脱水1 h。为准确确定脱水后的质量,还需要经过的操作有冷却(干燥器中)至室温→__________ _________________
(6)硫酸根离子质量分数的测定:准确称取自制的样品0.50 g,用200 mL水溶解,加入2 mol·L-1 HCl溶液5 mL,将溶液加热至沸腾,在不断搅拌下逐滴加入5~6 mL 0.5 mol/L BaCl2溶液,充分沉淀后,得沉淀0.466 g,则样品中w(SO42-)=________________。
(7)已知:Na2CO3·10H2O (s)=Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH2=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式__ __________。
下图是某化学兴趣小组设计的利用电子垃圾(含70%Cu、25%Al、4%Fe及少量Au、Pt)制备硫酸铜和硫酸铝晶体的路线: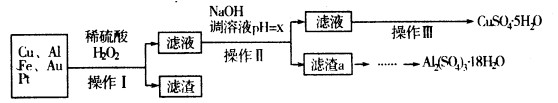
已知下列信息:
Cu可与稀硫酸和H2O2的混合液反应生成硫酸铜;铁、铝、铜等离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Cu(OH)2 |
| 开始沉淀 |
1.1 |
4.0 |
5.4 |
| 完全沉淀 |
3.2 |
5.2 |
6.7 |
请回答下列问题:
(1)写出Cu与稀硫酸和H2O2的混合液反应的化学方程式: .。
(2)在操作Ⅱ中,x的取值范围是 。
(3)在操作Ⅲ中,蒸发浓缩需要的玻璃仪器有 。
(4)由滤渣a制取Al2(SO4)3·l8H2O,探究小组设计了三种方案: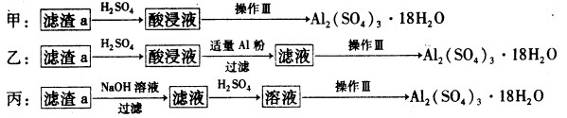
综合考虑上述三种方案,最具可行性的是 (填序号)。
(5)为测定CuSO4·5H2O晶体的纯度,进行下列实验:取a g试样配成l00 mL溶液,每次取20.00mL,消除干扰离子后,用b mol·L-1EDTA(Na2H2Y)标准溶液滴定其中的Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,平均消耗EDTA溶液l2.00 mL。(常温时,5%的Na2H2Y水溶液,其pH为4—6。)
①CuSO4·5H2O晶体的纯度是 。
②下列滴定方式中,最合理的是(夹持部分略去) (填序号)。
某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。
(1)提出假设 ①该反应的气体产物是CO2。
②该反应的气体产物是CO。
③该反应的气体产物是 。
(2)设计方案 如下图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
(3)查阅资料氮气不与碳、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)
饱和溶液混合加热反应制得氮气。请写出该反应的离子方程式: 。
(4)实验步骤
①按上图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g碳粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g。
步骤②、④中都分别通入N2,其作用分别为 ;
。
(5)数据处理试根据实验数据分析,写出该实验中氧化铁与碳发生反应的化学方程式:
。
(6)实验优化 学习小组有同学认为应对实验装置进一步完善。
①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是 。
②从环境保护的角度,请你再提出一个优化方案将此实验装置进一步完善: 。
试题篮
()