反应物间进行微粒交换是化学反应的特征之一,置换反应、复分解反应、取代反应都属于反应物间进行微粒交换的化学反应。
(1)NaHCO3和NaOH的反应是NaHCO3电离的H+离子和NaOH电离出的 离子相互交换的反应。
(2)在浓硫酸作用下,羧酸与醇也是微粒交换的反应,请写出乙酸和乙醇反应的化学方程式: 。
(3)工业上利用铝热反应用铝粉和MnO2冶炼金属锰,写出化学方程式: 。
(4)工业上制取粗硅的反应也是一个置换反应,此反应的反应物中含有三种元素,这三种元素的非金属性由强到弱的顺序为 。与硅同周期的某元素,其最高价氧化物既可溶于强酸又可溶于强碱,请写出该氧化物溶于强碱的离子方程式: 。
(5)NH3和Cl2发生置换反应,当NH3过量时,NH3继续与HCl反应。当有3molCl2参与反应时,有
molNH3被氧化。
(6)(NH4)2CO3和H2CO3的反应也进行微粒交换,当往(NH4)2CO3溶液中通入一定量CO2至溶液呈中性时,溶液中HCO3-和NH4+的比值 (填“大于”“小于”或“等于”)1:1。
颠茄酸酯(J)是一种溃疡病治疗的辅助药物,其合成路线如下: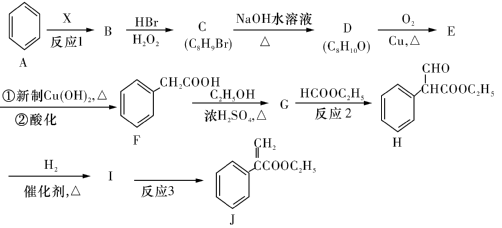
试回答下列问题:
(1)烃B其相对分子质量小于118,分子中氢的质量分数为7.69% ,且反应1为加成反应,则X的名称为________。B含有的官能团是____________。
(2)G→H 的反应类型为____________。
(3)C的结构简式为__________。
(4)反应3的化学方程式为_________________。
(5)化合物I有多种同分异构体,同时满足下列条件的结构有_______种。
①能发生水解反应和银镜反应;②能与FeC13发生显色反应;③苯环上有四个取代基,且苯环上一卤代物只有一种
(6)参照颠茄酸酯的合成路线,设计一条以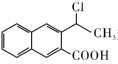 为起始原料制备
为起始原料制备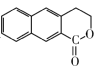 的合成路线___________________________________________。
的合成路线___________________________________________。
下列物质中属于强电解质的是 。
①含有强极性键的HF ②不溶于水的BaSO4、AgCl ③稀H2SO4溶液 ④易溶于水的醋酸 ⑤Na2O、Na2O2、NaCl ⑥水溶液浓度为0.1 mol·L-1,pH=1的HA ⑦NH3的水溶液⑧氯水
火箭发射时可用肼(N2H4)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。
已知N2 (g) + 2O2 (g)=2NO2 (g) △H ="+67.7" kJ/mol
N2H4 (g) +O2 (g)=N2 (g) + 2H2O (g) △H =" -534" kJ/mol
则N2H4和NO2反应的热化学方程式为____________________________________________
请把下列物质按类别填空:
A Na2O B K2SO4 C NaHCO3 D 镁铝合金
E Na F CaO G CaCO3 H Ca(OH)2
(1)属于盐的是________________________________;
(2)属于碱的是________________________________;
(3)属于单质的是________________________________;
(4)属于氧化物的是________________________________。
维生素和微量元素是生命基础的重要物质。如中学生每天需要补充维生素C约60㎎,微量元素碘约150μg。
(1)维生素C又称抗坏血酸,其水溶液显酸性。向维生素C的溶液中滴加紫色石蕊溶液,溶液变___色。某同学欲探究维生素C的还原性,可选择的试剂是_____(填序号)。
①碘水、淀粉 ②KI溶液 ③酸性KMnO4溶液
(2)食用加碘盐可预防碘缺乏症,其中加入的含碘物质是碘酸钾。碘酸钾的化学式为____(填序号)。
①I2 ②KI ③KIO3
已知在酸性条件下,碘化钾与碘酸钾反应可生成碘单质。若用盐酸酸化的碘化钾淀粉溶液检验碘盐中的碘酸钾,可观察到的现象是__________。
1个H2SO4分子中含有_______ 个氢原子,_______个氧原子,6.02×1023个H2SO4分子中H原子的物质的量_______,氧原子的物质的量_______。
相等质量的CO和CH4相比较,请完成下列问题。
(1)它们所含的分子数目之比为____________;
(2)同温同压时密度之比为___________;
(3)同温同体积时的压强之比为____________;
(4)同温同压时体积之比为___________。
已知氢气和氧气反应生成1mol水蒸气时可以放出241.8kJ的热量,1g水蒸气转化为液态水放热2.444kJ。写出表示H2燃烧热的热化学方程式 。
(1)0.1molO2中,含有 mol O;
(2)标准状况下,67.2L Cl2的物质的量为 mol;
(3)4gNaOH固体的物质的量为 mol,将其溶于水配成500mL溶液,此溶液中NaOH的物质的量浓度为
现有九种物质(1)铝线(2)石墨(3)氯气(4)硫酸镁晶体(5)无水乙酸(6)金刚石(7)石灰水(8)乙醇(9)熔融的硝酸钾
其中能导电的是 ;
属于电解质的是 ;
既不是电解质也不是非电解质的是 .
乙酸的电离方程式是
乙酸钠水解的离子方程式是
(1)有以下几种物质:①食盐晶体 ②铜 ③KNO3溶液 ④熔融的氢氧化钾 ⑤液态氯化氢 ⑥二氧化碳 ⑦酒精。回答以下问题(填序号):
以上物质中能导电的是 ;属于电解质的是 ;
(2)写出下列物质在水中的电离方程式:
H2SO4 ==
KClO3 ==
试题篮
()