用纯碱和双氧水混合可制作新型液体洗涤剂(2Na2CO3·3H2O2),它具有杀菌消毒去油污的能力且不会污染水源。
(1)检验这种新型洗涤剂中金属阳离子的操作和现象是 。
(2)这种洗涤剂中的双氧水可以将废水中的CN一转化生成NH3,写出该反应的离子方程式 。
(3)如果配制洗涤剂的水中含有铁离子,不仅会削弱洗涤剂的去污能力,甚至会完全失去杀菌作用。试分析其中可能的原因(写出其中一种即可,用离子方程式和简要文字表述)____________________。
(4)某化学学习小组为了定性探究铁离子对这种新型洗涤剂的不良影响,取该洗涤100mL,加入25gFeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请选用下列试剂和实验用品完成气体成分的探究过程:0.10mol.L-l NaOH溶液、8.0mol.L-l NaOH:溶液、澄清石灰水、0.l0mol.L-1 KMn04溶液、BaCI2稀溶液、品红溶液、蒸馏水、木条、酒精灯、火柴、洗气瓶。
①提出假设:对该气体成分提出合理假设。
假设1:气体是O2。
假设2:气体是CO2。
假设3:气体是
②设计方案:设计实验方案证明你的假设,在下表中完成实验步骤、预期现象和结论。
| 实验步骤 |
预期现象和结论 |
| 将气体依次通入盛有_____________________、________________的洗气瓶中,并_______________。 |
___________________________________ |
盐泥是氯碱工业中的废渣,主要含有镁、铁、铝、钙等的硅酸盐和碳酸盐。实验室以盐泥为原料制取MgSO4·7H2O的流程如下:

已知:(Ⅰ) Ksp[Mg(OH)2]=6.0×
(Ⅱ) Fe2+、Fe3+、Al3+开始沉淀到完全沉淀的pH范围依次为:7.1~9.6、2.0~3.7、3.1~4.7
(Ⅲ) 三种化合物的溶解度(S)随温度变化曲线如图。

回答下列问题:
(1)在盐泥中加H2SO4溶液控制pH为1~2以及第一次煮沸的目的是: 。
(2)若溶液中Mg2+的浓度为6 mol/L,溶液pH≥ 才可能产生Mg(OH)2沉淀。
(3)第二次过滤需要趁热进行,主要原因是 。所得滤渣的主要成分是 。
(4)从滤液Ⅱ中获得MgSO4·7H2O晶体的实验操作步骤为:①向滤液Ⅱ中加入 ,②过滤,得沉淀,③ ,④蒸发浓缩,降温结晶,⑤过滤、洗涤得产品。
(5)若获得的MgSO4·7H2O质量为24.6 g,则该盐泥中含镁[以Mg(OH)2计]的百分含量约 (MgSO4·7H2O式量为246)
空气污染问题日益引起全民关注。工业生产中产生的SO2、NO等为主要污染物。根据你所学化学知识完成下列问题:
Ⅰ.(1)PM2.5是指大气中直径小于或等于2.5μm(1μm=103nm)的颗粒物。下列说法不正确的是_________(填字母序号)。
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1~2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
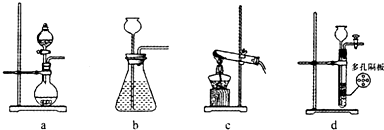
(2)SO2为重要的含硫化合物,是形成酸雨的主要污染物之一。在实验室中,若用70%的硫酸溶液和亚硫酸钠粉末反应制取二氧化硫,并要求方便控制反应速率,可选用如图所示气体发生装置中的_______(填下列序号字母)。
(3)为研究SO2的性质,如图在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条火准)。
下列有关说法正确的是___________
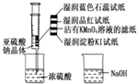
| A.蓝色石蕊试纸先变红后褪色 |
| B.湿润的品红试纸、蘸有KMnO4溶液的滤纸均褪色证明SO2具有漂白性 |
| C.湿润的淀粉KI-试纸未变蓝说明SO2的氧化性强于I2 |
| D.NaOH溶液可用于除去实验中多余的SO2 |
(4)一定温度下,在密闭容器中SO2与O2反应生成1molSO3气体时,放出akJ热量。
①该温度下SO2与O2反应的热化学方程式为__________________________。
②已知:2NO(g)+O2(g)═2NO2(g) △H=" -b" kJ•mol-1 (a>b>0)
则反应NO2(g)+SO2(g)═SO3(g)+NO(g) 的△H=________________。
Ⅱ.硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需要处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中的二氧化硫的含量,采用以下方案:
实验步骤如下图流程图所示:

(1)步骤①中反应的离子方程式为____________________________。
(2)步骤②中Ba(OH)2是否足量的判断方法是____________________________。
Ⅲ.工业生产中产生的SO2、NO直接排放将对大气造成严重污染。利用电化学原理吸收SO2和NO,同时获得 Na2S2O4和 NH4NO3产品的工艺流程图如下(Ce为铈元素).

请回答下列问题.
(1)装置Ⅱ中的反应在酸性条件下进行,写出NO被氧化为NO2-的离子方程式__________。
(2)装置Ⅲ的作用之一是再生Ce4+,其原理如图所示;
图中A为电源的______(填“正”或“负”)极.右侧反应室中发生的主要电极反应式为__________。
(3)已知进人装置Ⅳ的溶液中NO2-的浓度为 0.75mol/L,要使 1m3该溶液中的NO2-完全转化为 NH4NO3,需至少向装置Ⅳ中通入标准状况下的 O2的体积为_______L。
某小组同学为比较酸性条件下NO3-、SO42-、Fe3+的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
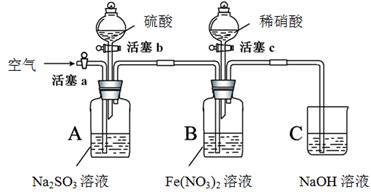
实验记录如下:
| |
实验操作 |
实验现象 |
| I |
打开活塞c,将过量稀HNO3加入装置B中,关闭活塞c |
B中浅绿色溶液立即变为深棕色;一段时间后,溶液最终变为黄色。 |
| II |
用注射器取出少量B装置中的溶液,加入KSCN溶液 |
溶液变为红色。 |
| III |
打开活塞b,向A装置中加入足量硫酸,关闭活塞b |
A中产生气体;B中有气泡,液面上有少量红棕色气体生成。 |
| IV |
一段时间后,用注射器取出少量B装置中的溶液,…… |
…… |
| V |
打开活塞a,通入一段时间空气 |
———— |
请回答下列问题:
(1)保存Fe(NO3)2溶液时,常加入铁粉,目的是(用化学方程式表示)________。
(2)实验I中,发生反应的离子方程式是________。
(3)资料表明,Fe2+能与NO结合形成深棕色物质[Fe(NO)]2+: Fe2+ + NO [Fe(NO)]2+
[Fe(NO)]2+
用平衡移动原理解释实验I中溶液由深棕色变为黄色的原因是________________________。
(4)分析实验现象,同学们得出了结论。则:
① 实验IV的后续操作是________________,观察到的现象是________________。
② 由实验得出的结论是_______________________。
(5)实验反思
① 实验操作V的目的是_______________________________________。
② 实验操作III,开始时B中溶液的颜色并无明显变化,此时溶液中发生反应的离子方程式是________。
③ 有同学认为装置中的空气会干扰实验结论的得出,应在实验前通一段时间的氮气。你是否同意该看法,理由是________________________________________。
乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4•xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x的值。通过查阅资料和网络查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
学习小组的同学设计了滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000 mol·L-1的KMnO4标准溶液进行滴定,达到终点时消耗了10.00mL。
请回答下列问题:
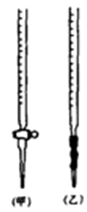
(1)滴定时,将酸性KMnO4标准液装在如图中的 (填“甲”或“乙”)滴定管中。
(2)本实验滴定达到终点的标志是 。
(3)通过上述数据,求得x= 。讨论:
①若滴定终点时俯视滴定管,则由此测得的x值会 (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 。
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:

(1)SO2气体还原Fe3+生成的还原产物是 (填离子符号),参加反应的SO2和Fe3+的物质的量之比是 。
(2)下列实验方案适用于在实验室制取所需SO2的是 (双选,填序号)。
| A.Na2SO3溶液与HNO3 | B.Na2SO3固体与浓硫酸 |
| C.固体硫在纯氧中燃烧 | D.铜与热浓H2SO4 |
(3)装置C的作用是 。
(4)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有 (双选,填序号)。
A 蒸发皿 B 石棉网 C 漏斗 D 烧杯 E 玻璃棒 F 坩埚
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的一个是 ,原因是 。
(6)上述装置中能表明I-的还原性弱于SO2的现象是 。
某学生为了测定部分变质的Na2SO3样品的纯度。按右图所示称取一定量的Na2SO3样品放入A装置的烧瓶中,滴入足量的H2SO4至完全反应;然后,将B中完全反应后的溶液与足量的BaCl2溶液反应,过滤、洗涤、干燥,得白色沉淀23.3g。回答下列问题: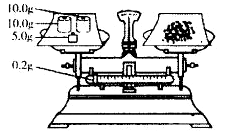

(1)写出A装置中玻璃仪器的名称:酒精灯、______________、______________。
(2)实验开始时,应先点燃__________________处酒精灯(填装置字母)。
(3) 写出D中反应的化学方程式__________________________________。
(4)实验开始后,写出B中反应的离子方程式_______________________。
(5)C中的现象是____________________,E装置的作用是__________________。
(6)原样品中Na2SO3的纯度为_________________(精确到0.1%)。按题给装置和操作进行实验,若装置连接和实验操作均无任何问题,该学生测得的Na2SO3的纯度__________(填“偏高”、“偏低”或“无影响”)。
Ⅰ.(1)实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。理论上硫酸和硝酸的物质的量之比最佳为:_____________
(2)实验上,即使铜粉、硫酸及硝酸都比较纯,制得的CuSO4·5H2O中还是可能存在杂质,除去这种杂质的实验操作称为___________。
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案甲:以空气为氧化剂。将铜粉反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案乙:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应.向反应液中加少量FeSO4,即发生反应,生成硫酸铜.反应完全后,加M调节pH,铁元素全部沉淀(一般认为铁离子的浓度下降到10-5 mol•L-1,就认为沉淀完全)然后过滤、浓缩、结晶。
请回答下列问题:
①方案甲中,钢丝应在__________中反复灼烧;(填仪器名称)
方案丙:将钢丝放到一定量的稀硫酸中,加入适量的H2O2,并控制温度在50℃~60℃,持续反应1h,也能获得硫酸铜。请回答下列问题:
②反应时温度必须控制在50℃~60℃,温度不宜过高的主要原因是______________________;
Ⅱ.用湿法制磷酸的副产品氟硅酸(H2SiF6)生成无水氟化氢的工艺如下图所示: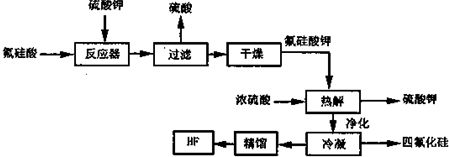
已知氟硅酸钾(K2SiF6)微酸性,有吸湿性,微溶于水,不溶于醇.在热水中水解成氟化钾、氟化氢及硅酸.
(1)写出反应器中的化学方程式:____________________________。
(2)在洗涤氟硅酸钾(K2SiF6)时常用酒精洗涤而不是用水,其目的是:_________________。
(3)该流程中哪些物质可以循环使用:____________________________。
(4)为了测定无水氟化氢的纯度,取标况下的气体产物2.24L,测得质量为3.1g,试解释,为什么标况下2.24L产物的质量远远大于2.0g,____________________________。
乙醛能与银氨溶液反应析出银,如果条件控制适当,析出的银会均匀分布在试管上,形成光亮的银镜,这个反应叫银镜反应。银镜的光亮程度与反应条件有关,某课外活动小组同学在课外活动中对乙醛的银镜反应进行了探究。
Ⅰ.探究银镜反应的最佳实验条件的部分实验数据如下表:
| 实验序号 |
银氨溶液 |
乙醛的量/滴 |
水浴温度/℃ |
反应混合液的pH |
出现银镜时间 |
| 1 |
1 |
3 |
65 |
11 |
5 |
| 2 |
1 |
3 |
45 |
11 |
6.5 |
| 3 |
1 |
5 |
65 |
11 |
4 |
| 4 |
1 |
3 |
30 |
11 |
9 |
| 5 |
1 |
3 |
50 |
11 |
6 |
| 6 |
1 |
5 |
80 |
11 |
3 |
请回答下列问题:
(1)若只进行实验1和实验3,其探究目的是____________________。
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11
时,出现银镜的时间范围是____________________。
(3)进一步实验还可探索_______________对出现银镜快慢的影响。
Ⅱ.探究对废液的回收处理:银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环
境,且造成银资源的浪费.通过查找资料,已知从银氨溶液中提取银的一种实验流程如下: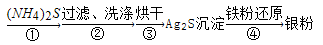
(4)操作④的方法是把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉,反应的化学方程 式为__________________。过滤需要用到的玻璃仪器有_______(填编号)。要得到纯净的Ag2S沉淀,需要洗涤沉淀,实验室过滤器中洗涤沉淀的操作是:________________________。

(5)根据电化原理也可Ag2S转变为Ag,方法是:在铝质容器中加入食盐溶液,再将表面生成Ag2S的银器浸入该溶液中,一段时间后发现黑色会褪去。
①该装置中银器为______极。
②该装置总反应的化学方程式为___________________________。
化学反应速率是描述化学反应进行快慢程度的物理量。下面是某同学测定化学反应速率并探究其影响因素的实验。
Ⅰ.测定化学反应速率
该同学利用如图装置测定化学反应速率。(已知:S2O32-+2H+===H2O+S↓+SO2↑)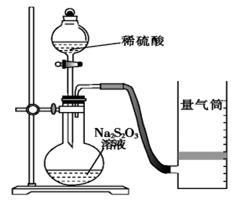
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是_____________________;除如图装置所示的实验用品、仪器外,还需要的一件实验仪器是______________。
(2)若在2 min时收集到224 mL(已折算成标准状况)气体,可计算出该2 min内H+的反应速率,而该测定值比实际值偏小,其原因是________________________。
(3)试简述测定该反应的化学反应速率的其他方法:__________________(写一种)。
Ⅱ.为探讨化学反应速率的影响因素,设计的实验方案如下表。
(已知 I2+2S2O32-===S4O62-+2I-,其中Na2S2O3溶液均足量)
| 实验序号 |
体积V/mL |
时间/s |
|||
| Na2S2O3溶液 |
淀粉溶液 |
碘水 |
水 |
||
| ① |
10.0 |
2.0 |
4.0 |
0.0 |
t1 |
| ② |
8.0 |
2.0 |
4.0 |
2.0 |
t2 |
| ③ |
6.0 |
2.0 |
4.0 |
Vx |
t3 |
(4)该实验进行的目的是_____________淀粉溶液的作用是____________。表中Vx==_______mL,比较t1、t2、t3大小,试推测该实验结论:___________________________
某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
 2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
2NO2 + 2NaOH = NaNO2 + NaNO3 + H2O
2NO2 + Na2CO3 = NaNO2 + NaNO3 + CO2
于是提出猜想,NO2和碱性的NaHCO3溶液也能发生类似反应。该小组利用如图所示装置,使NO2和NaHCO3溶液充分反应后,获得溶液X。

(1)Cu与浓硝酸反应的现象是_______________________。
(2)该小组同学为了对猜想进行探究,进行如下讨论和实验。
①甲同学认为,可通过检验X中是否存在NO3—的方法验证猜想。但经讨论后认为不可行,你认为其原因是 。
②乙同学在X中加入少量K2Cr2O7溶液,结果溶液褪色,则证明X中含有NaNO2。根据以上信息,写出NO2与NaHCO3溶液反应的离子方程式_________________ 。
(3)已知在酸性条件下NO2— 能将I— 氧化为I2。你认为能否用KI淀粉溶液检验X中存在NaNO2: ___________(填“能”或“不能”),原因是____________________________。
(4)已知5NO2— + 2MnO4—+6H+= 5NO3—+ 2Mn2+ +3H2O。称取a g KMnO4固体,加蒸馏水和少量稀硫酸溶解,配成250 mL溶液。移取20.00mL X于锥形瓶,用所配的酸性KMnO4溶液进行滴定,消耗b mL KMnO4溶液。滴点终点的现象是 ,则X中NaNO2的浓度是______________(用含a、b的式子表示)。
利用右图装置测定中和热的实验步骤如下:
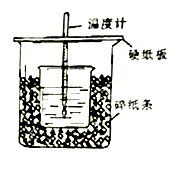
①量取50mL 0.25mol•L-1硫酸倒入小烧杯中,测量温度;
②量取50mL 0.55mol•L-1NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后,测量混合液温度。请回答:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________;
(2)NaOH溶液稍过量的原因_____________;
(3)加入NaOH溶液的正确操作是______(填字母).
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是_______;
(5)设溶液的密度均为1g/cm3,中和后溶液的比热容c=4.18J/(g•℃),请根据实验数据写出该反应的热化学方程式 _____________;
| 温度 实验次数 |
起始温度t1/℃ |
终止温度 t2/℃ |
温度差平均值(t2-t1)/℃ |
||
| H2SO4 |
NaOH |
平均值 |
|||
| 1 |
25.0 |
25.2 |
25.1 |
28.5 |
|
| 2 |
24.9 |
25.1 |
25.0 |
28.3 |
|
| 3 |
25.5 |
26.5 |
26 |
31.8 |
|
| 4 |
25.6 |
25.4 |
25.5 |
29.0 |
(6)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母) _______
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(7)______(填“能”或“不能”)用Ba(OH)2代替氢氧化钠溶液和稀硫酸反应;若将含0.5molH2SO4的 浓硫酸与含1molNaOH的溶液混合,放出的热量________(填“小于”、“等于”或“大于”)57.3kJ。原因是_______________________。
半导体生产中常需要控制掺杂,以保证控制电阻率,三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如图所示:(部分夹持装置略去)
已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;②PCl3遇水会强烈水解生 成 H3PO3和HC1;③PCl3遇O2会生成P0Cl3,P0Cl3溶于PCl3;④PCl3、POCl3的熔沸点见下表:
| 物质 |
熔点/℃ |
沸点/℃ |
| PCl3 |
-112 |
75.5 |
| POCl3 |
2 |
105.3 |
请回答下列问题:
(1)A装置中制氯气的离子方程式为______________;
(2)F中碱石灰的作用是_____________、_________________________;
(3)实验时,检査装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是______________;
(4)粗产品中常含有POCl3、PCl5等.加入黄磷加热除去PCl5后.通过_________填实验操作名称),即可得到较纯净的PCl3;
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为______________;
(6)通过下面方法可测定产品中PCl3的质量分数
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000mol•L-1碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol•L-1的Na2S2O3,溶液滴定
③重复②、③操作,平均消耗Na2S2O3,溶液8.40ml
已知:H3PO3+H2O+I2═H3PO4+2HI,I2+2Na2S2O3═2NaI+Na2S4O6,假设测定过程中没有其他反应.根据上述数据,该产品中PC13的质量分数为_________。
硫代硫酸钠(Na2S2O3·5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。它易溶于水,难溶于乙醇,加热、遇酸均易分解.工业上常用亚硫酸钠法、硫化碱法等制备.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图1: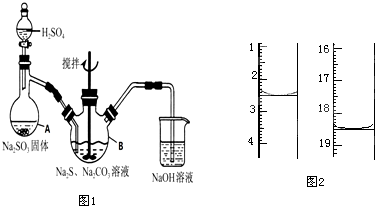
实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的SO2气体较均匀地
通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸.
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体.
③趁热过滤,将滤液加热浓缩,冷却析出Na2S2O3•5H2O.
④再经过滤、洗涤、干燥,得到所需的产品.
(1)写出仪器A的名称_____________,步骤④中洗涤时,为了减少产物的损失用的试剂可以是
___________;
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液pH<7,请用离子方程式解释原因___________;
(3)写出三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式___________;
(4)最后得到的产品中可能含有Na2SO4杂质.请设计实验检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论___________;
(5)测定产品纯度 准确称取1.00g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol•L-1碘的标准溶液滴定.反应原理为2S2O32-+I2═S4O62-+2I-.滴定起始和终点的液面位置如图2:则消耗碘的标准溶液体积为___________ mL,产品的纯度为___________。
高锰酸钾(KMnO4)是常用的氧化剂,工业上以软锰矿(主要成分是MnO2)为,原料制备高锰酸钾晶体。中间产物为锰酸钾(K2MnO4)下图1是实验室模拟制备的操作流程:

相关资料:
①物质溶解度
| 物质 |
KMnO4 |
K2CO3 |
KHCO3 |
K2SO4 |
CH3COOK |
| 20℃溶解度 |
6.4 |
111 |
33.7 |
11.1 |
217 |
②锰酸钾[K2MnO4]外观性状:墨绿色结晶.其水溶液呈深绿色,这是锰酸根(MnO42-)的特征颜色.
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42-会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是______________;实验中用 铁坩埚煅烧暴露在空气中的固体混合物发生反应的化学方程式为______________。
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式______________;其中氧化还原反应中氧化剂和还原剂的质量比为________。
(3)由于CO2的通人量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中_______,得到的产品纯度更高.
A.醋酸 B.浓盐酸 C.稀硫酸
(4)工业上一般采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式______________;传统工艺采用无膜电解法由于副反应发生,Mn元素利用率和电流效率都会偏低.有同学联想到离子交换膜法电解饱和食盐水提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图2).图中A口加入的溶液最好为_________;使用阳离子交换膜可以提高Mn元素利用率的原因为______________。
试题篮
()