在下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A.D为金属单质,其他为化合物。试推断:
(1)写出下列物质的化学式:A:________B:________G:________
(2)写出下列反应的化学方程式或离子方程式:
C→F的离子方程式________________________________________
C→E的化学方程式________________________________________
H→I的化学方程式________________________________________
有机物M和乙炔可合成3-羟基丁酸,3-羟基丁酸可以生成一种生物降解塑料PHB和通过两步反应生成另一种高聚物C:
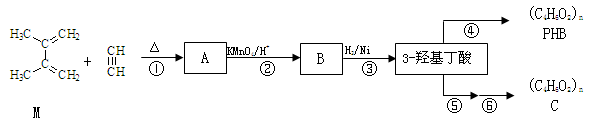
已知:i. 步骤②只有一种产物;C的结构中不含有甲基
ii. 
iii. 
41.M的系统命名为 。反应②反应类型 ,反应⑤的反应试剂及条件 。
42.写出B、C结构简式:B ,C 。
43.写出反应④化学方程式 ;
44.满足下列条件的B的同分异构体的结构简式为 。
a. 能发生银镜反应 b.分子中仅含2种化学环境不同的氢原子
45.理论上A也可以由1,3-丁二烯与烃F来合成,则F的结构简式为 。
[化学—物质结构与性质]
A、B、C、D、E五种元素中,A原子核外的M层中只有两对成对电子,B原子核外的L层电子数是K层的两倍,C是地壳内含量(质量分数)最高的元素,D的核电荷数是A与C的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)A、B的元素符号依次为_____________、_______________;
(2)AC2与BC2分子的立体结构分别是______和______,相同条件下两者在水中的溶解度较大的是______(写分子式),理由是___________________________________________;
(3)D的核外电子排布式为________________________,在形成化合物时它的最高化合价为__________。
下表为元素周期表前三周期的一部分。
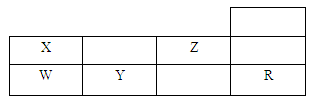
(1)X的氢化物与W的氢化物的比较稳定的是: (填化学式)。(2)从下列选项中选出X的基态原子的最外层原子轨道表示式 ,另一原子轨道表示式不能作为基态原子的轨道表示式是因为它不符合 。(填序号)。
A.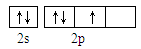 |
B.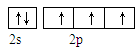 |
| C.泡利原理 | D.洪特规则 |
(3)以上五种元素中, 元素的电负性最大(填元素符号)。
无机推断题组(一题多变题组)
已知:A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。

(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出E中含有的化学键类型 ;已知1molA与水反应放出283.5kJ的热量,试写出A与水反应的热化学反应方程式 ;
(2)若A 为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则单质A与H2O反应的离子方程式 。
(3)若A 为淡黄色粉末,回答下列问题:
①1molA与足量的H2O充分反应时,转移电子总数为 。
②若X为非金属单质,通常为黑色粉末,写出D的结构式 ;
(4)若A为氧化物,X是Fe,溶液D加入KSCN溶液变红。
①A与H2O反应的离子方程式 。
②请用离子方程式表示D盐的净水原理 。
下表为周期表的一部分,其中的编号代表对应的元素。
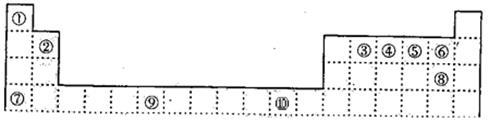
(1)⑨是 (填元素名称)。
(2)画出⑥的离子结构示意图 。
(3)元素⑦和⑧形成的化合物属于 晶体,它比NaF的熔点 (填“高”或“低”)。
(4)在 ①~⑩ 元素的最高价氧化物的水化物碱性最强的是 ,酸性最强的是 。(填化学式)
(5)⑧形成的最高价氧化物化学式是 。
(6)元素⑩在元素周期表的 族,其原子的外围电子排布式 。
(7)第四周期所有元素的基态原子中,4p轨道半充满的是 (请填元素符号,下同),4s轨道半充满的是 。
针对下面9种元素,完成以下各小题
| 周期 |
IA |
ⅡA |
ⅢA |
ⅣA |
|
ⅥA |
ⅦA |
O |
| 2 |
|
|
|
① |
② |
③ |
|
|
| 3 |
④ |
⑤ |
⑥ |
⑦ |
|
⑧ |
⑨ |
|
(1)单质为有色气体的元素是___________(填名称)。
(2)③④⑤简单离子的半径由大到小的顺序为_____________(填离子符号)。
(3)元素②的单质的电子式为________________。
(4)最高价氧化物对应的水化物酸性最强的是___________________。(填化学式)
(5)④和⑥的最高价氧化物对应的水化物反应的离子方程式为_____________。
(6)⑦的单质的用途正确的是___________。
A.光导纤维 B.太阳能电池 C.普通玻璃 D.计算机芯片
(7)元素①和⑦非金属性较强的是__________,写出一个能表示二者非金属性强弱关系的化学方程式为:______________。
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl﹣、SO42﹣、和NO3﹣的分离.实验过程如下图所示:
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X:_______,沉淀A:_______。
(2)上述实验流程中加入过量的Na2CO3的目的是_______。
(3)按此实验方案得到的溶液3中肯定含有_______(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的_______,之后若要获得固体NaNO3需进行的实验操作是_______(填操作名称)。
(1)有A、B、C、D四种均含有铝元素的化合物,它们之间存在如下的反应关系:
① A+NaOH=D+H2O ② B=A+H2O ③C+NaOH(适量)="B+NaCl" ④C+D+H2O=B+NaCl
则A是 、C是 (填化学式)
(2)实验室用加热二氧化锰和浓盐酸制氯气,离子方程式
若生成标况下2.24 L Cl2,则被氧化的HCl的物质的量为 。
化合物 是鞘氨醇激酶抑制剂,其合成路线如图:
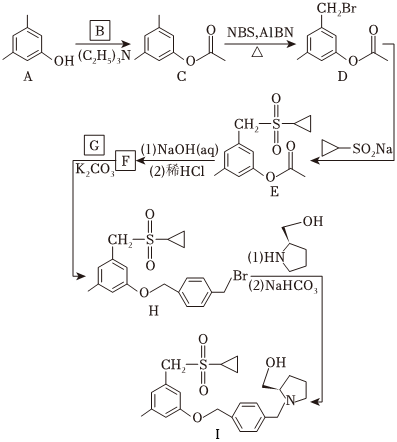
(1)化合物A的酸性比环己醇的_____(填“强”或“弱”或“无差别”)。
(2)B的分子式为 ,可由乙酸与 反应合成,B的结构简式为_____。
(3)A→C中加入 是为了结构反应中产生的_____(填化学式)。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:_____。碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使 酸性 溶液褪色;加热条件下,铜催化另一产物与氧气反应,所得有机产物的核磁共振氢谱中只有 个峰。
(5)G的分子式为 ,F→H的反应类型为_____。
(6)写出以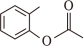 、
、 和
为原料制备
和
为原料制备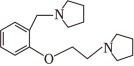 的合成路线流程图(须用
和
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(须用
和
,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
下列各物质转化关系如图所示,A是一种高熔点固体,D是一种红棕色固体。
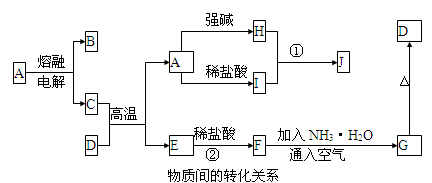
根据上述一系列关系回答:
(1)填写物质的化学式:B , G 。
(2)写出D物质中金属元素基态原子的核外电子排布图 。
(3)写出下列反应的离子方程式:
①H溶液和I溶液混合生成J___________ 。
②E和盐酸反应 。
(4)在电解熔融状态A的过程中,当电路中通过1mol电子时,阳极上产生的气体体积为 L。(标准状况下)
高分子材料E和含扑热息痛高分子药物的合成流程如下图所示:
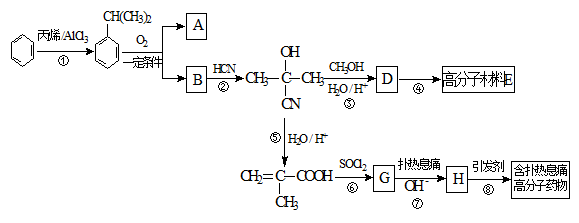
已知:I.含扑热息痛高分子药物的结构为: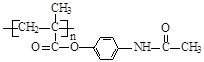 。
。
II.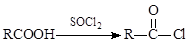
III.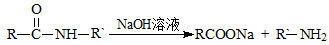
试回答下列问题:
(1)①的反应类型为____________,G的分子式为____________。
(2)若1 mol  可转化为1 mol A和1 mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式_____________。
可转化为1 mol A和1 mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式_____________。
(3)反应②为加成反应,则B的结构简式为__________;扑热息痛的结构简式为______________。
(4)写出含扑热息痛高分子药物与足量氢氧化钠溶液发生反应的化学方程式 。
(5)D蒸气密度是相同状态下甲烷密度的6.25倍,D中各元素的质量分数分别为碳60%,氢8%,氧32% 。D有多种同分异构体,其中属于链状酯类,且能发生银镜反应的同分异构体有_______种(考虑顺反异构)。
现有A、B、C、D、E五种原子序数依次增加的短周期元素,其中A的最低负价和最高正价代数和为零,且A2常温下为气态,B与其他元素形成的化合物种类最多,C与E可形成EC2和EC3两种物质,D是短周期最活泼的金属元素,用化学用语回答下列问题:
(1)D离子结构示意图_________________,B在元素周期表的位置_______________;
(2)A与C形成含18个电子的化合物的电子式是_______________;
(3)C与D形成的一种化合物颜色为淡黄色,其阴阳离子个数比为_____________,含有的化学键类型为___________;
(4)C、D、E的常见离子的离子半径由大到小的顺序__________________;
(5)B、E两元素得电子能力B________E(填“>”或“<”),试写出证明该结论的一个化学方程式_______;
(6)工业上常用氨水吸收尾气中的EC2,离子方程式为_______________________。
右图A→E是五种中学化学常见物质其中A、B、C、D常温下都是气体,B 为红棕色,A为气体单质。
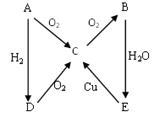
(1)写出化学式:B C
(2)实验室制备D实验中所用的干燥剂是: 。
(3)B与H2O反应,该反应的氧化剂和还原剂的物质的量之比为 。
(4)A与O2的反应方程式: ;D与O2的反应方程式:
;A与H2的反应方程式: 。
A、B、C、D、E为原子序数依次增大的短周期元素。A、C处于同一主族,C、D、E处于同一周期,E原子的最外层电子数是A、B、C原子最外层电子数之和,D是地壳中含量最高的金属元素;A、B组成的常见气体甲能使湿润的红色石蕊试纸变蓝;E的单质与甲反应能生成B的单质,同时生成两种水溶液均呈酸性的化合物乙和丙(该反应中氧化产物只有一种),25℃时0.1 mol/L的乙溶液pH>l;D的单质既能与C元素最高价氧化物的水化物的溶液反应生成盐丁,也能与丙的水溶液反应生成盐。
请回答下列问题:
(1)甲的化学式为 ;B单质的电子式为 。
(2)D元素的名称是 。
(3)写出丁溶液中通入过量二氧化碳时的离子方程式
(4)工业上利用A、B的单质合成甲(BA3):B2 (g)+3A2 (g)  2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=______________。
2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=______________。
(5)E的单质与甲反应生成的乙和丙的物质的量之比为2:4.反应中被氧化的物质与被还原的物质的物质的量之比为 。
试题篮
()