我国重载铁路加氢站今年投入了商业运营。机车加注 氢气做燃料,若用电解水的方法制取这些氢气,理论上需要水的质量是多少?(写出计算过程)
某兴趣小组用如图所示装置制取 ,加热混合物至不再产生气体后,称量试管中剩余固体的质量为 。请计算:
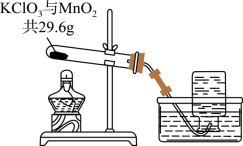
(1)生成 的质量为_____ 。
(2)剩余固体中 的质量分数。
化学兴趣小组对钢铁厂生产出来的某产品(只含铁和碳)产生好奇:它是生铁还是钢?该小组取 样品,加入到盛有足量稀硫酸的烧杯中,实验得到氢气的质量如下表。(提示:生铁的含碳量为 ,钢的含碳量为 )
|
时间/min |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
质量/g |
0 |
0.06 |
0.1 |
0.15 |
0.18 |
0.20 |
0.22 |
0.20 |
0.20 |
(1)分析判断:表格中第_____分钟的数据不合理;
(2)根据表格中合理的数据,在给出的坐标系上,画出氢气质量与时间的关系曲线:
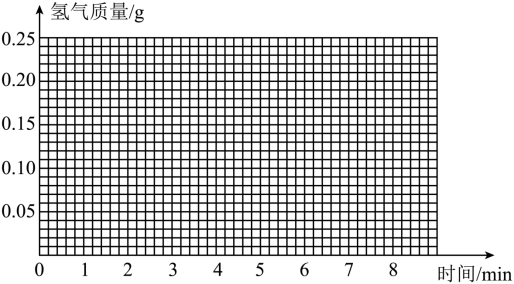
(3)通过计算判断该产品是生铁还是钢?(写出计算过程,计算结果保留到 )
根据
 反应原理,工业上可用来冶炼铁。现用
含四氧化三铁为
的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
反应原理,工业上可用来冶炼铁。现用
含四氧化三铁为
的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁质量是多少?
(2)理论上可炼出含铁 的生铁的质量是多少?
(1)用 克溶质质量分数为 的过氧化氢溶液配制成溶质质量分数为 的过氧化氢溶液,需加水_____克。
(2)取 克某过氧化氢溶液放入锥形瓶中并加入一定量的二氧化锰,用电子秤测其质量,不同时间电子秤的读数如下表所示。试计算该过氧化氢溶液的溶质质量分数(不考虑 逸出,写出计算过程,结果保留到 )。
|
反应时间/ |
|
|
|
|
|
|
|
|
锥形瓶+瓶内物质的总质量/ |
|
|
|
|
|
|
|
游览活动即将结束,化学精灵请同学们乘坐氢燃料汽车回家。氢气作为燃料具有热值高、无污染的优点,但是制备成本高,储存有难度。若用废旧黄铜( 合金)和稀硫酸为原料制备氢气,测得实验数据如图,请计算:
(1)该废旧黄铜中锌的质量为_____ 。
(2)实验中生成氢气的质量。

夏日鱼塘缺氧,鱼类“浮头”现象多发。养鱼师傅向鱼塘中撒入一种主要成分为过氧化钙( )的白色固体(杂质不与水反应),以解决鱼塘缺氧问题。
(1)影响气体溶解度的外界因素有_____。过氧化钙与水反应生成氢氧化钙和氧气,氢氧化钙对水产养殖颇有益处,列举一项__________。
(2)将 质量分数为 的白色固体 撒入鱼塘,产生氧气(密度为 )的体积是多少?(写出计算过程)
铝碳酸镁咀嚼片(主要成分是 )可治疗胃酸过多症,反应原理可用化学方程式表示为 。某化学兴趣小组使用如图所示装置,对该咀嚼片中的铝碳酸镁含量进行测定。先取足量稀盐酸于烧杯中,再向其中加入 片铝碳酸镁咀嚼片,开始计时,并将电子天平的读数记录在下表中。已知 的相对分子质量为 。请计算:
|
时间( ) |
|
|
|
|
|
|
|
|
|
读数( ) |
|
|
|
|
|
|
|
|
(1)生成二氧化碳_____ 。
(2)每片该咀嚼片中铝碳酸镁的含量为多少(计算结果保留到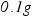 )?
)?

铝碳酸镁咀嚼片(主要成分是 )可治疗胃酸过多症,反应原理可用化学方程式表示为 。某化学兴趣小组使用如图所示装置,对该咀嚼片中的铝碳酸镁含量进行测定。先取足量稀盐酸于烧杯中,再向其中加入 片铝碳酸镁咀嚼片,开始计时,并将电子天平的读数记录在下表中。已知 的相对分子质量为 。请计算:
|
时间( ) |
|
|
|
|
|
|
|
|
|
读数( ) |
|
|
|
|
|
|
|
|
(1)生成二氧化碳____ 。
(2)每片该咀嚼片中铝碳酸镁的含量为多少(计算结果保留到 )?

钙在冶炼工业中具有重要的作用。可采用电解熔融氯化钙的方法生产钙,反应的化学方程式为
 。若制得
,计算参加反应的
的质量(写出计算过程及结果)。
。若制得
,计算参加反应的
的质量(写出计算过程及结果)。
纯碱可用于造纸、玻璃生产等领域。纯碱产品中常含有少量的氯化钠杂质,某兴趣小组的同学为测定某品牌纯碱样品中碳酸钠的质量分数,设计了如图方案并进行实验。
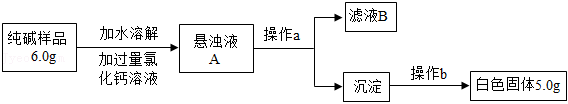
(1)滤液 中含有的阳离子有 __________(填化学符号)。
(2)若沉淀不经过操作 会使测定结果 _____(填“偏大”、“偏小”或“无影响”)。
(3)根据以上数据计算该样品中碳酸钠的质量分数(写出计算过程,结果精确至 )。
化肥对提高农作物的产量具有重要作用,尿素 是最常见的化肥之一。
(1)尿素属于_____(填标号)。
| A. |
氮肥 |
| B. |
磷肥 |
| C. |
钾肥 |
| D. |
复合肥 |
(2)尿素中氮元素的质量分数是_____ (结果保留到小数点后一位)。
(3)工业上生产尿素的反应为 。若生产 尿素,理论上需要氨气的质量是多少?(写出计算过程)

粮食安全是国家安全的重要基础,化肥对提高粮食产量有重要作用。尿素【
】是常用的氮肥之一,可促进植物茎、叶生长茂盛,叶色浓绿,提高植物蛋白质含量。已知:

(1)尿素中氮元素的质量分数为_____(结果精确到 )。
(2)巴中某农业合作社需要 吨尿素,请计算合成这些尿素需要 的质量是多少吨。(写出计算过程)
已知某种钾肥是 和 的混合物,为测定二者的质量比,在烧杯里放入一定质量的该钾肥样品,加入适量水,完全溶解后,再向其中加入 溶液至恰好完全反应,得到 溶质质量分数为 的 溶液,并生成 白色沉淀。
请计算:
(1)该钾肥样品中钾元素的质量。
(2)该钾肥样品中 与 的质量比(用最简整数比表示)。
试题篮
()