小明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白,于是想探究该固体的成分。
【提出问题】 该淡黄色固体的化学成分是什么?
【查阅资料】
(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体。
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热。
【设计实验方案】
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象。
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象。
比较以上两方案,你认为的最佳方案是 ,理由是(从环保或操作角度分析) 。
【实验验证并得出结论】
小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH)。通过实验验证,确定该淡黄色粉末为过氧化钠。
小明想对生成的气体成分判断,他提出了以下两种假设:①该气体是CO ②该气体是O2
你认为上述假设哪个更合理 (填“①”或“②”)。
请设计一个实验,验证你的合理假设(写出简要操作步骤、实验现象和结论)。
| 操作步骤 |
实验现象 |
结论 |
| |
|
|
【分析】过氧化钠与水反应的文字表达式为 。
【计算】在过氧化钠(Na2O2)中,
①氧元素的化合价为 ;
②过氧化钠的相对分子质量为 ;
③ 过氧化钠中钠、氧元素的质量比为 ;
④78克过氧化钠与多少克二氧化碳中所含氧元素的质量相等?(列式计算)
某同学按如下步骤对三种未知金属展开探究:
(1)将它们编号为:X、Y、Z;
(2)取样,分别加入到CuSO4溶液中,发现X、Z表面出现红色物质而Y却没有;
(3)取X、Z大小相等的颗粒,分别加入到溶质质量分数相等的稀H2SO4中,发现X表面产生气泡的速度明显比Z快,则X、Y、Z的金属活动性由强到弱依次为
| A.X>Y>Z | B.Z>Y>X | C.X>Z>Y | D.Z>X>Y |
二氧化硫是造成酸雨的主要物质之一。小丽为探究二氧化硫能与水反应生成酸,设计了如下实验方案。
【实验设计】她先用紫色石蕊溶液将白色滤纸浸润,干燥后做成紫色的小花,然后按下列图示进行实验。观察到实验(Ⅰ)和(Ⅲ)中的小花变红,(Ⅱ)中的小花不变色。
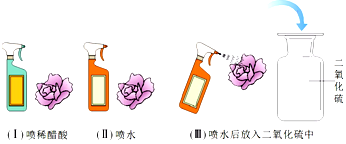
【评价反思】小虎对小丽的实验方案提出了质疑,他认为上述实验还不足以证明"二氧化硫和水反应生成了酸"。两位同学仔细讨论后认为还需补充如下一个实验,才能得出二氧化硫与水反应生成酸。
| 实验操作 |
实验现象 |
【拓展应用】二氧化硫也是实验室一种污染气体,常用碱液吸收。写出实验室用氢氧化钠溶液吸收二氧化硫的化学方程式:。
某化学兴趣小组设计四种实验方案来证明炭粉中是否含有氧化铜.其中可行的是:
| A.将固体高温加热,看是否有红色固体生成 |
| B.在样品中加稀硫酸,充分反应后,观察是否有固体剩余 |
| C.在样品中加水,是否有蓝色沉淀 |
| D.在样品中加硫酸,充分反应后,溶液是否呈蓝色 |
科学的假设与猜想是科学探究的先导和价值所在。在下列假设(猜想)引导下的探究肯定没有意义的选项是
| A.探究二氧化硫和水反应可能有硫酸生成 |
| B.探究钠与水的反应产生的气体可能是氢气 |
| C.探究镁条表面灰黑色的物质可能只是氧化镁 |
| D.探究铜在酒精灯火焰内灼烧时出现的黑色物质可能是炭黑 |
某无色气体可能含有CO2、CO、H2中的一种或几种。按下表中的步骤连续进行实验(假设每步反应均完全)。
资料:Ⅰ.相同条件下,等体积的气体含有相同数目的分子。
Ⅱ.白色的硫酸铜粉末遇水变蓝。
| 实验步骤 |
实验现象 |
| ①通过炽热的木炭,恢复到原温度 |
气体体积不变 |
| ②通过灼热的氧化铜 |
固体变为红色 |
| ③通过白色的硫酸铜粉末 |
粉末变为蓝色 |
| ④通入澄清的石灰水中 |
石灰水变浑浊 |
下列关于该气体的判断正确的是
A.一定含有CO2、CO和 H2 B.一定含有H2,一定不含CO2和CO
C.一定含有CO2和 H2,可能含有CO D.一定含有CO和 H2,一定不含CO2
探究小组用右图装置进行实验。胶头滴管和集气瓶中分别盛装某种物质,挤压胶头滴管向集气瓶中滴加适量液体后,能观察到气球变大的组合是
| 组合 |
胶头滴管 |
集气瓶 |
| A |
稀硫酸 |
Na2CO3 |
| B |
稀盐酸 |
Zn |
| C |
水 |
硝酸铵 |
| D |
浓硫酸 |
水 |
印刷铜制电路板的“腐蚀液”为FeCl3溶液。已知铜、铁均能与FeCl3溶液反应,反应方程式分别为:Cu+2FeCl3=2FeCl2+CuCl2,Fe+2FeCl3=3FeCl2。现将一包铜、铁的混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,关于烧杯中物质组成的说法正确的是
| A.溶液中一定含FeCl2,固体一定含铜 |
| B.溶液中一定含FeCl2,固体一定是铁和铜 |
| C.溶液中一定含FeCl3,固体一定是铁和铜 |
| D.溶液中一定含FeCl2、CuCl2,固体一定含铜 |
在实验探究过程中,如果有多种因素同时影响某一实验结果,当我们要探究其中的一种因素时,就要使其他因素保持不变,以探究此种因素对实验结果的影响。下表是稀硫酸与某金属反应的实验数据:
通过分析上述数据得出的结论不正确的是:
| A.对比实验1和2、4和5,可得出固体反应物的表面积越大,反应越快的结论。 |
| B.表明反应物的溶质质量分数越大,反应越快的只有2和5 |
| C.表明反应体系的温度越高,反应越快的只有6和7。 |
| D.实验中的所有反应,反应前后溶液的温度变化值相近(约15℃),推测其原因是:所有反应中,金属质量和硫酸体积均相等,且金属完全反应,产生热量相等,所以溶液温度变化值相近。 |
某同学对下列4个实验都设计了两种方案,其中方案一、方案二都合理的是
| 选项 |
A |
B |
C |
D |
| 实验目的 |
除去炭粉中少量的氧化铜 |
证明长期露置的氢氧化钠溶液已变质 |
鉴别硫酸钾和硝酸铵 |
证明稀醋酸溶液呈酸性 |
| 方案一 |
加稀硫酸 |
加足量稀盐酸 |
看外观 |
加无色酚酞试液 |
| 方案二 |
高温灼烧 |
加澄清石灰水 |
加熟石灰研磨闻气味 |
加氢氧化钠溶液 |
某校化学兴趣小组设计用下图所示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。[查阅资料]:①Fe与浓H2SO4反应,加热,有SO2生成;②C与浓H2SO4反应,加热,有CO2和SO2生成;③SO2可使澄清石灰水变浑浊;④SO2可使品红溶液的红色褪去,而CO2不能;⑤SO2可与酸性KMnO4溶液反应使其褪色,而CO2不能;⑥碱石灰的主要成分为NaOH和CaO。
[实验探究]称取mg铁碳合金,加入过量浓硫酸,加热待A中不再逸出气体时,停止加热,拆下E装置并称重,E增重bg。下列对实验结果分析正确的是
| A.B装置作用是为了除去反应中生成的SO2 |
| B.依据实验数据计算得出铁的质量分数为(3b-11m)/11m |
| C.装置内的CO2难以赶尽,E质量偏小,导致铁的质量分数偏小 |
| D.SO2未被酸性KMnO4除尽也可能会引起铁的质量分数偏小 |
下列实验的实验现象与实验结论都正确的是()
| 实验操作 |
实验现象 |
实验结论 |
|
| A |
将一根未打磨的铝条放入 硫酸铜溶液中 |
无紫红色固体析出 |
铝不如铜活泼 |
| B |
将带火星的木条伸入氧气中 |
木条复燃 |
氧气能支持燃烧 |
| C |
将
通过灼热的氧化铜 |
黑色氧化铜变成红色 |
具有可燃性 |
| D |
将氢氧化钠固体加入水中 |
溶液温度升高 |
该反应放热 |
兴趣是最好的老师,化学实验深深地吸引了我们每一个同学。下列装置或操作能达到实验目的的是( )
| A.稀释浓硫酸 | B.探究燃烧的三个条件 |
| C.测定空气中氧气的含量 | D.探究C02的性质 |
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大。则滴管和烧瓶中所用试剂可能是 
| A.甲: 稀硫酸和铜片乙: 水和CO |
| B.甲:双氧水,二氧化锰,乙: NaOH溶液和CO2 |
| C.甲: NaOH溶液和CO2乙: NaOH溶液和H2 |
| D.甲:H2O和NH3乙:稀盐酸和大理石 |
试题篮
()