人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属.硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如图的实验流程(有些反应的部分反应物和生成物已省略).

查阅资料发现:常温下,单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应(Si+2NaOH+H 2O═Na 2SiO 3+2H 2↑).
根据以上信息,回答下列问题:
(1)固体A的成分为 ,E的化学式为 ;
(2)滤液B中的金属阳离子为 ;
(3)在过滤操作时,若发现滤液浑浊,应 ;
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式 .
现有一包黑色粉末,可能由铁粉、碳粉和氧化铜中的一种或几种物质组成。某化学兴趣小组对黑色粉末的成分进行探究并提炼其中的某种金属。
【提出问题】黑色粉末是什么?
【初步实验】把少许黑色粉末与足量稀盐酸混合,立即产生气泡,且反应后无固体剩余。
【查阅资料】①常温下碳的化学性质不活泼,不与稀盐酸发生反应。
②氢气具有还原性,可用于冶金工业。
【初步结论】黑色粉末可能是 或 。
同学们为了进一步确定黑色粉末的成分,进行了如下实验。
【设计实验】如图所示实验
【实验现象】试管底部有红色物质生成。
【实验结论】黑色粉末是 ,试管中发生反应的化学方程式为 。
【拓展探究】为了提炼其中的某种金属,同学们取相同质量的黑色粉末,设计了如下两种实验方案:

(1)步骤2和步骤3中物质分离的操作名称是 。
(2)方案中的五个步骤,其中不能说明铁的活动性比铜强的步骤是 。方案中属于复分解反应的化学方程式为 。
(3)D、E是同一种溶质形成的溶液,但不能判断其中溶质质量大小,理由是 。
(4)请你分析哪种方案合理并说明理由 。

莫凡同学完成镁与稀盐酸反应的实验后,观察到有灰白色沉淀生成的"异常"现象,引起了他的兴趣,并进行了以下探究。
【初步探究】出现灰白色沉淀是否为偶然现象。
【实验Ⅰ】向4份相同体积与浓度的稀盐酸中分别加入一定长度的某种镁带,现象如下:
| 实验组别 |
A |
B |
C |
D |
| 镁带长度 |
1cm |
2cm |
3cm |
4cm |
| 沉淀量 |
无沉淀生成 |
少量沉淀 |
沉淀较多 |
沉淀很多 |
【实验结论】并非偶然,据表分析, 是实验出现"异常"的主要因素。
【再次探究】该沉淀的成分
【猜想假设】猜想1:Mg;猜想2:MgCl 2
【实验Ⅱ】
| 序号 |
实验操作 |
实验现象 |
实验结论 |
| ① |
取1g样品,加入足量 ,振荡 |
未见气泡 |
猜想1错误 |
| ② |
取1g样品,加入5mL蒸馏水,振荡 |
沉淀未溶解 |
猜想2错误 |
| ③ |
取1g MgCl 2固体,加5mL蒸馏水,振荡 |
固体全部溶解 |
【交流讨论】
(1)莫凡同学做出猜想Ⅰ的依据是他认为反应物Mg过量,作出猜想2的依据是他认为生成物MgCl 2 。
(2)从实验设计的角度讲,实验③的作用是 。
【深入探究】该沉淀的物质组成
【查阅资料】
灰白色沉淀的成分为碱式氯化镁,它存在多种组成,化学式可表示为Mg x(OH) yCl z•nH 2O[即每份Mg x(OH) yCl z结合了n份H 2O],它受热分解可产生氧化镁、氯化氢和水。
【实验Ⅲ】
洗去沉淀表面杂质并室温晾干,取其7.07g,用如图装置(夹持仪器未画出)按照正确的操作步骤进行实验,待反应停止后,测得硬质玻璃管中剩余固体质量为4.00g,装置B的质量增加了2.34g。
【问题讨论】
(1)反应停止后,应继续通入N 2一段时间,目的是 。
(2)该沉淀中,镁、氯的离子个数比n(Mg 2+):n(Cl ﹣)= 。
(3)若沉淀Mg x(OH) yCl z•nH 2O中,n=5,则X、Y、Z的数值依次为 。

新能源的开发和利用是人类社会可持续发展的重要课题。氢、氧燃料电池是一种新型能源,所用的氧气从空气中获得的方法是 。空气中的氧气按体积计算,大约是空气总体积的 。氢气可用天然气制取,这种方法制取的氢气中往往混有二氧化碳和一氧化碳,为了证明混合气体中H 2、CO 2、CO三种气体都存在,一化学实验小组设计以下实验。

【阅读提示】
①实验前,装置内的空气已排尽。
②实验过程中的尾气已处理。
③无水硫酸铜是白色粉末,吸水后变蓝。
请回答下列问题。
(1)A装置的作用是 。
(2)C装置中的实验现象是 。
(3)E装置中盛放的试剂应该是 ,该装置中发生反应的化学方程式为 。
(4)证明氢气存在的实验现象是 。
(5)另一小组同学利用上述实验装置(把其中的E装置换成装有碱石灰的干燥管),仿照上述实验过程,通过定量的方法确定一氧化碳存在,记录实验数据如下:
(注:反应生成的水蒸气被D装置完全吸收,不考虑其他水蒸气对实验结果的影响)
| 实验前C装置玻璃管内固体总质量/g |
m 1 |
| 实验后C装置玻璃管内固体总质量/g |
m 2 |
| 实验前D装置总质量/g |
n 1 |
| 实验后D装置总质量/g |
n 2 |
利用如表数据,计算出能证明CO存在的质量关系是 。(用m 1、m 2、n 1、n 2表示)
某同学为探究碳在氧气中不完全燃烧的气体产物中,既可能有一氧化碳,又可能有二氧化碳,他设计了如图所示实验:
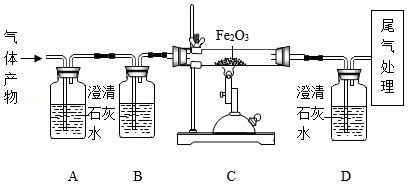
(1)装置A的作用是 。
(2)实验过程中,观察到装置C中玻璃管里的红棕色粉末逐渐变黑,说明原气体产物中含有一氧化碳,反应的化学方程式是 。
(3)通过观察装置D中澄清石灰水变浑浊,也能验证原气体产物中一氧化碳的存在,则装置B中应选择的试剂是 。
A.足量的氢氧化钠浓溶液
B.浓硫酸
C.水
(4)写出尾气处理的一种方法: 。
膨松剂是一种食品添加剂,某研究小组对膨松剂进行了如下探究
【趣味实验】
实验1:和面.向20g面粉中加入10mL水,制得的面团编为1号;向20g面粉中加入10mL水,再加入2g膨松剂M,制得的面团编为2号.
实验2:发面.将和好的2个面团放入微波炉中加热,几分钟后,取出面团,发现1号面团无明显胀大,2号面团明显胀大且手感比较松软.
【提出问题】膨松剂M的成分是什么?
【提出假设】
假设1:M是NH4HCO3;
假设2:M是NaHCO3;
假设3:M是NH4HCO3和NaHCO3
【实验探究1】
序号 |
实验步骤 |
实验现象 |
实验结论 |
① |
取少量M于试管中,加热一段时间 |
无刺激性气味 试管内壁有水珠 试管内有固体剩余 |
假设 成立 假设 不成立 |
【提出新问题】实验①试管中剩余固体是什么?
【实验探究2】
实验②:将实验①所得固体继续加热,无明显现象.冷却,向试管中加水,固体全部溶解,将所得溶液分为2份;向其中1份溶液中滴加稀盐酸,有气泡生成,将生成的气体通入澄清石灰水,有白色沉淀;向另1份溶液中滴加足量氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液不变红.
【得出结论】
实验①试管中剩余固体是 (填化学式)
【反思提高】
(1)NH4HCO3受热分解的化学方程式是 .
(2)受热稳定性:Na2CO3 (填“>”“=”或“<”)NaHCO3.
【拓展应用】
某品牌复配膨松剂N的配料为:磷酸二氢钙、碳酸氢钠和玉米淀粉,N遇水会发生如下反应:Ca(H2PO4)2+2NaHCO3═CaHPO4↓+Na2HPO4+2CO2↑+2H2O;利用N和面和发面(加热)时,面团都会胀大.下列叙述正确的是 (填序号)
a.常温下的溶解度:Na2HPO4>CaHPO4
b.碳酸氢钠在水溶液中遇到酸性物质能产生气体
c.根据上述反应,产生0.22gCO2至少需要NaHCO3的质量为0.42g.
钠盐种类较多,在实验室里,钠盐通常都摆放在同一药品柜中,小华所在的化学兴趣小组在整理药品柜时,发现某种试剂瓶外壁两边贴上了新旧两个标签,分别是"Na 2SO 4溶液"、"Na 2CO 3溶液",小华认为其原因是:Na 2CO 3溶液的试剂瓶混入了Na 2SO 4溶液,并加贴了新标签.该兴趣小组对溶液的成分进行了探究.请你完成以下探究过程,并将①~⑤处的答案填入答题卡相应位置.
【提出问题】
【提出猜想】猜想Ⅰ:溶质仅为Na 2SO 4;
猜想Ⅱ:溶质仅为Na 2CO 3;
猜想Ⅲ:溶质为Na 2SO 4和Na 2CO 3.
【实验探究】
| 实验操作 |
实验现象 |
实验结论 |
| 1.取少量样品于一只洁净试管中,加入足量稀硫酸 |
|
猜想Ⅰ不成立 |
| 2. ,向其中加入过量的BaCl 2溶液,过滤,向所得沉淀中加入足量稀硝酸 |
先产生白色沉淀;加入硝酸溶液后,有气泡产生,沉淀部分溶解 |
猜想 成立 |
【问题讨论】试写出加入BaCl 2溶液后,生成不溶于硝酸的白色沉淀的化学方程式 .
(一)请结合下列实验装置,回答问题:

(1)以高锰酸钾为原料、利用A装置制取氧气的化学方程式为 。
(2)用石灰石和稀盐酸制取并收集二氧化碳,选用的装置为 (填字母)。
(3)与集气瓶配套使用的玻璃片一般一面为光滑面,另一面为磨砂面,收集气体时用玻璃片的 盖好集气瓶(填"光滑面"或"磨砂面")。
(二)题中制取CO 2后残留的废液收集在学校实验室的废液缸中。某化学课外小组的同学想探究废液中溶质的成分,请我们共同参与探究并回答下列问题:
(1)[查阅资料]CaCl 2溶液呈中性。
(2)[提出问题]废液中的溶质是什么物质?
(3)[作出猜想]猜想一:废液中的溶质只有CaCl 2。
猜想二:废液中的溶质有CaCl 2和 (填化学式)。
(4)【实验与结论】①甲同学取少量CaCl 2溶液和废液分别加入到2支试管中,并向其中分别滴加无色酚酞溶液做对比实验,结果两试管中溶液均无色,于是甲同学认为猜想一是正确的。
②你认为甲同学的实验 (填"能"或"不能")证明猜想是正确的,理由是 。
③如果要证明猜想一是正确的,你做对比实验时选择加入的试剂是 ,实验时装有废液的试管中可能观察到的现象是 。
市售的"自热米饭"带有一个发热包,遇水后可迅速升温至150℃,保温时间达3小时,能将生米做成熟饭。梧州市某中学化学兴趣小组对发热包非常感兴趣,进行了以下探究。
【查阅资料】
(1)发热包主要由生石灰、铁粉、镁粉、铝粉、炭粉、氯化钠中的若干种组成。
(2)氢氧化镁和氢氧化铝均为不溶于水的白色固体,但后者可溶于NaOH溶液。
【成分探究】取出某品牌的发热包内灰黑色的固体粉末,分成两份。
(1)小吴用磁铁靠近其中一份粉末,发现有黑色物质被磁铁吸引,证明粉末中含有 。用磁铁将该物质全部吸出后,剩余粉末为样品A。
(2)小周将另一份粉末加水溶解、过滤后,取部分滤液滴入酚酞试液,滤液变 色,证明原粉末中含生石灰;再向滤液中加入 ,看到白色沉淀生成,证明原粉末中含有氯化钠。
(3)除上述物质外,还可能存在镁粉、铝粉、炭粉,对此大家提出了以下几种猜想:
猜想一:只存在上述三种中的一种;
猜想二:上述三种同时存在;
猜想三:存在铝粉和炭粉;
猜想四:存在镁粉和铝粉;
猜想五: 。
【实验验证】小施用样品A进行实验,流程如下。向滤液B滴加氢氧化钠溶液时,他观察到开始时有白色沉淀生成,后来又全部消失,最后得到的是无色溶液E。
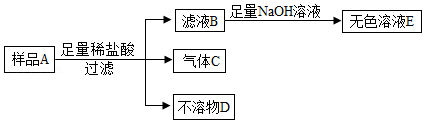
【实验结论】
不溶物D是 。
大家结合实验现象讨论后,认为猜想 正确,理由是 。
【原理探究】
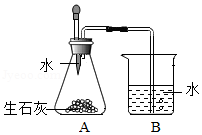
小吴利用如图装置证明发热包放热主要来自于生石灰与水的反应。加水后发现A中温度迅速升高,B中有气泡产生,该气体为 (填名称)。但温度很快下降,说明该反应很快结束,不能长时间保温。
【猜想】大家大胆猜测应该还有其他放热反应存在。
【实验验证】
同学们按资料介绍,用铁粉、炭粉和食盐水在锥形瓶中模拟铁的锈蚀实验,不久后发现锥形瓶外壁微烫,并持续较长时间。该现象很好地解释了发热包的保温机理。
【拓展活动】
在上述铁的锈蚀实验中未观察到红色的铁锈产生。老师告诉同学们,铁锈蚀时首先生成一种碱。请写出该反应的化学方程式 。
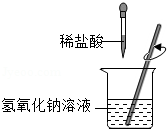
小红同学进行酸碱中和反应的实验(如图所示)。她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液颜色没有变化。于是她对烧杯中的溶液进行了以下探究:
(1)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应;②氢氧化钠有剩余;③盐酸过量。
小明同学却断定不可能"氢氧化钠有剩余",他的理由是: ;
(2)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写如表:
| 试验方法 |
可能观察到的现象 |
结论 |
| 将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中。 |
如果 |
则盐酸过量 |
| 如果 |
则盐酸与氢氧化钠恰好完全反应 |
(3)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的。你认为其中不正确的是 (填序号)。
A.生锈的铁钉 B.碳酸钠粉末 C.硫酸钠粉末 D.氢氧化铜
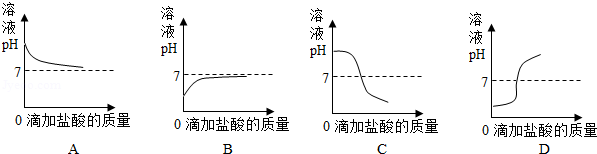
(4)如图曲线能够表示小红所做试验中溶液pH变化趋势的是 (填序号)。
碳酸钙、碱石灰(NaOH和CaO的混合物)等作为吸收剂可以对燃煤烟气进行脱硫处理,利用数字化实验可以来测定燃煤烟气中SO2的含量,得到如图所示的SO2含量与时间的关系曲线图
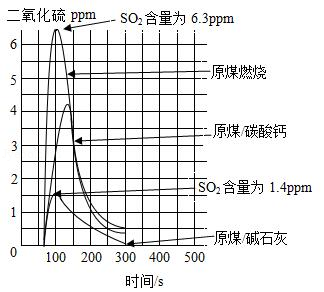
(1)由图可知,脱硫效率较高的吸收剂是 (填名称)。
(2)实验时,称取的3份原煤的质量要相等,其目的是 。
(3)利用碳酸钙吸收SO2转化为CaSO3,CaSO3与空气中O2反应转化为CaSO4.写出CaSO3转化为CaSO4的化学方程式 。
(4)利用碱石灰吸收SO2时,下列措施能使脱硫效率提高的是 (填序号)
a.将原煤与碱石灰粉碎,混合均匀
b.将碱石灰的用量适当增加
c.将时间300s变为500s
(5)利用碱石灰吸收1.28gSO2时,碱石灰中的NaOH、CaO与SO2反应转化为Na2SO3和CaSO3,则理论上反应消耗碱石灰的质量(m)范围是 。
化学学科实践活动课上,老师拿来一包粉末。它是由长期放置在空气中的铁粉和久置的碱石灰干燥剂混合而成,让同学们设计实验进行探究。
【提出问题】固体样品的成分是什么?
【查阅资料】(1)碱石灰干燥剂是CaO和NaOH的混合物。
(2)BaCl2溶液显中性。
【猜想与假设】固体样品中可能含有Fe、Fe2O3、CaO、NaOH、Ca(OH)2、Na2CO3和 等七种物质。
【进行实验】
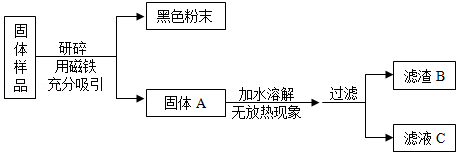
甲组同学对滤渣B的成分进行探究,记录如下:
实验操作 |
实验现象 |
实验结论及化学方程式 |
取少量滤渣B于试管中,加入足量稀盐酸,将生成的气体通入澄清的石灰水中 |
① ② |
结论:滤渣B中有Fe2O3,CaCO3.实验操作中反应的化学方程式为: (答出一个即可) |
乙组同学对滤液C的成分进行探究,记录如下:
实验操作 |
实验现象 |
实验结论 |
取少量滤液C于试管中,加入过量BaCl2溶液,静置,向上层清液中滴加无色酚酞试液,振荡 |
①有白色沉淀生成 ②酚酞试液由无色变成红色 |
滤液C中有 |
【解释与结论】(1)乙组同学实验中加入过量BaCl2溶液的目的是 。
(2)通过以上实验探究,该固体样品中能确定一定含有的成分是 。
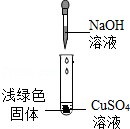
氢氧化钠和氢氧化钙是两种常见的碱,化学实验活动课上,同学们进行了如图所示的实验。

(1)实验一中,B试管中发生反应的化学方程式为 。
A、B两支试管中共同的实验现象是 。
(2)实验二中,C试管中有白色沉淀生成,该白色沉淀是 (填化学式)。D试管中无现象,为了探究通入二氧化碳后D试管中溶质的成分,同学们进行了如下探究。
【提出猜想】猜想1:溶质是NaOH。
猜想2:溶质是NaOH和Na2CO3
猜想3:溶质是Na2CO3
实验操作 |
实验现象 |
实验结论 |
①取D中少量溶液于试管中加入过量稀盐酸 |
|
猜想1不成立 |
②取D中少量溶液于另一试管中,加入过量的Ca(OH)2溶液,过滤,取滤液加入酚酞溶液 |
产生白色沉淀, 酚酞溶液变红 |
猜想2成立 |
【反思与评价】I.小军评价实验操作②中加入Ca(OH)2溶液不正确,理由是 。
若要验证猜想2成立,需将Ca(OH)2溶液换成 溶液。
Ⅱ在实验室中氢氧化钠固体密封保存的原因是 (用文字叙述)
兴趣小组实验中,将NaOH溶液滴入CuSO4溶液中,结果溶液中生成了浅绿色的固体。于是,他们对该浅绿色固体的成分进行探究。
【查阅资料】
①NaOH与CuSO4反应会生产Cu(OH)2,也会生成Cu4(OH)4SO4(碱式硫酸铜)。
②Cu(OH)2在80℃会分解生成CuO。
③Cu4(OH)4SO4不溶于水,能与酸反应,分解温度需300℃。
【猜想与假设】
猜想一:浅绿色固体为Cu(OH)2。
猜想二:浅绿色固体为 。
猜想三:浅绿色固体为Cu(OH)2和Cu4(OH)4SO4。
【获取事实与证据】
①取少量浅绿色固体放入试管中,加热至100℃,观察到黑色固体物质,说明浅绿色固体中存在 。
②另取少量浅绿色固体放入试管中,加入足量稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀,该白色沉淀是 。
【结论】整个实验证明猜想 正确。
同学们用大理石和稀盐酸制取二氧化碳后,小欣同学发现容器内液体是浑浊的,她很好奇,浑浊液体是什么?于是她和同学们一起将浑浊的液体过滤,得到滤液和固体,并对此展开了探究(溶解于水中的气体成分忽略不计)
【提出问题】滤液中的溶质以及过滤得到的固体的成分是什么?
【查阅资料】
①大理石中含有SiO2(不溶于水,且不与盐酸反应),可能含有少量的Fe2O3等。
②FeCl3溶液遇到硫氰化钾(KSCN)溶液能够很灵敏显现出红色。
【猜想验证】
Ⅰ经讨论,大家认为滤液中一定含有CaCl2,原因是 (用化学方程式表示)
Ⅱ小欣同学根据资料中大理石的成分,猜想滤液中可能含有少量 。
她取少量滤液于试管中,滴加硫氰化钾(KSCN)溶液,观察到滤液颜色无变化,由此得出的结论是 。
Ⅲ小雨又提出猜想,滤液中还可能含有 (填化学式)。请你和小雨一起验证他的猜想。
实验操作 |
实验现象 |
实验结论 |
取少量滤液于试管中,向其中滴加 。 |
溶液变成红色 |
小雨的猜想成立 |
Ⅳ根据小雨的验证结果,可知过滤得到的固体中含有 。
【得出结论】最终同学们确定了滤液中的溶质以及过滤得到的固体的成分。
试题篮
()