天然气是一种比较清洁的化石能源,主要成分为甲烷。现对甲烷的制取、性质、应用做以下研究,请回答相关问题。
[制取研究]
查阅资料得知:①通常状况下,甲烷是一种无色无味难溶于水的气体,密度比空气小;
②实验室中常用无水醋酸钠(CH3COONa)和碱石灰(发生反应的是其中的氢氧化钠)两种固体药品,研磨均匀混合,通过加热制取甲烷,同时还生成碳酸钠。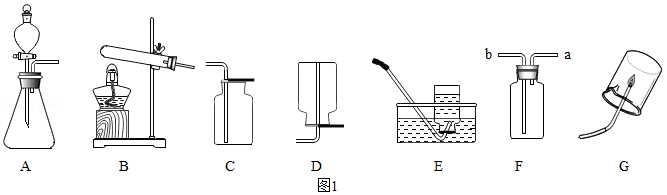
在实验室中:
(1)可用于制取甲烷的发生装置为 (填字母)。
(2)可用于收集甲烷的装置为 (填字母)。
(3)制取甲烷的化学方程式: 。
[性质研究]
用装置F收集了一瓶纯净的甲烷气体,在装置G中进行燃烧实验。
(4)可用水将F中气体压出,通入G中,那么,水应从 端(填“a”或“b”)注入。
(5)点燃后,烧杯内壁看到的现象是 ,同时还生成二氧化碳气体,请设计一个简单实验证明: 。
[应用研究]
尿素[CO(NH2)2]是一种常用氮肥。如图是利用甲烷制尿素的主要流程:

(6)设备I中分离出氮气和氧气的过程发生了 (填“物理变化”或“化学变化”)。
(7)设备Ⅲ中产生并分离开CO2和H2,进入下一设备使用,依据流程图可判断进入设备Ⅳ是 。
(8)设备V中的气体,可以循环利用的是 。
下列实验操作中能达到实验目的是( )
选项 |
实验目的 |
实验方案 |
A |
除去CuSO4溶液中的稀硫酸 |
加入过量铁粉,过滤 |
B |
除去CO2中的CO |
通入过量O2,点燃 |
C |
分离氧化铁粉末和碳粉的混合物 |
加入过量稀硫酸,过滤 |
D |
鉴别(NH4)2SO4固体和Na2SO4固体 |
分别加入熟石灰研磨,闻气味 |
A.AB.BC.CD.D
探究辨真伪
如图,用一次性塑料水杯盛鲜榨果汁时,常用带皮柠檬片作装饰。网上传言,柠檬皮可以溶解这种水杯中的聚苯乙烯,危害人体健康,这种说法是真的吗?为了查明真相,小东用泡沫饭盒(主要成分是聚苯乙烯)和柠檬皮进行探究。
(1)探究一:柠檬皮真的能溶解聚苯乙烯吗?
进行实验:
将柠檬皮研磨成酱,取一匙涂在泡沫饭盒上,2分钟后饭盒光滑的表面变得凹凸不平,5分钟后凹凸更加明显,10分钟后出现很多小孔。
结论与解释:
柠檬皮中含有柠檬烯(C 10H 16),柠檬烯是一种(填"有机"或"无机") 溶剂,可以溶解聚苯乙烯。
反思交流:
用一次性塑料水杯喝水时,聚苯乙烯不会进入人体,放了带皮柠檬片后,聚苯乙烯会被溶解而进入人体,这说明物质的溶解性与 有关。
一次性泡沫饭盒、一次性塑料水杯随意丢弃造成的环境问题被称为 ,果汁加工厂的大量柠檬皮被丢弃浪费,对此你有什么建议 。
(2)探究二:酸性、碱性溶液对柠檬皮溶解聚苯乙烯有影响吗?
实验用品:泡沫饭盒、柠檬皮酱、食醋、纯碱溶液、食盐水、水。
查阅资料:酸性溶液、碱性溶液均不能溶解聚苯乙烯。
进行实验:
①取一匙柠檬皮酱,与2mL水混合均匀后涂在泡沫饭盒上;
②取一匙柠檬皮酱,与2mL(写溶质化学式) 混合均匀后涂在泡沫饭盒上
③取一匙柠檬皮酱,与2mL(写溶质化学式) 混合均匀后涂在泡沫饭盒上。
该实验方案中采用了对照实验的方法,请指出其中的对照实验(填实验编号):第一组对照实验 ,第二组对照实验 。
5分钟后观察到三个泡沫饭盒表面的凹凸程度几乎相同,实验结论为 。
(3)探究三:温度对柠檬皮溶解聚苯乙烯有影响吗?
请将下表填写完整(柠檬皮中的成分在实验温度下性质稳定)。
| 实验步骤 |
实验现象 |
实验结论 |
|
|
|
温度越高,越不利于柠檬皮酱溶解聚苯乙烯 |
解释实验结论 。

控制变量是实验探究的重要方法。下列实验设计不能达到实验目的是( )
|
|
|
|
A、探究铁、镁金属活动性强弱 |
B、探究二氧化碳与水是否发生反应 |
C、探究不同溶剂中物质溶解性大小 |
D、探究温度对分子运动快慢的影响 |
A.AB.BC.CD.D
除去下列物质中少量的杂质,下列实验方案能达到实验目的的是( )
选项 |
物质(括号内为杂质) |
实验方案 |
A |
CO2(HCl) |
先通过NaOH溶液,再通过浓硫酸干燥 |
B |
CuCl2(FeCl2) |
先加足量水溶解,再加足量铁粉,过滤 |
C |
MnO2(KCl) |
先加足量水溶解,再过滤、洗涤、干燥 |
D |
NaCl(Na2CO3) |
先加足量水溶解,再加足量稀硫酸,蒸发结晶 |
A.AB.BC.CD.D
实验是进行科学探究的重要方式。请根据如图回答问题
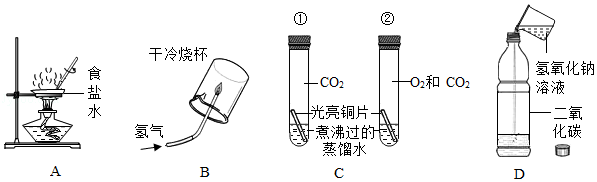
(1)用图A 所示装置蒸发食盐水时,玻璃棒的作用是 。
(2)用图B 所示装置在空气中点燃氢气,该反应的化学方程式为 。在点燃氢气等可燃性气体前,一定要先 。
(3)图 C 所示装置是探究铜生锈的部分实验,铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3].实验所用铜片形状、大小相同。一段时间后,试管①中铜片保持光亮,试管②中铜片出现绿色锈渍。对比试管①②的实验现象,得出的结论是 。
(4)甲同学用图D 所示装置探究二氧化碳能否与氢氧化钠发生反应。他向盛满二氧化碳的软塑料瓶中倒入 10%的氢氧化钠溶液 50mL,迅速拧紧瓶盖,振荡,观察到软塑料瓶变瘪。由此得出结论:二氧化碳能与氢氧化钠发生反应。乙同学认为甲同学的实验方案不严谨,理由是 。乙同学利用图D 所示装置,补做一个对比实验:将甲同学实验中的 换成 ,实验步骤与甲同学完全相同,对比两个实验的现象得出结论:二氧化碳能与氢氧化钠发生反应。
分离与提纯是获得物质的重要方法。下列实验操作不能达到实验目的是( )
实验目的 |
实验操作 |
|
A |
除去氢氧化钠溶液中的碳酸钠 |
加入过量的石灰水,充分反应后过滤 |
B |
除去氮气中的氧气 |
将气体缓缓通过足量的灼热铜网 |
C |
除去硫酸铜溶液中的硫酸 |
加入过量的氧化铜粉末,充分反应后过滤 |
D |
除去银粉中的锌粉 |
加入过量的稀盐酸,充分反应后过滤、洗涤、干燥 |
A.AB.BC.CD.D
鉴别物质是学习化学常用的方法之一。下列实验设计不能达到实验目的是( )
实验目的 |
实验设计 |
|
A |
鉴别空气、氧气、二氧化碳 |
燃着的木条分别伸入集气瓶 |
B |
区分氢氧化钠溶液和碳酸钠溶液 |
分别滴加无色酚酞溶液 |
C |
鉴别稀盐酸和稀硫酸 |
分别滴加BaCl2溶液 |
D |
鉴别稀盐酸和澄清石灰水 |
分别滴加紫色石蕊溶液 |
A.AB.BC.CD.D
根据你所学的化学知识和生活经验判断,下列做法不科学的是( )
A.用肥皂水区分硬水和软水
B.用钢刷、沙等擦洗铝制炊具
C.用燃烧的方法区分羊毛纤维和合成纤维
D.用相互刻画来比较黄铜片(铜锌合金)和铜片的硬度
下列实验操作不能达到实验目的是( )
选项 |
实验目的 |
实验操作 |
A |
除去CaCl2溶液中混有少量的HCl |
加入过量的氢氧化钙溶液 |
B |
除去CO2中少量的CO |
将混合气体通过灼热氧化铁粉末 |
C |
鉴别棉线和羊毛线 |
点燃后,闻气昧 |
D |
鉴别NaCl和NH4NO3固体 |
分别加少量水溶解 |
A.AB.BC.CD.D
下列实验操作不能达到实验目的是( )
选项 |
实验目的 |
实验操作 |
A |
除去CaCl2溶液中混有少量的HCl |
加入过量的氢氧化钙溶液 |
B |
除去CO2中少量的CO |
将混合气体通过灼热氧化铁粉末 |
C |
鉴别棉线和羊毛线 |
点燃后,闻气昧 |
D |
鉴别NaCl和NH4NO3固体 |
分别加少量水溶解 |
A.AB.BC.CD.D
生活中经常遇到一些“长相”类似的物质,如家庭制作食品用到的碳酸钠和碳酸氢钠。区分二者,比较简单的方法就是溶解度法(溶解度曲线见图)。
①小亮同学利用这种方法,在室温条件下设计了下面实验,请完善实验内容:
实验步骤 |
现象和结论 |
取两只试管,各倒入10g水,分别向两试管中逐步加入碳酸钠和碳酸氢钠固体,充分振荡、静置、观察现象。 |
至固体不能再溶解为止,其中,固体溶解量少的,所对应的物质是 (填化学式,下同),另一种物质是 |
②现有碳酸钠(2g)、碳酸氢钠(2g)和足量蒸馏水。请仿照上述①中的方法和实验设计,在室温条件下,调整变量、自主设计实验,进一步区分碳酸钠、碳酸氢钠两种物质:
实验步骤 |
现象和结论 |
|
|

为达到以下实验目的所设计的实验方案,不合理的是( )
实验目的 |
实验方案 |
|
A |
区别NaCl、Na2CO3两种溶液 |
滴加酚酞试剂 |
B |
鉴别某种溶液是FeCl2溶液 |
观察溶液颜色,滴加AgNO3溶液 |
C |
除去NaCl溶液中的Na2SO4 |
滴加适量BaCl2溶液,充分反应后,过滤 |
D |
分离出含有少量NaCl的KNO3 |
高温下配制KNO3的饱和溶液,趁热过滤 |
A.AB.BC.CD.D
为除去下列各物质中混有的少量杂质,采用的相应除杂方案正确的是( )
选项 |
物质 |
杂质 |
除杂方案 |
A |
铜粉 |
氧化铜 |
在空气中充分灼烧 |
B |
NaCl溶液 |
Na2CO3 |
加入适量稀硫酸 |
C |
H2 |
CO2 |
通过足量NaOH溶液,干燥 |
D |
CaCl2溶液 |
HCl |
加入过量铁粉,过滤 |
A.AB.BC.CD.D
某同学在做铝与酸反应的实验中发现了一个怪现象并记录于下表中,为了探究影响反应速率的因素及两者反应差异的原因,该同学做出了以下假设,你认为假设不合理的是( )
| 反应时间/min |
1 |
2 |
5 |
15 |
20 |
|
| 实验1 |
质量分数10%的盐酸 |
极少量气泡 |
较多气泡 |
大量气泡 |
反应剧烈 |
铝片耗尽 |
| 实验2 |
质量分数10%的硫酸 |
无明显现象 |
极少量气泡 |
|
|
|
| |
|
|
|
|
|
|
A.与盐酸反应开始产生气泡速率慢的原因:铝片表面有氧化膜
B.与盐酸反应产生气泡速率越来越快的原因:反应放热,溶液温度升高
C.两者反应差异的原因:盐酸中有H +,稀硫酸中没有H +
D.两者反应差异的原因:Cl ﹣对反应有促进作用,SO 4 2 ﹣对反应有阻得作用
试题篮
()