利用铜制备硫酸铜,设计了如下两个方案:
方案①:Cu+2H 2SO 4(浓) CuSO 4+SO 2↑+2H 2O
方案②:2Cu+O 2 2CuO CuO+H 2SO 4(稀)═CuSO 4+H 2O
对比上述两个方案,若硫酸足量且不考虑铜的损耗,下列说法不正确的是( )
| A. |
两个方案都需要加热 |
| B. |
方案①中可以用稀硫酸代替浓硫酸 |
| C. |
方案②中硫酸的利用率高,不会产生污染空气的二氧化硫 |
| D. |
等质量的铜分别按两个方案制备,可获得等质量的硫酸铜 |
除去下列物质中的少量杂质,如表实验方案能达到目的的是( )
| 选项 |
物质(括号内为杂质) |
实验方案 |
| A |
CuCl 2溶液(CuSO 4) |
加入过量的BaCl 2溶液,过滤 |
| B |
ZnCl 2溶液(CuCl 2) |
加入过量的锌粒,过滤 |
| C |
Fe 2O 3固体(CuO) |
加入足量稀盐酸,过滤 |
| D |
NaOH溶液[Ca(OH) 2] |
加入过量的Na 2CO 3溶液,过滤 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
分离与提纯是获得物质的重要方法。下列实验操作能达到实验目的的是( )
| |
实验目的 |
实验操作 |
| A |
除去二氧化碳气体中的一氧化碳 |
通入适量氧气,点燃 |
| B |
除去氯化钠固体中的泥沙 |
加入足量的水溶解,过滤,蒸发结晶 |
| C |
除去氯化钙溶液中的盐酸 |
加入过量的碳酸钙固体,充分反应后过滤 |
| D |
除去碳酸钠溶液中的氯化钠 |
加入过量的硝酸银溶液,过滤 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
下列实验方案正确的是( )
| 序号 |
实验目的 |
实验方案 |
| A |
鉴别CO 2和N 2 |
将燃着的木条分别伸入气体中,观察现象 |
| B |
鉴别NH 4Cl和KCl两种白色固体肥料 |
加入熟石灰研磨后闻气味 |
| C |
除去CO 2中混有的少量CO |
将气体通过灼热铜丝网 |
| D |
除去氢氧化钠溶液中的碳酸钠 |
加入过量的石灰水,充分反应后过滤 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
除去下列各物质中的杂质,所选用的试剂、操作方法不能达到目的的是( )
| 选项 |
物质 |
杂质(少量) |
选用试剂 |
操作方法 |
| A |
食盐 |
泥沙 |
水 |
加水溶解、过滤、蒸发结晶 |
| B |
FeCl 2 |
CuCl 2 |
Fe |
加入足量Fe粉,过滤 |
| C |
CaCl 2溶液 |
HCl |
Ca(OH) 2 |
加入过量Ca(OH) 2 |
| D |
N 2 |
O 2 |
Cu |
将混合气体通过足量灼热Cu粉 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
下列实验设计,不合理的是( )
| 选项 |
实验内容 |
实验过程 |
| A |
二氧化碳的溶解性 |
在充满二氧化碳气体的软塑料瓶中倒入 的水,拧紧瓶盖,振荡,塑料瓶迅速变瘪 |
| B |
浓盐酸的挥发性 |
打开盛有浓盐酸的细口瓶,瓶口有白雾产生 |
| C |
鉴定某溶液是氯化铁溶液 |
向溶液中滴加氢氧化钠溶液,有白色沉淀产生 |
| D |
硫酸铵是一种铵态氮肥 |
硫酸铵样品与熟石灰混合后研磨,有刺激性气味气体生成 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
下列实验设计不能达到实验目的的是( )
A.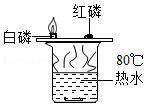 探究可燃物燃烧需达到着火点
探究可燃物燃烧需达到着火点
B.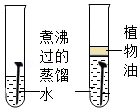 探究钢铁生锈需要氧气
探究钢铁生锈需要氧气
C.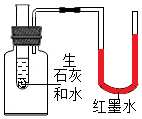 验证生石灰遇水放热
验证生石灰遇水放热
D.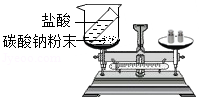 验证质量守恒定律
验证质量守恒定律
化学是一门以实验为基础的自然科学。根据所学知识回答以下问题:
(1)实验室制取二氧化碳,应选用以下药品①块状石灰石②碳酸钠粉末③稀盐酸④稀硫酸中的 (填序号)。现有大理石粉末和稀硫酸,你认为 (填“能”或“否”)用于实验室制取二氧化碳。
(2)实验室有如图1装置,根据要求回答问题:
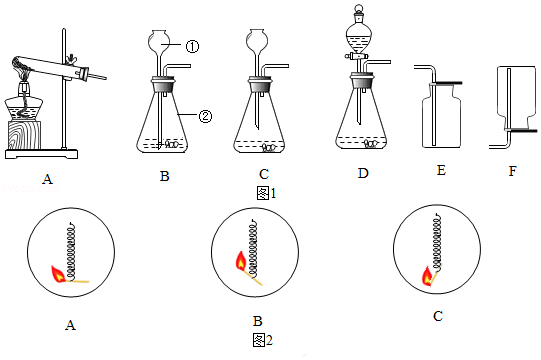
Ⅰ.写出标号仪器的名称① ,② 。
Ⅱ.对比装置B、C,有错误的是 (填序号,下同)。
Ⅲ.实验室要制取二氧化碳应选择的发生装置是 ,收集装置是 ;利用制取二氧化碳的发生和收集装置还能制取另外一种常见气体,利用此装置制取该气体的化学方程式是 。
Ⅳ.图2是同学们进行“铁丝在氧气中燃烧的性质实验”时的几种操作方式,更能提高实验成功率的方式是 (填序号)。
(3)有的同学完成上述实验后,提出“铁丝能否在二氧化碳中燃烧呢?”,他们设计了如下方案:(已知:在点燃的条件下,镁带能在二氧化碳中剧烈燃烧。)
方案①:将弯成螺旋状的细铁丝系上一根火柴,点燃火柴,待火柴快燃尽时,插入装有二氧化碳的集气瓶中,观察铁丝能否被引燃。
方案②:将弯成螺旋状的细铁丝系上一段镁带,点燃镁带,待镁带快燃尽时,插入装有二氧化碳的集气瓶中,观察铁丝能否被引燃。
你认为方案 (填①或②)更为科学,理由是 。
依据实验目的,下列设计的实验方案中不合理的是( )
| |
实验目的 |
实验方案 |
| A |
区分氧气和氮气 |
分别把燃着的木条伸入盛放气体的集气瓶中 |
| B |
鉴别氯化铵和氯化钾固体 |
分别与少量熟石灰混合后,研磨、闻气味 |
| C |
比较铜和银的金属活动性 |
把洁净的铜丝浸入硝酸银溶液中,观察现象 |
| D |
除去烧碱溶液中少量的碳酸钠 |
向溶液中滴加适量的氯化钙溶液,充分反应后过滤 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
除去下列物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是( )
选项 |
物质 |
杂质 |
除杂试剂及操作方法 |
A |
Cu |
Fe |
加入过量的CuCl2溶液,过滤、洗涤、干燥 |
B |
KCl |
MnO2 |
加入足量的水溶解,过滤、洗涤、干燥 |
C |
NaCl |
NaNO3 |
加入适量的硝酸银溶液至不再产生沉淀 |
D |
Cu |
C |
在空气中灼烧 |
A.AB.BC.CD.D
下列实验操作不能达到实验目的的是( )
选项 |
实验目的 |
实验操作 |
A |
除去FeSO4溶液中少量的CuSO4 |
加入过量锌粉,充分反应后过滤 |
B |
除去KCl固体中少量的MnO2 |
加水溶解,过滤,将滤液蒸发结晶 |
C |
除去铜粉中少量的镁粉 |
加入足量稀盐酸,充分反应后,过滤、洗涤、干燥 |
D |
除去N2中少量的O2 |
将气体缓缓通过灼热的铜网 |
A.AB.BC.CD.D
下列说法正确的是( )
A.用铁、铜和硫酸锌溶液可以验证锌、铁、铜三种金属的活动性强弱
B.Fe2+、Na+、Cl﹣、SO42﹣在pH=2的溶液中能大量共存,形成无色溶液
C.用燃着的木条可以鉴别N2、O2、CO2、H2四种气体
D.配制20g溶质质量分数为5%的氯化钠溶液,主要实验步骤是:计算、称量(量取)、溶解、装瓶贴标签
“化学链燃烧”是燃料不直接与空气接触的燃烧,是以载氧体在两个反应器之间的循环来实现燃料在较低温度下燃烧的过程。该过程具有无火焰、低污染、高效率等特点。氧化镍(NiO)作载氧体的“化学链燃烧”过程如图。与直接燃烧甲烷相比,对该技术的评价错误的是( )

A.反应更充分、能源利用率高
B.较安全,减少爆炸风险
C.消耗等质量甲烷,参加反应氧气较少
D.有利于分离和回收较纯净的二氧化碳
下列除去物质中少量的杂质,所选用的试剂和主要操作方法都正确的是( )
物质(括号内为杂质) |
所用试剂和主要操作方法 |
|
A |
ZnCl2溶液(CuCl2) |
加入足量的铁粉后过滤 |
B |
铜粉(木炭) |
在空气中灼烧 |
C |
CO2(CO) |
通入过量的氧气后点燃 |
D |
KCl(MnO2) |
加水充分溶解后过滤,蒸发结晶 |
A.AB.BC.CD.D
某学习小组将足量Zn条插入一定量的浓H2SO4中,发现Zn表面有大量气泡产生。(注:随着反应进行,硫酸浓度逐渐变小)
【提出问题】气体的成分是什么?
【猜想假设】猜想一:只有SO2
猜想二:只有H2
猜想三:
【查阅资料】(Ⅰ)SO2可以使品红溶液褪色
(Ⅱ)SO2可以和碱性溶液反应
(Ⅲ)H2+CuO Cu+H2O
【实验探究】用如图装置验证猜想(部分夹持仪器省略)
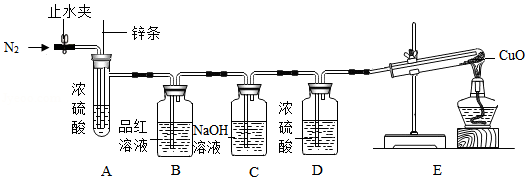
【方案设计】
主要实验步骤 |
主要现象 |
解释或结论 |
①打开止水夹,先通入一段时间N2 |
/ |
/ |
②关闭止水夹,将足量Zn条下放,浸入浓硫酸中,点燃E装置处酒精灯 |
B装置处品红溶液褪色 E装置处 |
猜想三成立 |
③结束实验 |
/ |
/ |
【表达交流】
(1)在步骤①中,通入N2的目的是: 。
(2)请你设计一个实验,用化学方法证明E装置中CuO未完全反应。
实验步骤 |
实验现象 |
结论 |
|
|
CuO未完全反应 |
【反思拓展】
(1)请你根据上述实验探究,补充Zn与浓硫酸反应的化学方程式
Zn+2H2SO4═ZnSO4+SO2↑+ 。
(2)已知Al与H2一样,在加热条件下能与CuO发生化学反应,请写出该反应的化学方程式 。
试题篮
()