甲、乙、丙三种固体物质的溶解度曲线如图所示,回答下列问题:
(1)曲线中P点含义是 。
(2)将t1℃时甲、乙、丙三种物质的饱和溶液分别升温到t2℃,此时三种物质的溶质质量分数从大到小的顺序是 。
(3)要想从乙物质饱和溶液中结晶得到大量乙物质的最好方法是 。
(4)t3℃时,若要在此温度下将组成在M点的甲溶液转化为N点的甲溶液,可采用的方法是 。

甲、乙、丙三种固体物质的溶解度曲线如图所示.据图回答问题:
(1)t3℃时,甲物质的溶解度是 .
(2)t2℃,把甲、乙、丙三种物质的饱和溶液降温到t1℃,溶质质量分数不变的是 .
(3)t2℃时,把20g乙物质加到50g水中,充分搅拌后所得溶液的质量是 g;若要让乙物质从它的饱和溶液中全部结晶析出,应采取的方法是 .

甲、乙两种固体物质的溶解度曲线如图所示,据图回答下列问题:
(1)乙物质的溶解度随温度的升高而 (填“增大”或“减小”).
(2)欲将t1℃甲物质的不饱和溶液变为该温度下的饱和溶液,可采取的方法: (任填一种).
(3)若甲物质中混有少量乙物质,可用 的方法提纯甲.
(4)等质量甲、乙两种物质分别配成t2℃时的饱和溶液,需要水的质量大小关系是
甲 乙(填“>”、“=”或“<”).

t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。
(1)烧杯②中的上层清液是否达到饱和状态? (填“是”“否”或“无法判断”);
(2)烧杯①中溶解的溶质是 (写名称或化学式);
(3)将t1℃时50g硝酸钾的饱和溶液稀释成10%的溶液,需加水 g;
(4)关于图1中烧杯内的物质,下列说法正确的是 。
A.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
B.蒸发一定量的水,两烧杯中都一定有固体析出
C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)

水是生命之源,也是一种重要的资源,日常生活、工农业生产和科学实验都离不开水,请回答下列问题:
(1)自然界的水一般都不是 (填"纯净物"或"混合物")含有较多可溶性钙、镁化合物的水叫硬水,生活中一般采用 的方法把硬水转化为软水.
(2)为了除去粗盐中的Ca 2+、Mg 2+、SO 4 2 ﹣等,可将粗盐溶于水,再进行如下操作:①加入适量稀盐酸 ②加入过量NaOH溶液 ③加入过量Na 2CO 3溶液 ④加入过量BaCl 2溶液 ⑤过滤 ⑥蒸发结晶,请将上述操作按合理顺序补充完整:② ⑥(填序号)
(3)如图是甲、乙两种固体物质(甲、乙均不含结晶水)在水中的溶解度曲线图.
①a点表示的意义是 .
②将t 1℃时甲、乙两物质的饱和溶液升温到t 2℃,其溶液中溶质质量分数大小关系是甲 __ 乙.(填">"、"<"或"=")
(4)化学实验中,水除了用于溶解物质外,你还知道水的用途有 (答一种即可)
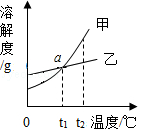
如图所示是甲、乙、丙三种固体物质的溶解度曲线。
(1)t 2℃时,甲、乙、丙三种物质的溶解度大小关系是 ;
(2)t 1℃时,50g水中加入30g的甲物质充分溶解后,可得到 g溶液;
(3)下列说法正确的是(填序号) 。
①t 1℃时,甲、丙两溶液的溶质质量分数一定相等
②t 3℃时,向100g20%甲的溶液中加100g水,充分搅拌,溶液的溶质质量分数为10%
③t 2℃时,升高丙溶液的温度,一定有晶体析出
④t 3℃时,用等质量的甲、乙、丙分别配制成三种物质的饱和溶液,所需溶剂的质量为甲<乙<丙。
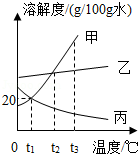
图中A、B、C分别表示三种不同的固体物质,其溶解度曲线如图所示。请回答下列问题:
(1)这三种物质的溶液中,适用于海水晒盐原理进行结晶提纯的是 。
(2)在t 2℃时,将质量均为25g的上述三种物质分别加入到100g水中,不能形成饱和溶液的是 。
(3)在t 2时,将足量的三种物质的饱和溶液各蒸发10g水后再冷却到t 2,它们析出晶体的质量分别为m(A)、m(B)和m(C),则三者的大小关系是 。
(4)将t 2℃的这三种物质的饱和溶液分别降温至t 1℃,所的溶液中溶质的质量分数分是ω(A)、ω(B)和ω(C),则三者的大小关系是 。
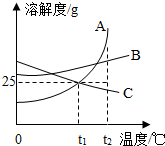
如图是甲,乙、丙三种固体物质的溶解度曲线,据图回答下列问题:
(1)P点的含义是 。
(2)t 2℃时,把50g甲中加入到200g水中充分搅拌,静置,形成的是 溶液(填"饱和"或"不饱和")。
(3)稍微加热丙的饱和溶液即出现浑浊现象,其原因是 。
(4)除去甲中混有的少量乙,步骤是:加水溶解、加热浓缩、 、过滤、洗涤、干燥。
(5)将t 2℃时等质量的甲、乙两物质的饱和溶液分别降温至t 1℃,对所得溶液的叙述正确的是 (填字母序号)
A.溶剂质量:甲>乙 B.析出晶体质量:甲>乙
C.溶质质量分数:甲<乙
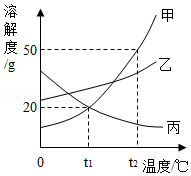
A、B、C三种固体物质的溶解度曲线如图所示。请回答下列问题。
(1)t 1℃时,溶解度相同的物质是 。
(2)若保持溶液质量不变,将C的饱和溶液变为不饱和溶液的方法是 。
(3)t 2℃时,把50gA放入50g水中,所得溶液中溶质和溶液的质量比为 (填最简整数比)。
(4)将t 2℃时等质量的A、B、C三种物质的饱和溶液,降温度温至t 1℃时所得溶液中溶剂质量由大到小顺序为 。

如图是A、B两种固体物质的溶解度曲线。
(1)当温度为 ℃时,A.B两种物质的溶解度相等。
(2)欲使饱和状态的B溶液变成不饱和溶液,可采用的一种方法是 。
(3)t2℃时,将30gA物质加入50g水中,充分溶解后,所得溶液中溶质与溶液的质量比是 。
(4)将t2℃等质量的A、B饱和溶液降温至t1℃,所得溶液的质量关系A B(选填“>”。“<”或“=”)

如图是甲、乙、丙三种固体物质的溶解度曲线图,请回答:
(1)t1℃时,甲物质的溶解度为 g。
(2)乙中有少量甲,提纯乙的方法是 。
(3)将t1℃时丙的饱和溶液升温到t2℃,观察到的现象是 。
(4)t2℃时,等质量甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液质量最小的是 。

t1℃时,向盛有10mL水的A、B两支试管中分别加入等质量的甲、乙两种可溶性固体,充分溶解后,观察到如图1所示的现象。请回答:
(1)t1℃时, 试管中的溶液一定是饱和溶液。
(2)图2中表示乙物质溶解度曲线的是 。
(3)若甲物质中混有少量的乙物质,提纯甲物质可以采取的方法是 。
(4)关于两支试管中的物质,下列说法不正确的是 。
A.t1℃时,试管A上层清液溶质质量分数<试管B中溶质质量分数
B.保持温度不变,向试管A中加入一定质量的水,则溶液中溶质质量分数一定变大
C.若温度升高到t2℃,两支试管中溶质质量分数一定相等(不考虑水分蒸发)
D.蒸发一定质量的水,两支试管中都一定有固体析出

水和溶液在生活、生产和化学实验中起着重要的作用。
(1)图甲是电解水的实验装置,切断装置中的电源,用 分别检验a、b两个玻璃管中产生的气体。
(2)图乙为A、B两种固体物质的溶解度曲线。据图回答:
①A、B两种物质的溶解度曲线交于P点,则P点表示的意义是 。
②若A中含有少量B,提纯A应采取的方法是 。
③有同学说:“t2℃时A物质饱和溶液中溶质的质量分数为70%。”这种说法对吗? (填“对”或“不对”)。

甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答。
(1)t2℃时,甲、乙、丙三种物质溶解度的大小关系为
(2)若甲中含有少量乙,提纯甲的方法是
(3)t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液中溶质的质量分数由小到大的顺序为 。
(4)t1℃时,溶质与溶剂质量比为2:11的甲溶液是 (填“饱和”或“不饱和”)溶液。

试题篮
()