下表是氯化钠和硝酸钾在不同温度下的溶解度。
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
|
溶解度/g |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
|
请回答下列问题:
(1)30℃时,硝酸钾的溶解度为 。
(2)使硝酸钾饱和溶液变为不饱和溶液,可采用的一种方法是 。
(3)50℃时,将80.0g一定质量分数的氯化钠溶液恒温蒸发,溶液的质量随蒸发水的质量变化关系如图所示,则a点溶液中溶质的质量为 。
(4)下列有关说法正确的是 (填标号)。
A.与氯化钠相比,硝酸钾的溶解度受温度影响较大
B.除去硝酸钾中混有的氯化钠,可采用降温结晶的方法
C.20℃时,向40.0g质量分数为25%的氯化钠溶液中加入10.0g氯化钠,可得到40%的氯化钠溶液
D.40℃时,分别向氯化钠和硝酸钾的饱和溶液中加入等量的水,所得溶液的质量分数可能相等

水和溶液在生产生活中用途广泛,请回答下列问题。
(1)自来水厂在净化水的过程中加入明矾的作用是 (填“杀菌”或“使悬浮物沉淀”);水能灭火的主要原因是 。
(2)生活中的下列物质属于溶液的是 (填字母序号,下同)。
A.白酒
B.豆浆
C.糖水
D.泥浆
(3)在2021年全国两会上,“蓝天、碧水、净土保卫战”成为聚焦重点,下列符合这一目标的是 。
A.生活污水任意排放
B.工业废水坚持达标排放
C.大量使用农药和化肥,增加农作物产量
D.农业上改漫灌为滴灌
(4)t2℃时,向盛有10mL水的Ⅰ、Ⅱ两支试管中分别加入等质量的甲、乙两种固体,充分溶解后,观察到如图1所示的现象。图2是甲、乙两种固体的溶解度曲线。请回答:
①图2中表示甲物质溶解度曲线的是 (填“a”或“b”)。
②根据图2分析,下列说法正确的是: 。
A.乙中混有少量甲,可用降温结晶法提纯乙
B.等质量甲、乙饱和溶液由t2℃降温至t1℃,所得溶液溶质质量分数相等
C.升温可使甲的饱和溶液变为不饱和溶液
D.t1℃时,将20g甲物质加入50g水中充分溶解,得到70g溶液

甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,如图所示,下列说法正确的是( )

A.三种物质的溶解度都随温度的升高而增大
B.P点表示t2℃时甲、丙两物质的溶解度相等
C.t1℃时,乙物质的饱和溶液溶质质量分数为30%
D.甲中含有少量乙,可采用蒸发结晶的方法提纯甲
K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如图:
温度/℃ |
20 |
30 |
50 |
60 |
80 |
|
溶解度/g |
K2CO3 |
110 |
114 |
121 |
126 |
139 |
KNO3 |
31.6 |
45.8 |
85.5 |
110 |
169 |
|
(1)图1中能表示K2CO3溶解度曲线的是 (填“甲”或“乙”)。
(2)在20℃时,将20g的KNO3加入到50g的水中,充分搅拌,得到溶液的质量为 g。
(3)在t℃时,K2CO3饱和溶液的溶质质量分数(w1)和KNO3饱和溶液的溶质质量分数(w2)的大小关系:w1 w2(填“>”、“=”或“<”)。
(4)在不改变溶液质量的情况下,要使一定量接近饱和的KNO3溶液变为饱和溶液的方法是: 。

图中是a、b、c三种物质的溶解度曲线,回答下列问题。
(1)P点的含义: 。
(2)在t3℃时,将120g a物质加入到200g水中,充分溶解后所得到的溶液质量为 g。
(3)b中混有少量a,提纯b的方法是 (选填“蒸发结晶”或“降温结晶”)。
(4)分别将t3℃时a、b的饱和溶液降温到t2℃,析出晶体的质量大小关系为 (选填一个序号)。
①a>b
②a<b
③a=b
④均有可能

如图为A、B、C三种固体物质的溶解度曲线,根据图回答下列问题:
(1)10℃时,A、B、C三种物质中溶解度最大的是 。
(2)若A中含有少量B时,可用 的方法提纯A。
(3)将等质量的A、B、C饱和溶液由50℃降温到20℃时,所得溶液中溶质质量由大到小的顺序为 。
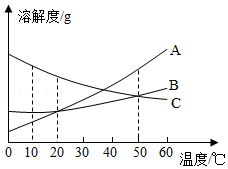
本题有甲、乙两图,图甲为硝酸钾和氯化铵的溶解度曲线,图乙为兴趣小组进行的实验,R物质是硝酸钾或氯化铵中的一种。

关于图乙中烧杯内的物质,下列说法正确的是( )
A.R 物质是氯化铵
B.溶液的溶质质量分数是烧杯①小于烧杯②
C.若使烧杯③中的固体溶解,只能采用加水的方法
D.烧杯①②③中,只有烧杯③中上层清液是饱和溶液
Ⅰ.溶液在生产、生活中起着十分重要的作用。请回答(1)﹣(2)题。
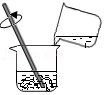
(1)如图,在木块上滴几滴水,将装有某种固体的大烧杯放置于木块上,向大烧杯中加水进搅拌,结果木块上的水结冰了,则大烧杯内的固体可能是 。
| A. |
氯化钠 |
B. |
硝酸铵 |
| C. |
氢氧化钠 |
D. |
蔗糖 |
(2)用汽油或加了洗涤剂的水都能除去衣服上的油污,两者去油污的原理分别是 。
| A. |
乳化、乳化 |
B. |
乳化、溶解 |
| C. |
溶解、乳化 |
D. |
溶解、溶解 |
Ⅱ.如图是甲、乙、丙三种固体物质的溶解度曲线。请回答(3)(4)题。
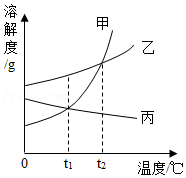
(3)现有t 1℃时甲乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t 2℃,所得溶液中溶质质量分数大小关系是 。
| A. |
甲=乙>丙 |
B. |
乙>甲=丙 |
| C. |
乙>甲>丙 |
D. |
甲>乙>丙 |
(4)为了将近饱和的丙溶液变为饱和溶液,可采用的方法有 (有2﹣3个选项符合题意)。
| A. |
加固体丙 |
B. |
加水 |
| C. |
降低温度 |
D. |
蒸发浓缩 |
如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
(1)t2℃时,A物质的溶解度为 。
(2) (填“t1℃”或“t2℃”)时,A、C两物质的溶解度相等;
(3)t2℃时,将30g A物质放入50g水中充分溶解,所得溶液是 (填“饱和溶液”或“不饱和溶液”);
(4)t2℃时,将A、B、C三种物质的饱和溶液分别降温到t1℃,此时所得溶液中溶质的质量分数由大到小的顺序为 。

甲、乙、丙三种固体物质的溶解度曲线如图所示,下列说法正确的是( )

A.甲和丙两种物质的溶解度相等
B.甲的饱和溶液中含有少量的乙,可以用冷却结晶方法提纯甲物质
C.t2℃时,将25g甲物质加入50g水中充分溶解后,所得溶液质量为75g
D.甲、乙、丙三种物质的饱和溶液,温度由t2℃降到t1℃,都有晶体析出
如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,根据如图回答下列问题。
(1)P点的含义是 。
(2)t2℃时,a、b、c三种物质的溶解度由大到小的顺序是 。
(3)t1℃时,将25g a物质加入到100g水中,充分搅拌溶解后恢复到原温度,所得溶液中溶质与溶剂的质量比是 (最简整数比)。
(4)t2℃时,将a、b、c三种物质的等质量的饱和溶液降温至t1℃,下列说法正确的是 。
A.都是饱和溶液
B.溶质质量分数大小关系是:b>a>c
C.析出晶体质量最多的是a
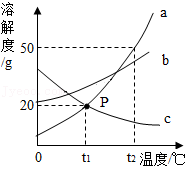
甲、乙、丙三种固体物质的溶解度曲线如图所示,下列相关说法正确的是( )

A.t2℃时甲和丙的溶解度都是60
B.t3℃时,甲、乙、丙三种物质的溶液中溶质质量分数一定是甲>乙>丙
C.将t3℃时甲和丙的饱和溶液降温到t2℃,两溶液的溶质质量分数相等
D.将t2℃时160g甲物质的饱和溶液降温到t1℃可析出20g固体(不含结晶水)
60℃时,向100g水中加入一定量KNO3形成溶液,再降温至20℃,析出固体质量的变化如图1。结合图2,下列说法正确的是( )

A.加入的KNO3质量为41.6g
B.降温过程中KNO3溶液始终为饱和溶液
C.蒸发溶剂可将M点的溶液转化到N点
D.20℃时,100g KNO3饱和溶液中有KNO331.6g
a、b两种固体物质的溶解度曲线如图所示,据图回答:

(1)两种物质中,溶解度随温度升高而减小的是 。
(2)当温度为 ℃时,a和b的溶解度相等。
(3)t2℃时,由图2推测W是图1中的 物质。
试题篮
()