A、B两物质的溶解度曲线如图所示,请根据曲线回答下列问题
(1)、t1℃时,A的饱和溶液中溶质与溶液质量比
(2)、若B中含有少量A,应用 法提纯B;
(3)、若将A的饱和溶液从t2℃降温到t1℃时,一定不会发生改变的是 。
A.溶解度 B.溶剂质量
C.溶质质量 D.溶质质量分数
(4)看下图可知,20 ℃时NaCl的溶解度为36 g,本实验溶解3.6g的粗盐,蒸馏水的最佳使用量约为 ml.增加蒸馏水的用量虽然能加快粗盐的溶解,但会引起的不良后果是 
如图是甲、乙、丙三种固体物质的溶解度曲线图,请回答:
(1)t1℃时,甲物质的溶解度为 g。
(2)乙中有少量甲,提纯乙的方法是 。
(3)将t1℃时丙的饱和溶液升温到t2℃,观察到的现象是 。
(4)t2℃时,等质量甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液质量最小的是 。

无土栽培是现代农业栽培植物的一种方法。无土栽培的植物从营养液中吸取养料和水分。
(1)栽培番茄的某种营养液中含有Ca(NO3)2、KNO3、NH4H2PO4三种物质,依据营养液的成分,其中含番茄生长需要量较大的营养元素是______________(填名称)。
(2)溶解度曲线可以为营养液配制提供相应的数据,下图硝酸钾的溶解度曲线可以提供的信息是 (答一条)。欲配制一定量的KNO3浓溶液以备稀释使用,根据KNO3的溶解度曲线。你认为40℃时,80 kg的KNO3 _______(填“能”或“不能”)溶解在100 kg水中。
(3)将100 kg溶质质量分数为20%的KNO3溶液稀释为4%的KNO3 溶液,用于栽培番茄,需加水_________kg。
甲、乙、丙三种物质的溶解度曲线如图所示。请回答下列问题:
(1)在 0℃~60℃之间,三种物质中溶解度受温度影响最小的是 。
(2)20℃时,三种物质的溶解度由小到大的顺序为 。
(3)在不改变溶液中溶质的质量分数的前提下,要使接近饱和的丙溶液变为饱和溶液,可采取的一种措施是 。
(4)50℃时,将甲、乙、丙各20 g分别加入盛有50 g水的烧杯中,充分溶解,静置,然后各取上层清液m g,再降温至10℃,此时三种溶液中溶质的质量分数分别为ω(甲)、ω(乙)、ω(丙),则三者之间的大小关系是 。

下表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答下列问题:
(1)10℃时,KNO3溶解度是_______g。
(2)60℃时,KNO3的饱和溶液中含有少量NaCl,通过_______方法获得较纯净的KNO3晶体。
(3)T℃时,NaCl和KNO3的饱和溶液溶质的质量分数相同,该温度范围是____。(填序号)
a.10~20℃ b.20~40℃ c.40~60℃ d.60~80℃
(4)向20 mL水中溶解一定量KNO3固体的操作如下图,请根据实验现象和溶解度数据回答:A、B、C中溶液一定是不饱和溶液的是_______。当x=_______g时,B中恰好没有固体剩余。
A、B、C三种固体物质(均不含结晶水)的溶解度曲线如图所示,请回答问题。

(1)t1℃时,三种固体物质的溶解度的大小关系是 。
(2)若B中含有少量的A时,提纯B的方法是 。
(3)t2℃时,将80gA物质放入100g水中,所得溶液中溶质与溶剂的质量比是 (填最简整数比)。
(4)将t2℃时等质量的A、B、C三种物质的饱和溶液,降温到t1℃时所得溶液质量由大到小的顺序是 。
如图是甲、乙、丙三种不含结晶水的固体物质在水中的溶解度曲线,请回答下列问题。
(1)交点P的含义是 。
(2)将乙溶液中的溶质结晶的方法通常是 。
(3)t2℃时,将甲、乙、丙各30g分别充分溶于100g水中,所得溶液质量大小关系为 ,其中 是不饱和溶液。
(4)t1℃时将等质量的甲、乙、丙三种饱和溶液分别升温至t2℃,所得溶液中溶剂的质量大小关系为 。

甲、乙、丙三种物质的溶解度曲线如图所示,回答下列问题:
(1)t1℃时,甲、乙、丙三种物质溶解度由大到小的顺序是 。
(2)t3℃时,将20g物质丙加入50g水中充分溶解,并恢复到原温度,所得溶液的溶质质量分数为 。(结果保留到0.1%)
(3)在不改变溶质质量分数的前提下,将甲的不饱和溶液转化为饱和溶液的方法是 。
(4)下列说法不正确的是 (填字母序号)。
A.t1℃时,用甲、乙、丙三种固体配制等质量的饱和溶液,所需水的质量大小关系是乙>甲>丙
B.t2℃时,甲、丙两物质饱和溶液中所含溶质质量相等
C.将t3℃时的甲、丙的饱和溶液降低温度至t2℃,所得溶液的溶质质量分数相等
D.乙中混有少量甲,可以采用蒸发结晶的方法提纯乙

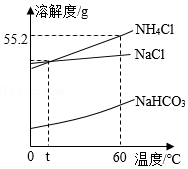
侯德榜先生发明了侯氏制碱法,主要原理及部分操作为:一定条件下,将NH 3、CO 2通入饱和氯化钠溶液,发生反应:NaCl+CO 2+H 2O+NH 3═NaHCO 3↓+NH 4Cl,过滤,滤液中主要含有NH 4Cl、NaCl两种物质,如图为NH 4Cl、NaCl、NaHCO 3三种物质的溶解度曲线。回答下列问题:
(1)60℃时,氯化铵的溶解度是 g。
(2)碳酸氢钠晶体首先从溶液中析出的原因是 。
(3)从滤液中得到氯化铵晶体的操作:蒸发浓缩、 、过滤、洗涤、干燥。
(4)将60℃时氯化铵和氯化钠的饱和溶液各100g分别蒸发掉10g水,然后降温至t℃,过滤,得到溶液甲和溶液乙,下列说法正确的是 (填标号)。
| A. |
甲和乙都是饱和溶液 |
| B. |
溶剂的质量:甲<乙 |
| C. |
溶液的质量:甲>乙 |
| D. |
溶质的质量分数:甲=乙 |
故填:ABD。
氯化钠具有广泛的用途。

(1)生理盐水中的溶剂是 。
(2)生理盐水标签如图1所示。某同学欲配制标签中所标示的生理盐水一瓶,需要水的质量是 g。
(3)氯化钠主要存在于海水中,海水晒盐能够得到粗盐和卤水。卤水中含有MgCl2、KCl和MgSO4等物质,如图2是它们的溶解度曲线。分别将t2℃的MgCl2、KCl和MgSO4三种物质的饱和溶液降温到t1℃时,溶液中溶质质量分数从大到小的关系是 (填写字母序号)。
(4)某同学利用实验探究NaCl在水中的溶解度,所得数据记录如表。
序号 |
温度 |
水质量 |
加入NaCl质量 |
溶液质量 |
① |
20℃ |
25g |
9g |
34g |
② |
20℃ |
50g |
20g |
68g |
③ |
20℃ |
100g |
34g |
134g |
④ |
20℃ |
150g |
54g |
204g |
上述实验中,所得溶液为饱和溶液的是 (填数字序号)。
如图为甲、乙、丙三种固体物质的溶解度曲线,请回答。
(1)t1℃时,甲、乙、丙三种物质的溶解度大小关系是 。
(2)甲中混有少量乙,若要提纯甲,可采取的结晶方法是 。
(3)t2℃时,将50g丙物质放入100g水中充分溶解, 所得溶液中溶质和溶液的质量比为 (填最简整数比)。
(4)t3℃时,将等质量的甲、乙、丙三种物质的饱和溶液分别降温到t1℃,所得溶液的质量由大到小的顺序是 。

如图是甲、乙、丙三种物质的溶解度曲线。

(1)t 1℃时,三种物质的溶解度由大到小的关系为 。
(2)t 2℃时,甲、乙、丙三种物质的饱和溶液降温至t 1℃时为不饱和溶液的是 。
(3)现有含少量甲的乙固体,若要通过结晶法进行提纯乙(甲与乙不发生反应),现有下列实验步骤可供选择:
①取一定量的水将固体溶解②充分冷却后过滤③趁热过滤④加热蒸发至大部分晶体析出⑤加热蒸发至溶液接近饱和⑥停止加热用余热将溶液蒸干⑦用少量水洗涤晶体并烘干。合理的操作顺序为 (按顺序填编号)。
(4)t 3℃时,取等质量甲、乙、丙三种物质的饱和溶液,恒温蒸发一定质量的水(析出的晶体均不含结晶水),析出晶体的质量关系为甲=乙<丙,则剩余溶液的质量由大到小的关系为 。
(5)t 2℃时,配制甲、乙、丙三种物质的饱和溶液,一定相等的是 (填字母)。
A.溶质质量
B.溶剂质量
C.溶质质量分数
D.溶解度
KNO3和KCl的溶解度曲线如图所示:
(1)t3℃时,KNO3的溶解度为 。
(2)将t3℃时KCl的饱和溶液70.0g稀释成质量分数为20.0%的KCl溶液,需加水 g(精确到0.1g)。查阅相关物质的密度后,在实验室完成该实验通常需要的仪器有烧杯、量筒、 (填字母标号)。
A.托盘天平 B.药匙 C.胶头滴管 D.玻璃棒
(3)现有t2℃时KNO3的饱和溶液m1g和KCl的饱和溶液m2g.不考虑水的蒸发,下列关系一定成立的是 (填字母标号)。
A.两溶液中溶质的质量分数相等
B.分别降温到t1℃,析出KNO3的质量大于析出KCl的质量
C.分别升温至t3℃,所得溶液中溶质的质量分数相等
D.保持t2℃不变,分别加入等质量的水,混匀后所得溶液中溶质的质量分数相等

甲、乙两种固体物质的溶解度曲线如图所示,据图回答下列问题:
(1)乙物质的溶解度随温度的升高而 (填“增大”或“减小”).
(2)欲将t1℃甲物质的不饱和溶液变为该温度下的饱和溶液,可采取的方法: (任填一种).
(3)若甲物质中混有少量乙物质,可用 的方法提纯甲.
(4)等质量甲、乙两种物质分别配成t2℃时的饱和溶液,需要水的质量大小关系是
甲 乙(填“>”、“=”或“<”).

试题篮
()