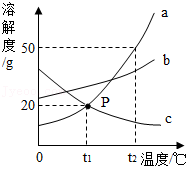
如图是a、b、c三种物质的溶解度曲线,回答下列问题。
(1)P点的含义是 。
(2)t2℃时,将60g a物质加入到100g水中,充分溶解后,所得溶液中溶质与溶液的质量比是 。
(3)t2℃时,要使接近饱和的c溶液变为饱和溶液,采用的方法是 。
(4)t2℃时,等质量的a、b、c三种物质的饱和溶液中溶质的质量分数由大到小的顺序为 。
根据NaCl和KNO3的溶解度数据表,回答下列问题:
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
|
溶解度/g |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
|
(1)10℃时,NaCl的溶解度是 g;
(2)30℃时,溶解度较大的是 (选填“NaCl”或“KNO3”);
(3)下列分析正确的是 。
A.10℃时,能够配制出溶质的质量分数为20.9%的KNO3溶液
B.20℃时,20g NaCl固体加入100g水,充分溶解后得到NaCl的不饱和溶液
C.20℃到30℃之间,能配制出溶质质量分数相等的NaCl饱和溶液和KNO3饱和溶液
D.将KNO3溶液经过某种操作后,析出KNO3晶体,过滤后所得溶液溶质的质量分数与原溶液相比,可能变大、变小或不变
我国制碱工业先驱侯德榜发明了"侯氏制碱法",促进了世界制碱技术的发展。其主要化学反应原理如下:
NH 3+CO 2+H 2O═NH 4HCO 3 ①
NaCl+NH 4HCO 3═NaHCO 3↓+NH 4Cl ②
x NaHCO 3  Na 2CO 3+CO 2↑+H 2O ③
Na 2CO 3+CO 2↑+H 2O ③
已知NaCl、NaHCO 3和NH 4Cl在不同温度下的溶解度数据如下表:
| 温度(℃) |
0 |
10 |
20 |
30 |
40 |
|
| 溶解度/g |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
| NaHCO 3 |
6.9 |
8.1 |
9.6 |
11.1 |
12.7 |
|
| NH 4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
|
请回答下列问题:
(1)反应①的基本反应类型属于 反应。
(2)反应②产生的NH 4Cl在农业生产中常用作 (选填"氮肥"、"磷肥"或"钾肥")。
(3)反应③中的化学计量数x= 。
(4)20℃时,反应②中的生成物溶解度较小的是 (填化学式)
(5)20℃时,将NaCl和NaHCO 3的饱和溶液各100g,分别加热蒸发20g水,再恢复至原温度,析出晶体并得到溶液,对于所得溶液下列说法正确的是 (填序号)
A、所得溶液仍是饱和溶液
B、所得溶液的质量前者大于后者
C、所得溶液的溶质质量分数都增大
试题篮
()