化学是从宏观和微观两个视角认识物质的,请按要求回答问题:
(1)氧气从宏观视角看,是由 组成的;从微观视角看,是由 构成的。
(2)在化学反应前后,肯定不变的是 。
A.原子的种类 B.分子的种类
C.物质的种类 D.元素的种类
(3)用化学用语书写:①1个铜原子 ②氧化镁
(4)依据图示回答:A、B、C、D表示4种物质,其微观示意图如下所示,A和B在一定条件下反应生成C和D。
①1个B分子中含 个原子;
②该化学反应的反应类型是 。
氮化镁是一种应用范围非常广泛的无机化合物,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物,制备特殊的陶瓷材料等。某校化学研究小组用镁与氮气反应制备氮化镁(Mg3N2),并用实验方法测定氮化镁的纯度。
I.制备氮化镁
【查阅资料】
①(NH4)2SO4+2NaNO2 2N2↑+Na2SO4+4H2O,该反应为放热反应。
2N2↑+Na2SO4+4H2O,该反应为放热反应。
②饱和硫酸亚铁溶液能吸收氧气;稀硫酸能吸收氨气。
③在常温下或温度不高的条件下镁几乎与水不反应。
【实验】
制备氮化镁的装置示意图如下:
(1)D装置的作用是 ,G装置的作用是 。
(2)E装置中发生反应的化学方程式为 。
(3)实验时先进行 (选填“A”或“E”)处加热,理由是 。
II.测定氮化镁的含量
氮化镁是浅黄色粉末,极易与水反应生成Mg(OH)2沉淀和NH3,反应的化学方程式为 ,氮化镁(Mg3N2)中氮元素的化合价是 。
【定性分析】
步骤一:取少量氮化镁样品于试管中,加足量蒸馏水,试管底部有沉淀生成,试管口闻到有刺激性气味的气体生成。
步骤二:弃去上层清液,加入稀盐酸,观察到沉淀全溶且冒气泡。该步骤中产生气泡的化学方程式为 。
【定量测定】
按下图实验装置进行实验:
(4)取氮化镁样品16g进行实验,I装置增重3.4g,求该样品中氮化镁的质量分数(请写出计算过程)。
(5)球形干燥管的作用是 。
某化学课外小组同学,用如图所示实验验证质量守恒定律。
(1)某甲同学用A装置探究质量守恒定律,实验步骤如下:如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使硫酸铜溶液与铁钉接触,一段时间后,再把烧杯放在天平上。
①烧杯内反应的实验现象为
②最后天平的指针(填序号) (a.偏左 b.偏右 c.不偏转 d.无法预测)。
(2)①乙同学用B装置研究质量守恒定律,实验步骤如下:
将烧杯放在天平上用砝码平衡,然后倾斜烧杯使盐酸与碳酸钠粉末接触,一段时间后再把烧杯放在天平上,发现天平的指针 (a.偏左 b.偏右 c.不偏转 d.无法预测),该反应 (填符合或不符合)质量守恒定律。
②若将本实验中的烧杯替换成带有气球的锥形瓶,如图所示
其他操作不变,装置气密性良好,最后天平仍不平衡,仍不平衡的原因 。可见,在验证质量守恒定律时,若利用有气体参加或有气体生成的化学反应来设计实验,在装置设计方面应做到 。
空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应.图1是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程.请按要求回答下列问题:
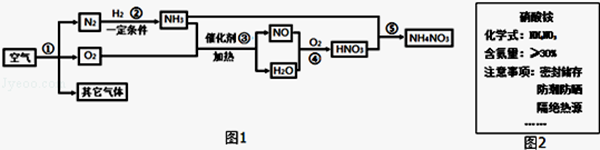
(1)步骤①中发生的是 变化(填“物理”或“化学”).
(2)写出步骤③中发生反应的化学方程式 .
(3)图2是化肥硝酸铵包装袋上的部分说明:硝酸铵应具有的性质是 (填字母).
A.易溶于水 B.有挥发性 C.受热易分解
化学是研究物质组成、结构、性质及其变化规律的基础自然科学,请回答:
(1)从组成角度看:氯化钠是由 组成.
(2)从微粒角度看:氯化钠是由 构成(用微粒符号表示).
(3)从制备角度看:将海水进行 可得到粗盐.除去粗盐中含有的SO42﹣、Ca2+、Mg2+等杂质,常加入过量的①Na2CO3溶液、②BaCI2溶液、③NaOH溶液,三种试剂的加入顺序为 (填序号),然后再加适量的盐酸.
有一包固体粉末,可能是NaOH、Na2SO4、MgCl2、CuSO4中的一种或几种组成,为了分析固体粉末的成分,取少量该固体粉末进行实验,实验方案设计如下:
(1)固体粉末中一定有 ,一定没有 .
(2)若现象X为“沉淀不溶解”或“沉淀部分溶解”,结论是固体粉末中 ;若现象X为“沉淀全部溶解”,结论是固体粉末中 。
(3)实验步骤①和③都有相同的实验操作,该操作名称为 。
(4)写出实验步骤②的化学方程式 。
(5)简单修改上述实验方案,可取消第④步实验,修改的方法是 。
金属钠很软,可以用刀切割。切开外皮后,可以看到钠具有银白色的金属光泽。钠的密度是0.97g/cm3,比水的密度小,钠的熔点是97.81℃,沸点是882.9℃。将金属钠放入水中,可以反应生成NaOH和H2;钠跟氧气混合加热生成淡黄色的过氧化钠(Na2O2)固体,钠跟CO2在加热条件下反应生成碳酸钠和单质碳。
(1)请写出金属钠的两点物理性质_________________________________
(2)分别写出钠跟水、氧气、CO2反应的化学方程式:
钠跟水:_________________________________
钠跟氧气:_________________________________
钠跟CO2:_________________________________
(1)下列氮肥含氮量由高到低的排列顺序是:(用序号表示)
| 常见氮肥 |
①
|
②
|
③
|
| 相对分子质量 |
80 |
79 |
60 |
(2)治理汽车尾气中的
和
的一种方法是:在汽车的排气管上装一个催化转化装置。使
和
反应生成
和
,写出该反应的化学方程式。
(3)有机物中碳氢化合物可用
表示,其完全燃烧的化学方程式:
判断等质量的①
,②
,③
,三种碳氢化合物完全燃烧消耗氧气由大到小的顺序是 (用序号表示)。
现有以下6个变化:
①在点燃的条件下,氢气在氧气中燃烧;
②给水通直流电
③锌加入稀硫酸溶液中;
④氢氧化钠溶液与稀盐酸混合
⑤冷却硝酸钾热饱和溶液析出硝酸钾晶体;
⑥日本福岛第一核电站发生核反应,铀235裂变产生碘131
请回答下列问题:
(1)探究化学变化的规律始终是化学科学的核心任务。上述变化中,属于化学变化的是(填变化的代号,下同)_______________,属于物理变化的是______________;
(2)化学变化也叫化学反应,在上述化学反应中,属于分解反应的有________________,属于复分解反应的有________________,将化学反应分为分解反应、化合反应、复分解反应和置换反应等四种基本反应类型的依据是_________________________、
(3)我们知道,能直接构成物质的微粒有分子、原子、离子。物质之所以发生化学反应,从微观的角度看,是因为反应物的微粒之间在一定条件下发生有效的相互作用,使微粒的结构发生改变,或微粒重新排列组合,宏观上表现为生成了新的物质。
在反应①中,发生有效相互作用的微粒是(写出微粒的符号)___________________。
反应的化学方程式为___________________________________________________
发生有效相互作用而促使反应发生的微粒是(写出微粒符号)__________________,微粒的转化过程是________________________________________________________________,
在反应④中,发生有效的相互作用而促使反应发生的微粒是(写出微粒的符号)____________
现欲探究一固体混合物A的成分,已知其中可能含有NH4Cl、Cu(OH)2、BaSO4、CaO、NH4 NO3五种物质中的两种或多种。按下图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应均恰好完全反应)
试根据实验过程和发生的现象判断:
(1)常温下,气体B的水溶液显_________(填“酸性”“中性”“碱性”之一)。
(2)滤渣D的化学式是_________________。
(3)固体混合物A中,一定存在的物质是(写化学式)___________________________。
(4)滤液C中,一定大量存在的金属离子是(写离子符号)________________________。
(5)写出过程③中可能发生的一个化学方程式: 。
(6)固体混合物A中还不能确定存在的物质是(写化学式) ,得出此结论的理由是 。
鸡蛋腐败会发出一种无色、有臭鸡蛋气味的气体(H2S).硫化氢气体是一种大气污染物,它在空气中点燃能完全燃烧生成二氧化硫和水,把硫化氢气体通入浓硫酸中,发生的反应为:H2S+H2SO4(浓)=SO2+S↓+2H2O
(1)从上述叙述中,归纳出硫化氢的物理性质:① 、② ;硫化氢的化学性质是:① 、② .
(2)若工厂排放的尾气中含有硫化氢,用浓硫酸来吸收是否可以? ,原因是 .
(2分)下图为某化学反应的微观过程,其中“ ”和“
”和“ ”表示两种不同原子。
”表示两种不同原子。

(1)该反应属于 (填基本反应类型)反应。
(2)虚线框内应填的微观图示是 (选填A、B、C、D)。

为了测定某含杂质7%的黄铜样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验:

(1)配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是;
(2)发生反应的化学方程式为;
(3)根据已知条件列出求解100g该黄铜样品中锌的质量(x)的比例式为;
(4)该黄铜样品中铜的质量分数是;
(5)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数是;
(6)欲将黄铜样品中的铜转化为铜盐,可将过滤后所得的不溶性物质洗涤、烘干,然后在空气中加热,充分反应,则可得到含杂质的氧化铜的质量是,再经过某些反应及操作就得到了所需铜盐。
草酸是一种酸,草酸晶体(H2C2O4•2H2O)易溶于水,熔点较低,加热会熔化、气化和分解。草酸(H2C2O4)与氢氧化钙的反应:H2C2O4 + Ca(OH)2= CaC2O4↓(白色)+ 2H2O。
【分析讨论】
(1)草酸的水溶液的pH 7(填“>”、“=”、“<”)
(2)实验室可用加热草酸晶体分解的方法获得CO
①先加热草酸晶体生成CO、CO2和H2O,其化学方程式是 ;
②再将生成的混合气体通过NaOH溶液吸收CO2,其化学方程式是 ;
③最后用下图装置收集CO,气体应从 端进入(选填“a”或“b”)。
【实验反思】
(3)甲认为下图中试管口应略向下倾斜,老师、同学讨论后一致认为装置是正确的,理由是 。
(4)实验中观察到澄清石灰水变浑浊,乙认为一定是由草酸晶体受热分解产生的CO2所导致,丙认为乙的结论不严密,理由是 。
【生活链接】菠菜营养丰富,但菠菜豆腐同食,易得结石(主要成分:草酸钙晶体),小组同学对草酸钙晶体的性质及组成产生了兴趣。
【性质探究】按下图装置将草酸钙晶体(CaC2O4·xH2O)样品高温加热,使其完全分解并检验产生的气体。
【问题讨论】
(5)B中观察到 现象,说明反应生成了水;
(6)C、G中澄清石灰水均变浑浊,说明反应还生成 和 气体。
(7)反应开始前通入氮气的目的是 。
【组成确定】
(8)利用热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,获得相关数据,绘制成固体质量—分解温度的关系如图。
①温度为200℃左右时,晶体全部失去结晶水,晶体中结晶水的质量为 g。
②计算CaC2O4·xH2O中的x(CaC2O4的相对分子质量:128),x = 。
③800℃以上时,经检验残留固体为氧化物,图中m的值是 。
④写出固体质量由12.8g变为10.0g时的化学方程式 。
水是生命之源,也是化学实验中的一种重要物质,下列实验都与水有关。

(1)图22实验中,水发生的是变化;图23实验中,水发生的是变化(填"物理"或"化学")。水的电解实验得到氢气、氧气,证明了水由氧、氧两种元素组成,其本质原因是。
(2)图24是氯化钠和硝酸钾的溶解度曲线,从图中你能得到的信息有(只写一条)。
(3)某同学做了如下两个实验。

根据图24的溶解度曲线,判断a~f对应的溶液中,为饱和溶液的是。
(4)由实验1、2可知,使不饱和溶液转化为饱和溶液的方法有。
试题篮
()